Clear Sky Science · fr
Double estérification catalysée par un carbène permettant le verrouillage conformationnel énantiosélectif des pillar[5]arènes
Façonner de petits anneaux pour des matériaux intelligents
Les chimistes apprennent à sculpter les molécules presque comme des horlogers façonnent des engrenages. Cette étude montre comment « verrouiller » une petite molécule annulaire dans une configuration de type main, en utilisant un catalyseur simple et des réactifs courants. Parce que ces anneaux peuvent accueillir d’autres molécules, ce contrôle inédit de la forme pourrait influencer les capteurs, matériaux et outils médicaux de demain.
Pourquoi la forme d’un anneau compte
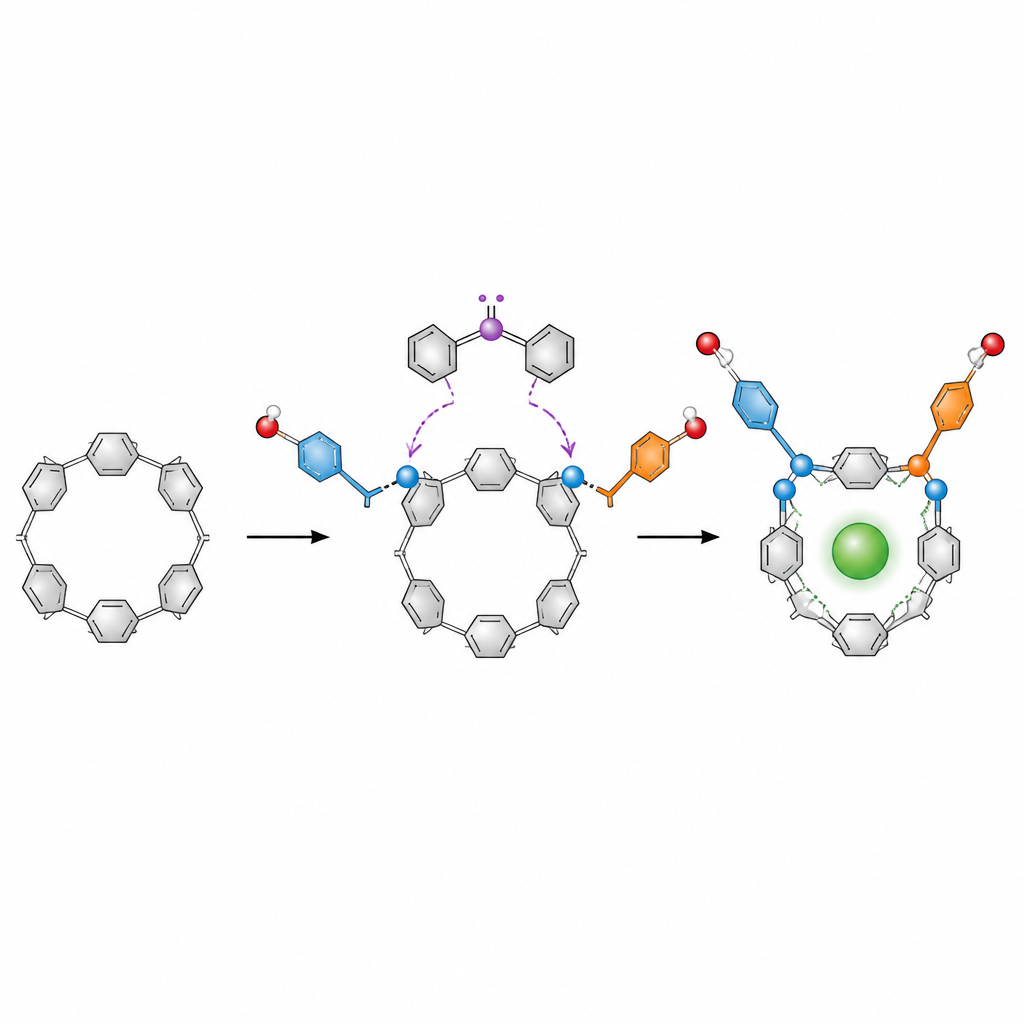
Les protagonistes de cette histoire sont les pillar[5]arènes, des anneaux en forme de beignet construits à partir de cinq unités aromatiques répétées. Ces anneaux sont prisés en chimie hôte‑invité, où ils jouent le rôle de minuscules conteneurs pour des ions, des médicaments ou des colorants. Sur le papier, une pillar[5]arène peut basculer entre plusieurs formes images‑miroir qui s’échangent continuellement. Pour les utiliser comme outils précis, il faut figer une forme « chirale » et favoriser une image miroir par rapport à l’autre, mais les méthodes existantes reposent souvent sur des métaux, de multiples étapes et des séparations fastidieuses des mélanges.
Un raccourci sans métal pour des anneaux verrouillés
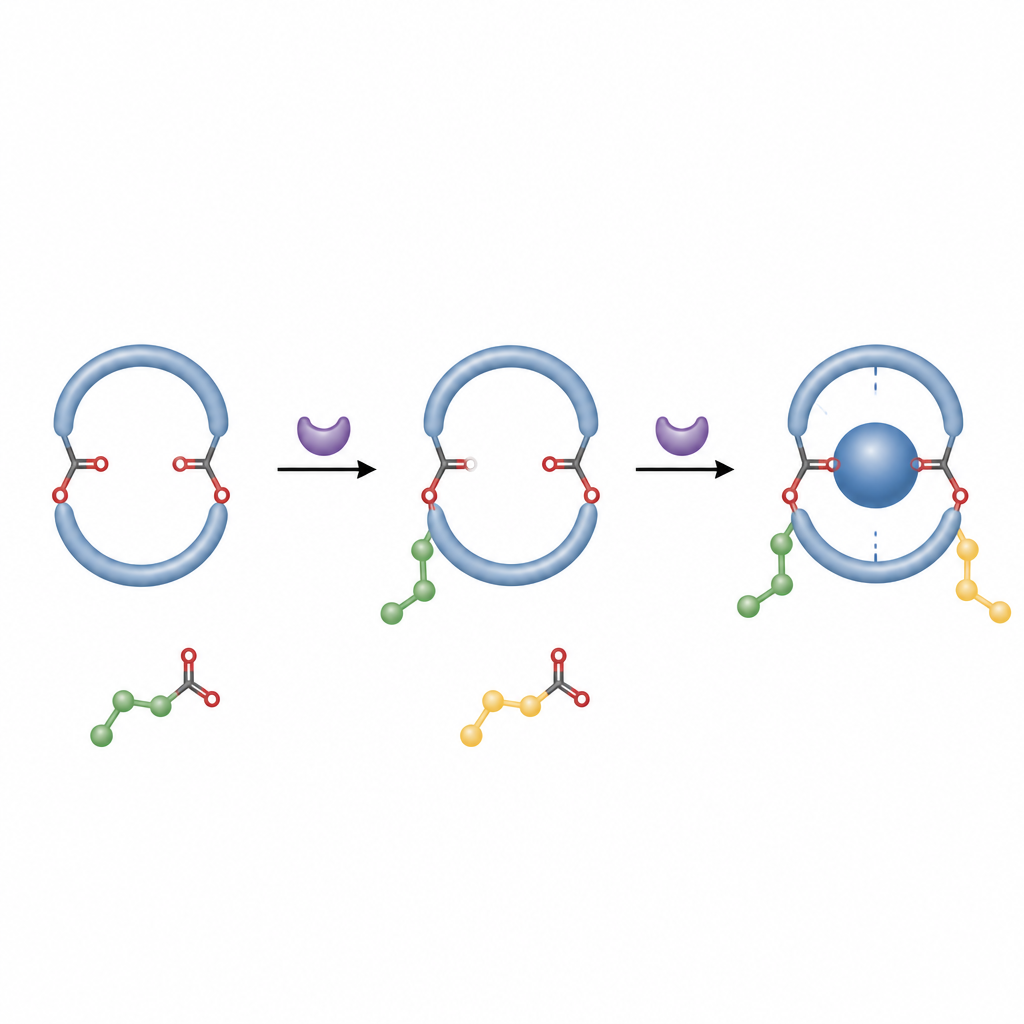
Les auteurs ont conçu une approche beaucoup plus simple basée sur l’organocatalyse, qui utilise de petites molécules organiques au lieu de métaux pour diriger les réactions. Ils sont partis d’une pillar[5]arène diformylée, une version de l’anneau portant deux groupes aldéhyde réactifs. En présence d’un catalyseur carbène chiral, d’un oxydant et d’une base, ces groupes subissent une double estérification avec des alcools aromatiques tels que les naphtols. Chaque réaction fixe un « bras » ester sur l’anneau. Une fois deux bras volumineux en place, l’anneau ne peut plus basculer librement : une forme chirale devient bloquée et fortement favorisée.
Ajuster la portée de la réaction
Par des tests systématiques, l’équipe a identifié des conditions donnant à la fois de hauts rendements et une nette préférence pour une image miroir. Ils ont examiné comment la nature du catalyseur, du solvant, de la base et de l’oxydant influence le résultat, et ont constaté que l’acétate de sodium en dichlorométhane à température modérée fonctionne particulièrement bien. Le procédé tolère de nombreux partenaires aromatiques différents, y compris des naphtols porteurs de groupes donneurs ou attracteurs d’électrons et une gamme de phénols. À l’aide d’une analyse stérique astucieuse, ils ont montré que seuls des substituants suffisamment longs et volumineux empêchent réellement le basculement de l’anneau, ce qui explique pourquoi de petits groupes comme le méthyle ne produisent pas de produits chiraux stables.
Des anneaux simples à des invités complexes
La méthode va au‑delà des blocs de construction simples. Les chercheurs ont réussi à fixer des fragments issus de molécules naturelles et bioactives, telles que l’estrone et le médicament hypocholestérolémiant ézétimibe, tout en conservant un fort contrôle de la « main ». Ils ont en outre montré que les anneaux verrouillés résistent à la chaleur et aux modifications chimiques sans perdre leur pureté chirale. À l’échelle du gramme, le produit clé se forme avec un rendement presque quantitatif. Des réactions supplémentaires sur les groupes fonctionnels restants permettent d’obtenir des structures plus complexes, y compris un rotaxane, dans lequel une molécule en forme d’haltère est enfilée à travers l’anneau de pillar[5]arène et piégée par des cales volumineuses.
Ce que cela signifie pour les machines moléculaires futures
En termes simples, les auteurs ont trouvé un moyen d’immobiliser un anneau moléculaire dans une pose fixe gauche ou droite en utilisant un procédé simple et sans métal. Cela facilite grandement la préparation d’hôtes purs et définis par leur forme, capables d’agripper d’autres molécules de façon prévisible. Ce contrôle de l’énantiosélectivité et de la stabilité est crucial pour la conception de matériaux réactifs, de capteurs chiraux et de dispositifs moléculaires, et cette double estérification directe offre une nouvelle voie pratique vers ces architectures avancées.
Citation: Dočekal, V., Hladík, O., Lóška, L. et al. Carbene-catalyzed double esterification enables enantioselective conformational self-locking of pillar[5]arenes. Nat Commun 17, 4253 (2026). https://doi.org/10.1038/s41467-026-70809-1
Mots-clés: pillararenes, organocatalyse, hôtes chiraux, estérification, chimie supramoléculaire