Clear Sky Science · it
La doppia esterificazione catalizzata da carbene consente il bloccaggio conformazionale enantioselettivo delle pillar[5]arene
Plasmare anelli minuscoli per materiali intelligenti
I chimici stanno imparando a scolpire le molecole quasi come orologiai che sagomano gli ingranaggi. Questo studio mostra come “bloccare” una piccola molecola ad anello in una sola forma destrorsa o sinistrorsa, usando un catalizzatore semplice e reagenti comuni. Poiché tali anelli possono accogliere altre molecole, questo nuovo controllo sulla forma potrebbe influenzare futuri sensori, materiali e strumenti medici.
Perché la forma di un anello conta
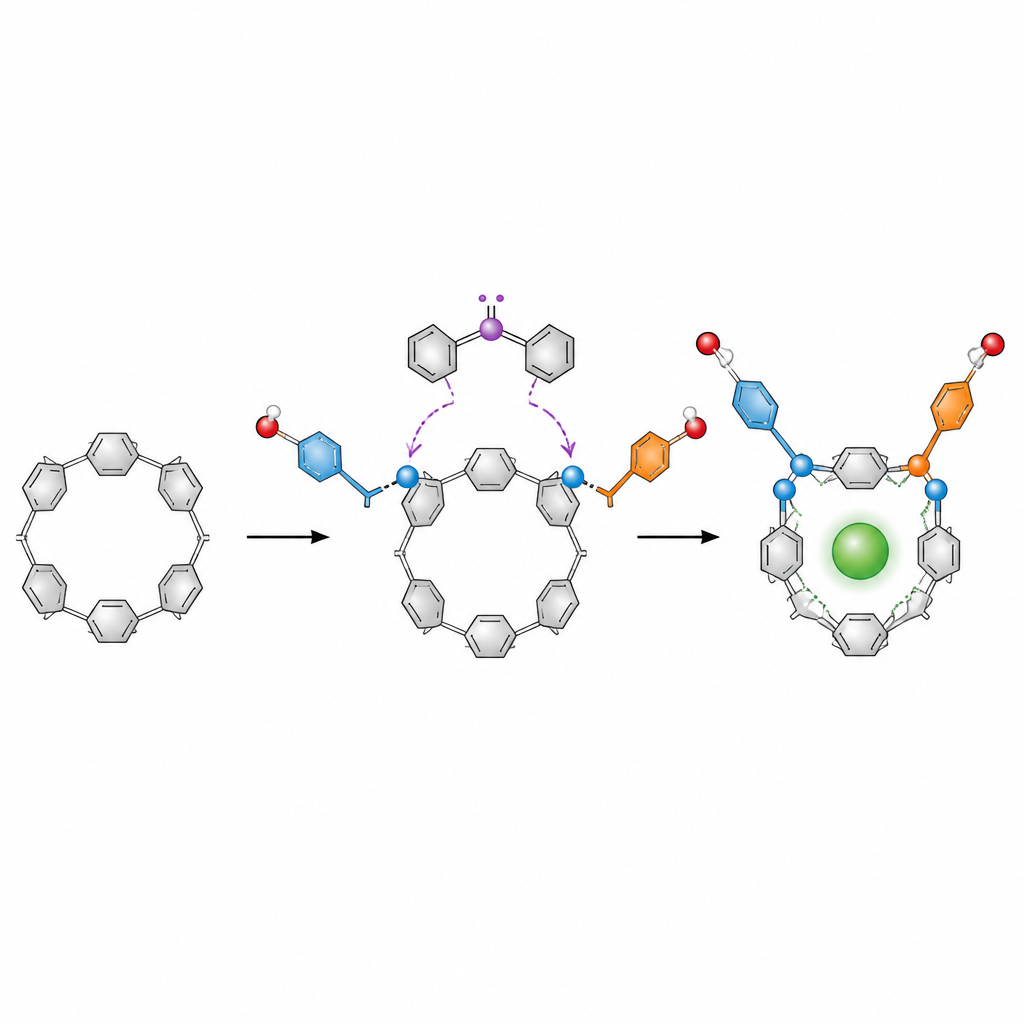
Le protagoniste sono le pillar[5]arene, anelli a forma di ciambella costruiti da cinque unità aromatiche ripetute. Questi anelli sono molto usati nella chimica host–guest, dove agiscono come piccoli contenitori per ioni, farmaci o coloranti. In teoria, una pillar[5]arene può ruotare in diverse forme immagine‑speculare che si interconvertono. Per usarle come strumenti precisi, i chimici devono fissare una forma “enantionera” in posizione e arricchire un’immagine speculare rispetto all’altra, ma i metodi esistenti spesso si basano su metalli, più passaggi e laboriose separazioni di miscele.
Una scorciatoia senza metalli per anelli bloccati
Gli autori hanno ideato un approccio molto più semplice basato sull’organocatalisi, che usa piccole molecole organiche al posto dei metalli per indirizzare le reazioni. Sono partiti da una pillar[5]arene diformilica, una versione dell’anello con due gruppi aldeidici reattivi. In presenza di un catalizzatore carbene chirale, un ossidante e una base, questi gruppi subiscono una doppia esterificazione con alcoli aromatici come i naftoli. Ogni reazione attacca un “braccio” estere all’anello. Una volta che due bracci ingombranti sono installati, l’anello non può più ruotare liberamente, quindi una forma chirale viene bloccata e fortemente favorita.
Regolare l’estensione della reazione
Attraverso test sistematici, il gruppo ha individuato condizioni che danno sia rese elevate sia una forte preferenza per una delle immagini speculari. Hanno esaminato come la natura del catalizzatore, del solvente, della base e dell’ossidante influenzi il risultato, e hanno scoperto che l’acetato di sodio in diclorometano a temperatura moderata funziona particolarmente bene. Il processo tollera molti diversi partner aromatici, inclusi naftoli con gruppi elettron‑donatori o elettron‑attrattori e una gamma di fenoli. Usando un’analisi sterica intelligente, hanno mostrato che solo i sostituenti abbastanza lunghi e voluminosi impediscono veramente il ribaltamento dell’anello, il che spiega perché gruppi piccoli come il metile non producono prodotti chirali stabili.
Da anelli semplici a ospiti complessi
Il metodo va oltre i semplici mattoni di costruzione. I ricercatori hanno attaccato con successo frammenti tratti da molecole naturali e bioattive, come l’estrone e il farmaco ipocolesterolemizzante ezetimibe, mantenendo al contempo un elevato controllo della “maneggiabilità” (enantioselettività). Hanno inoltre dimostrato che gli anelli bloccati resistono al calore e a modifiche chimiche senza perdere la loro purezza chirale. Su scala di grammi, il prodotto chiave si forma con resa quasi quantitativa. Reazioni aggiuntive sui gruppi funzionali residui creano strutture più complesse, inclusa una rotaxane, in cui una molecola a manubrio attraversa l’anello di pillar[5]arene ed è intrappolata da tappi ingombranti.
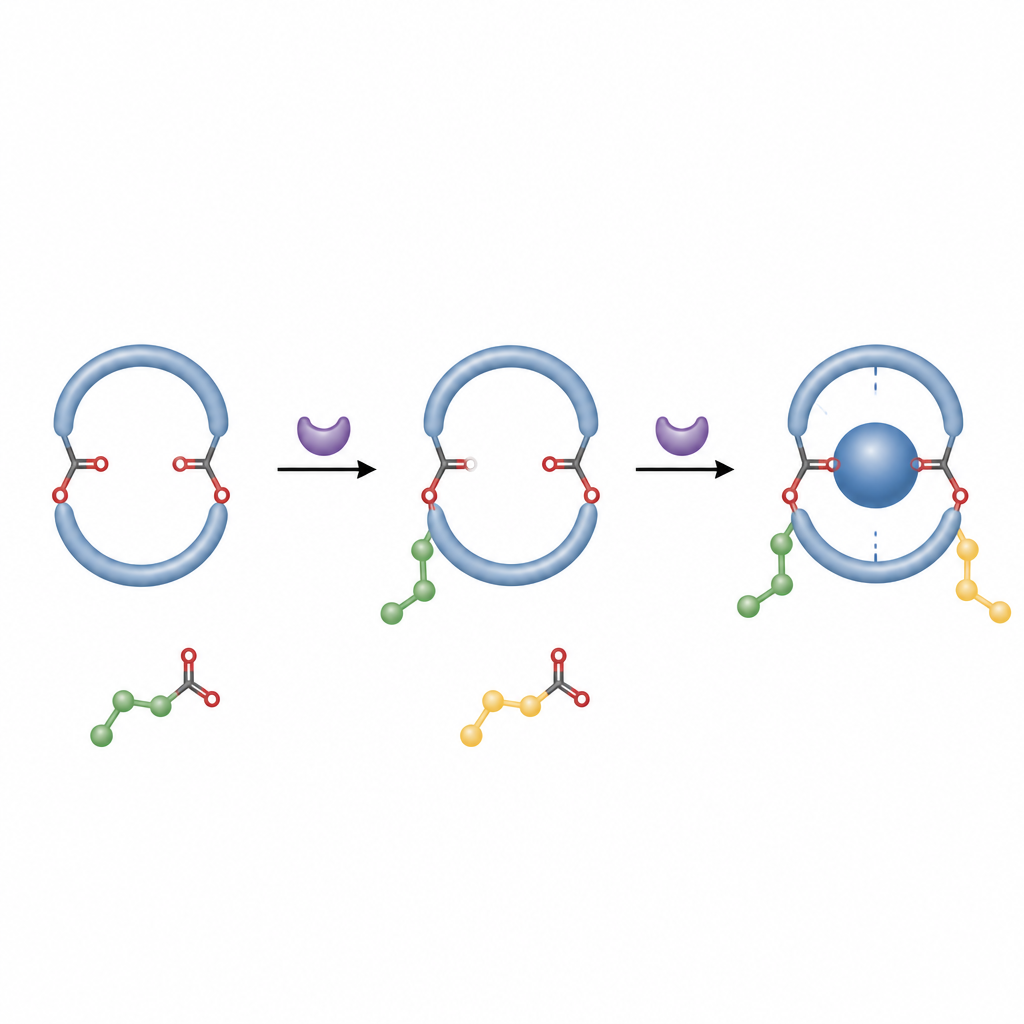
Cosa significa per le future macchine molecolari
In termini pratici, gli autori hanno trovato un modo per fissare un anello molecolare in una posa destra o sinistra usando un processo semplice e senza metalli. Questo rende molto più facile preparare ospiti puri e definiti nella forma che possono afferrare altre molecole in modi prevedibili. Tale controllo sull’enantiomero e sulla stabilità è importante per progettare materiali reattivi, sensori chirali e dispositivi molecolari, e questa diretta doppia esterificazione offre una nuova via pratica verso quelle strutture avanzate.
Citazione: Dočekal, V., Hladík, O., Lóška, L. et al. Carbene-catalyzed double esterification enables enantioselective conformational self-locking of pillar[5]arenes. Nat Commun 17, 4253 (2026). https://doi.org/10.1038/s41467-026-70809-1
Parole chiave: pillararenes, organocatalysis, chiral hosts, esterification, supramolecular chemistry