Clear Sky Science · ru
Понижение триптофана может способствовать побочным эффектам напроксена
Почему обычные обезболивающие важны для всего организма
Миллионы людей принимают нестероидные противовоспалительные препараты (НПВП), такие как напроксен, при головных болях, боли в суставах или травмах, часто полагая, что они безвредны и доступны без рецепта. Однако эти препараты могут незаметно повышать риск желудочного кровотечения и сердечных проблем. В этом исследовании поставлен простой, но важный вопрос: как эти лекарства меняют химию организма и может ли природный нутриент триптофан помочь объяснить — и, возможно, смягчить — часть их скрытых опасностей?
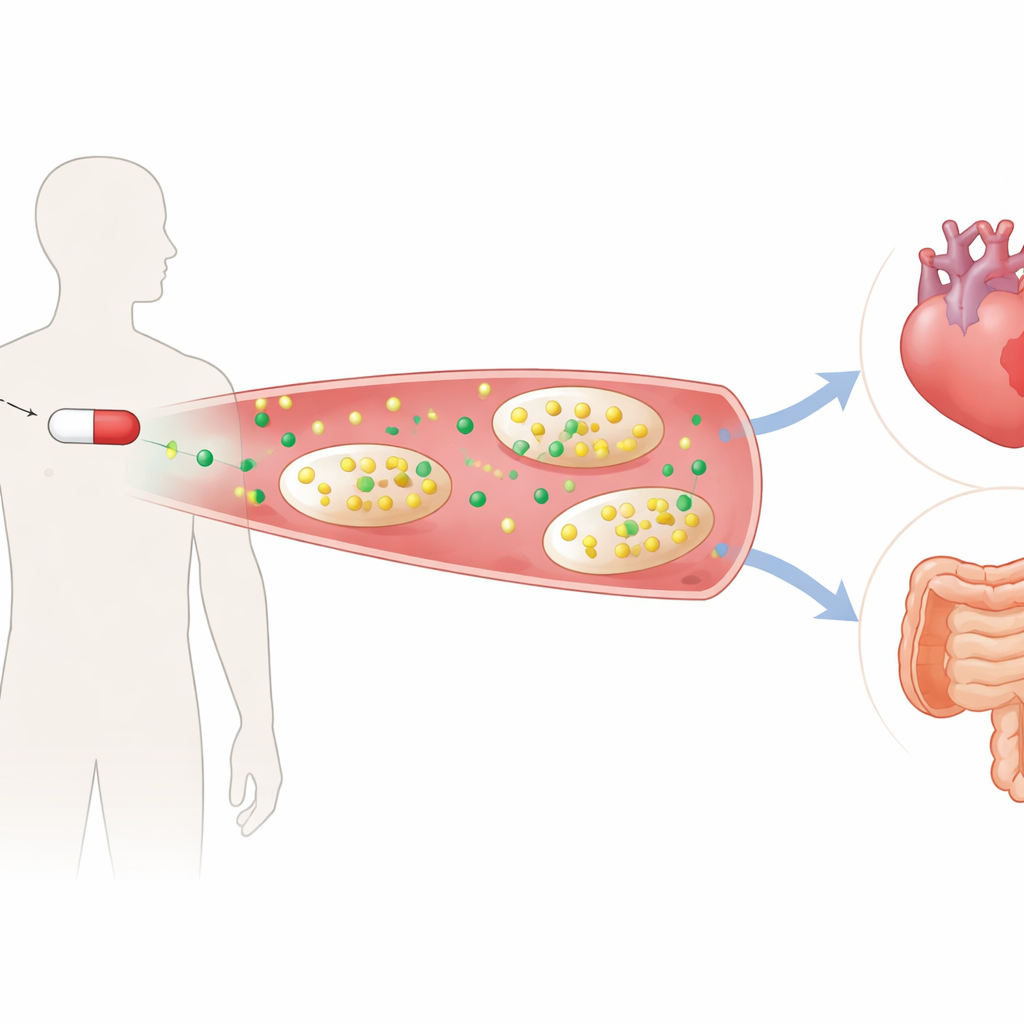
Более пристальный взгляд на два похожих обезболивающих
Исследователи сравнили напроксен, традиционный НПВП, блокирующий два родственных фермента, с целекоксибом — более новым препаратом, нацеленным только на один из них. Шестнадцать здоровых добровольцев получали каждое лечение — напроксен, целекоксиб или плацебо — на протяжении недели в тщательно контролируемом перекрёстном исследовании. Затем образцы крови и мочи анализировали с помощью детального химического профилирования, чтобы увидеть, как изменяются тысячи малых молекул в ответ на препараты. Хотя оба лекарства успешно снижали уровни жирнокислотных медиаторов боли и жара, напроксен выделялся тем, что вызывал заметное падение триптофана и его основного продукта распада — кинуренина, тогда как целекоксиб этого не делал. Такая картина указывала на то, что напроксен нарушает важный метаболический путь за пределами своей целевой активности.
Неожиданная роль обычной аминокислоты
Триптофан наиболее известен как строительный блок для белков и некоторых мозговых нейромедиаторов, но он также питает сеть путей, связанных с иммунитетом, артериальным давлением и энергетическим обменом. У людей и у мышей напроксен последовательно снижал циркулирующие уровни триптофана и кинуренина, оставляя при этом другие родственные молекулы в основном неизменными. Последующие эксперименты показали, что этот эффект не зависел от блокировки ферментов, которые напроксен предназначен ингибировать. Даже мыши, генетически лишённые этих ферментов, теряли триптофан при приёме препарата. Вместо этого напроксен, по-видимому, конкурировал непосредственно с триптофаном за связывание с альбумином — крупным белком крови, который транспортирует многие молекулы по организму. Крепче прилипая к этим сайтам, напроксен вытеснял триптофан и кинуренин с белка в циркуляцию, где их легче расщепляли и выводили.
Вступление в игру микробов кишечника и воспалённых органов
Команда также изучила, как это химическое смещение может распространяться по организму. У людей и у мышей лечение напроксеном тонко меняло микробиом кишечника, способствуя росту отдельных групп бактерий, ранее связанных с превращением триптофана в индольные соединения. Одновременно у мышей, получавших напроксен, наблюдались небольшие, но показательные признаки вреда: больше скрытой крови в стуле и активность генов в сердце и кишечнике, указывающая на воспаление и повреждение тканей. Многие из этих сигналов тревоги восходили к путям, вызванным иммунным медиатором IL-1β, и к молекулярному комплексу, называемому инфламмасомой, которые вовлечены в серьёзные сердечно-сосудистые и кишечные заболевания.
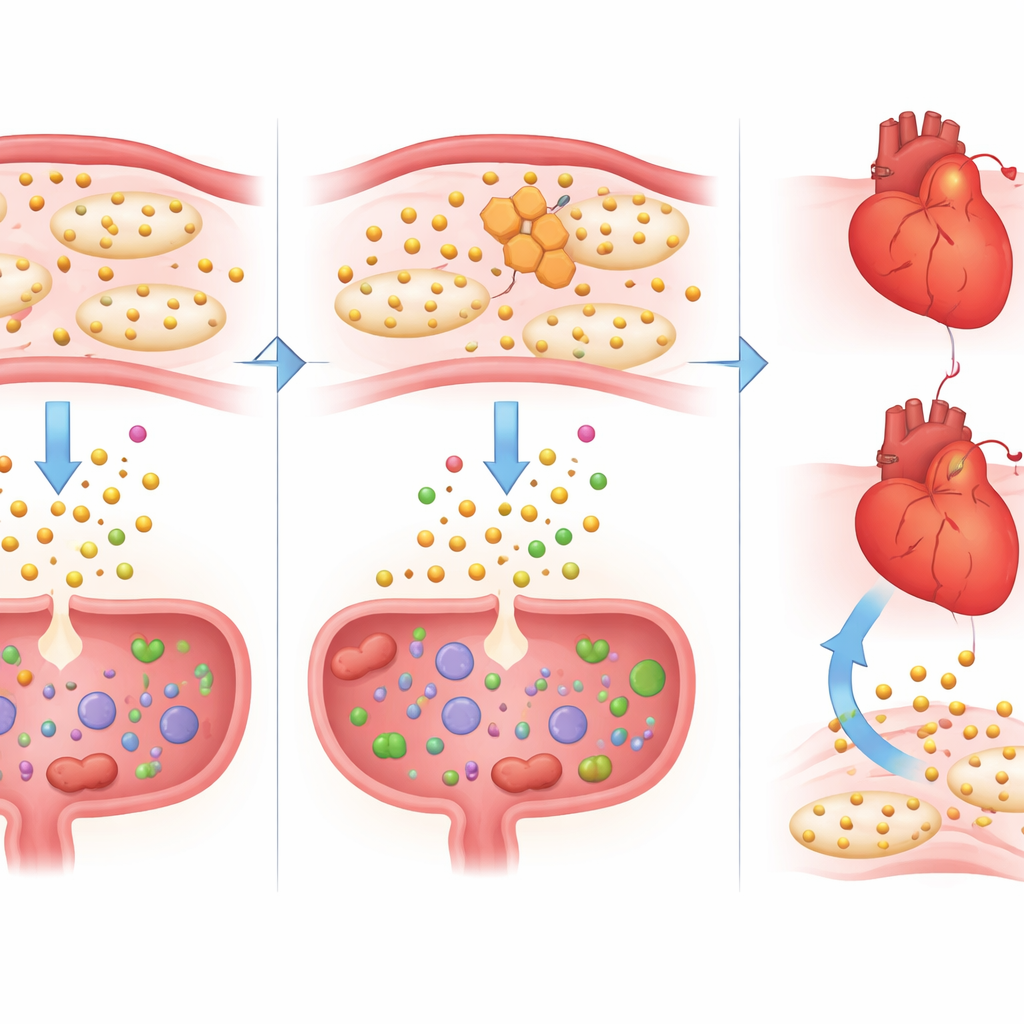
Восстановление баланса при дополнительном приёме триптофана
Чтобы проверить, является ли потеря триптофана частью проблемы, а не безвредным побочным эффектом, учёные дали некоторым мышам, получавшим напроксен, контролируемую дозу дополнительного триптофана. Эта добавка вернула уровни триптофана в крови к норме и дала впечатляющие результаты. В сердце сотни генов, которые напроксен сдвинул в сторону более воспалённого и склонного к повреждению состояния, вернулись к более здоровому профилю. Сигналы, связанные с цитокиновыми штормами, увеличением сердца и ухудшением насосной функции, ослабли, а активность IL-1β снизилась как на уровне РНК, так и на уровне белка. В кишечнике триптофан уменьшил кровоточивость стула и обратил изменения в генах, связанных с целостностью барьера, заживлением ран и контролем иммунитета. Примечательно, что это восстановление не отменяло эффекта напроксена на тромбоциты, что указывает на облегчение повреждений без вмешательства в желаемое антитромботическое действие.
Что это означает для людей, принимающих обезболивающие
В совокупности эти результаты позволяют предположить, что склонность напроксена истощать триптофан — и направлять его к распаду микробами кишечника — может способствовать нежелательным эффектам препарата для сердца и пищеварительного тракта. Хотя нужны дополнительные исследования на больших и длительных когортах людей, данные намекают, что мониторинг уровня триптофана в крови может служить ранним маркером риска, а аккуратно спроектированные добавки триптофана когда‑то могли бы смягчать побочный урон от широко используемых обезболивающих. Пока же исследование подчёркивает: даже привычные лекарства без рецепта способны сдвигать химию нашего организма неожиданными способами, и понимание этих сдвигов может открыть пути к повышению безопасности повседневных препаратов.
Цитирование: Ghosh, S., Lahens, N.F., Barekat, K. et al. Depression of tryptophan may contribute to adverse effects of naproxen. Nat Commun 17, 2776 (2026). https://doi.org/10.1038/s41467-026-69684-7
Ключевые слова: напроксен, триптофан, побочные эффекты НПВП, микробиом кишечника, воспаление сердечно-сосудистой системы