Clear Sky Science · es
La depresión del triptófano puede contribuir a los efectos adversos del naproxeno
Por qué las pastillas comunes para el dolor importan para todo el cuerpo
Millones de personas toman antiinflamatorios no esteroideos (AINE) como el naproxeno para dolores de cabeza, molestias articulares o lesiones, asumiendo a menudo que son auxiliares inofensivos de venta libre. Sin embargo, estos fármacos pueden aumentar silenciosamente el riesgo de hemorragia gástrica y problemas cardíacos. Este estudio plantea una pregunta simple pero importante: ¿qué hacen estos medicamentos a la química del cuerpo, y podría un nutriente natural llamado triptófano ayudar a explicar, y quizá mitigar, algunos de sus peligros ocultos?
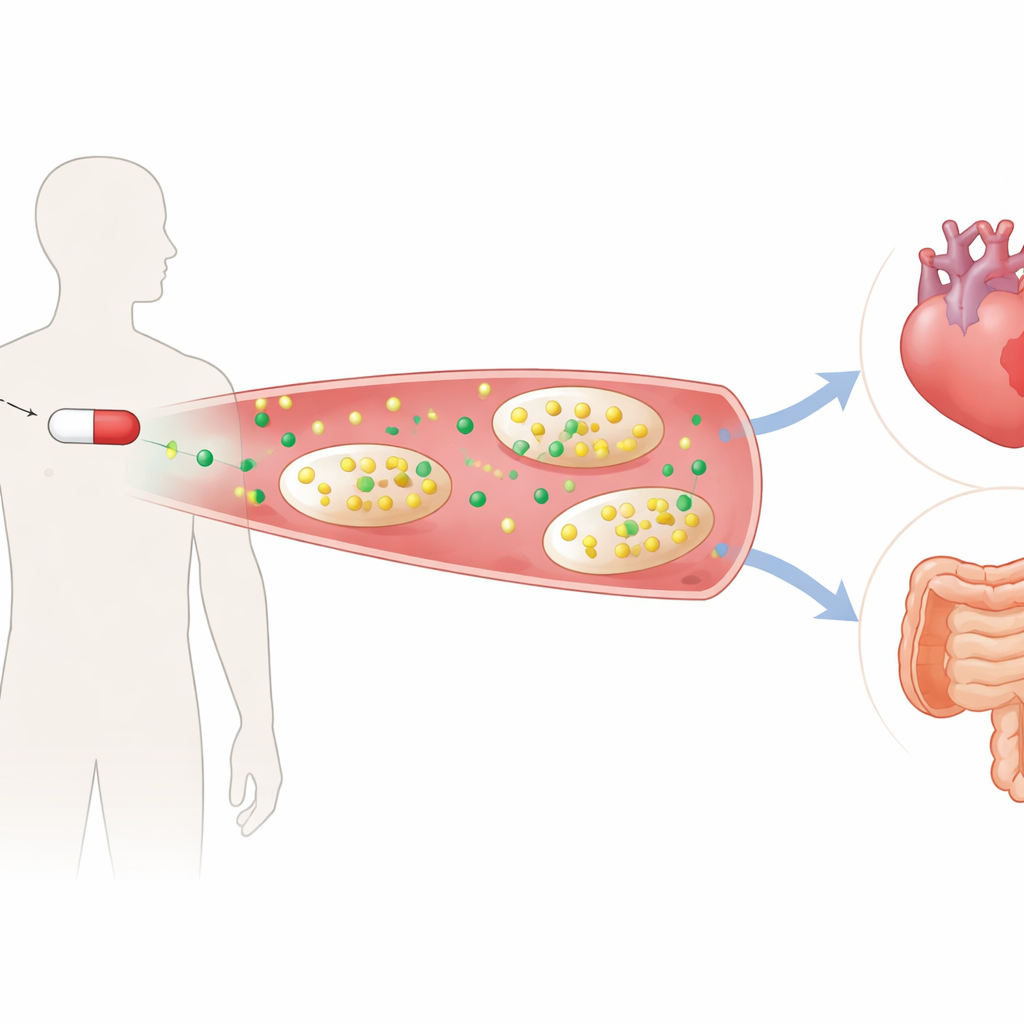
Un vistazo más atento a dos analgésicos similares
Los investigadores compararon el naproxeno, un AINE tradicional que bloquea dos enzimas relacionadas, con el celecoxib, un fármaco más nuevo que apunta solo a una de ellas. Dieciséis voluntarios sanos tomaron cada tratamiento —naproxeno, celecoxib o un placebo— durante una semana en un estudio cruzado cuidadosamente controlado. A continuación se analizaron muestras de sangre y orina mediante perfiles químicos detallados para ver cómo cambiaban miles de moléculas pequeñas en respuesta a los fármacos. Aunque ambos medicamentos redujeron con éxito los mensajeros derivados de ácidos grasos que impulsan el dolor y la fiebre, el naproxeno destacó por provocar una caída clara del triptófano y de su principal producto de degradación, la quinurenina, mientras que el celecoxib no lo hizo. Este patrón sugirió que el naproxeno estaba perturbando una vía metabólica importante más allá de su objetivo previsto.
El papel sorprendente de un aminoácido cotidiano
El triptófano es conocido principalmente como el bloque de construcción que el cuerpo usa para fabricar proteínas y ciertos químicos cerebrales, pero también alimenta una red de vías vinculadas a la inmunidad, la presión arterial y el uso de energía. En humanos y ratones, el naproxeno redujo de forma consistente el triptófano circulante y la quinurenina, mientras que otras moléculas relacionadas permanecieron en gran medida sin cambios. Experimentos complementarios mostraron que este efecto no dependía de bloquear las enzimas que el naproxeno está diseñado para inhibir. Incluso ratones modificados genéticamente para carecer de esas enzimas perdieron triptófano al recibir el fármaco. En cambio, el naproxeno pareció competir directamente con el triptófano por sitios de unión en la albúmina, una proteína sanguínea principal que transporta muchas moléculas por el cuerpo. Al aferrarse más firmemente a esos sitios, el naproxeno desplazó al triptófano y a la quinurenina de la proteína hacia la circulación, donde se degradaron y eliminaron más fácilmente.
Los microbios intestinales y los órganos inflamados entran en la historia
El equipo también exploró cómo este cambio químico podría propagarse por el organismo. En humanos y ratones, el tratamiento con naproxeno remodeló sutilmente el microbioma intestinal, favoreciendo ciertos grupos bacterianos previamente ligados a la degradación del triptófano en compuestos indólicos. Al mismo tiempo, los ratones alimentados con naproxeno mostraron señales pequeñas pero reveladoras de daño: más sangre oculta en sus heces y actividad génica en el corazón e intestino que apuntaba a inflamación y lesión tisular. Muchas de estas señales de alarma se remontaron a vías impulsadas por el mensajero inmune IL-1β y a un complejo molecular llamado inflamasoma, ambos implicados en enfermedades cardiovasculares e intestinales graves.
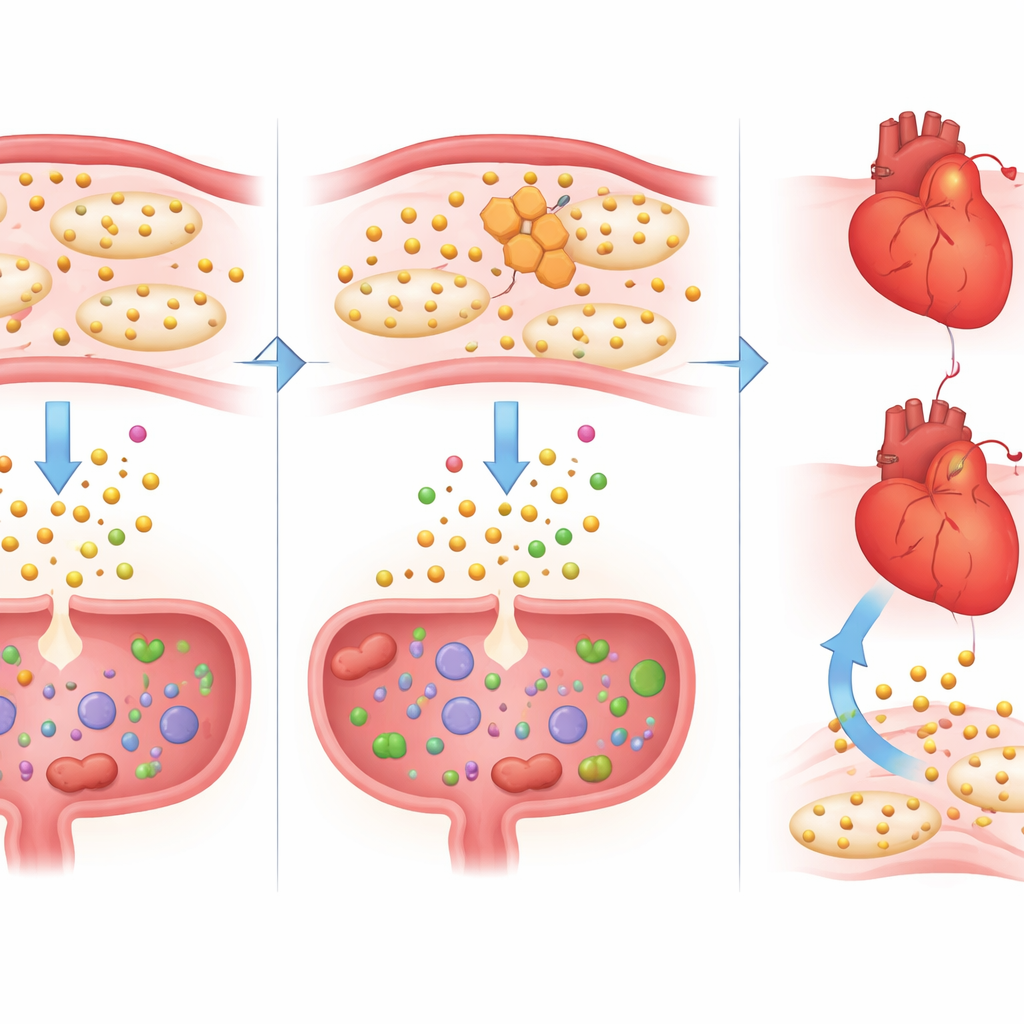
Restaurar el equilibrio con triptófano adicional
Para comprobar si la pérdida de triptófano era parte del problema en lugar de un efecto secundario inocuo, los científicos administraron a algunos ratones tratados con naproxeno una dosis controlada de triptófano adicional. Esta suplementación restauró los niveles de triptófano en sangre a la normalidad y tuvo beneficios llamativos. En el corazón, cientos de genes que el naproxeno había desplazado hacia un estado más inflamatorio y propenso a la lesión volvieron hacia un patrón más saludable. Los signos vinculados a tormentas de citoquinas, agrandamiento cardíaco y función de bombeo deficiente se atenuaron, y la actividad de IL-1β disminuyó tanto a nivel de ARNm como de proteína. En el intestino, el triptófano redujo la sangre en las heces y revirtió cambios en genes implicados en la integridad de la barrera, la cicatrización y el control inmune. Es notable que este rescate no anuló el efecto del naproxeno sobre las plaquetas, lo que indica que alivió el daño sin interferir con la acción antiagregante prevista.
Qué significa esto para las personas que usan analgésicos
En conjunto, estos hallazgos sugieren que la tendencia del naproxeno a agotar el triptófano —y a canalizarlo hacia la degradación por microbios intestinales— puede contribuir a los efectos indeseados del fármaco en el corazón y el tracto digestivo. Aunque se necesita más trabajo en estudios humanos más amplios y prolongados, los resultados apuntan a que controlar el triptófano en sangre podría servir como un marcador de aviso temprano del riesgo, y que una suplementación con triptófano cuidadosamente diseñada podría algún día atenuar el daño colateral de analgésicos de uso generalizado. Por ahora, el estudio subraya que incluso fármacos familiares de venta libre pueden alterar la química de nuestro cuerpo de maneras inesperadas, y que comprender esos cambios puede abrir vías para hacer los medicamentos cotidianos más seguros.
Cita: Ghosh, S., Lahens, N.F., Barekat, K. et al. Depression of tryptophan may contribute to adverse effects of naproxen. Nat Commun 17, 2776 (2026). https://doi.org/10.1038/s41467-026-69684-7
Palabras clave: naproxeno, triptófano, efectos secundarios AINE, microbioma intestinal, inflamación cardiovascular