Clear Sky Science · it
La depressione del triptofano potrebbe contribuire agli effetti avversi del naprossene
Perché gli analgesici comuni contano per tutto il corpo
Milioni di persone assumono farmaci antinfiammatori non steroidei (FANS) come il naprossene per mal di testa, dolori articolari o traumi, spesso pensando che siano rimedi innocui da banco. Eppure questi farmaci possono silenziosamente aumentare il rischio di sanguinamento gastrico e problemi cardiaci. Questo studio pone una domanda semplice ma importante: cosa fanno questi medicinali alla chimica del corpo e potrebbe un nutriente naturale chiamato triptofano aiutare a spiegare, e forse attenuare, alcuni dei loro pericoli nascosti?
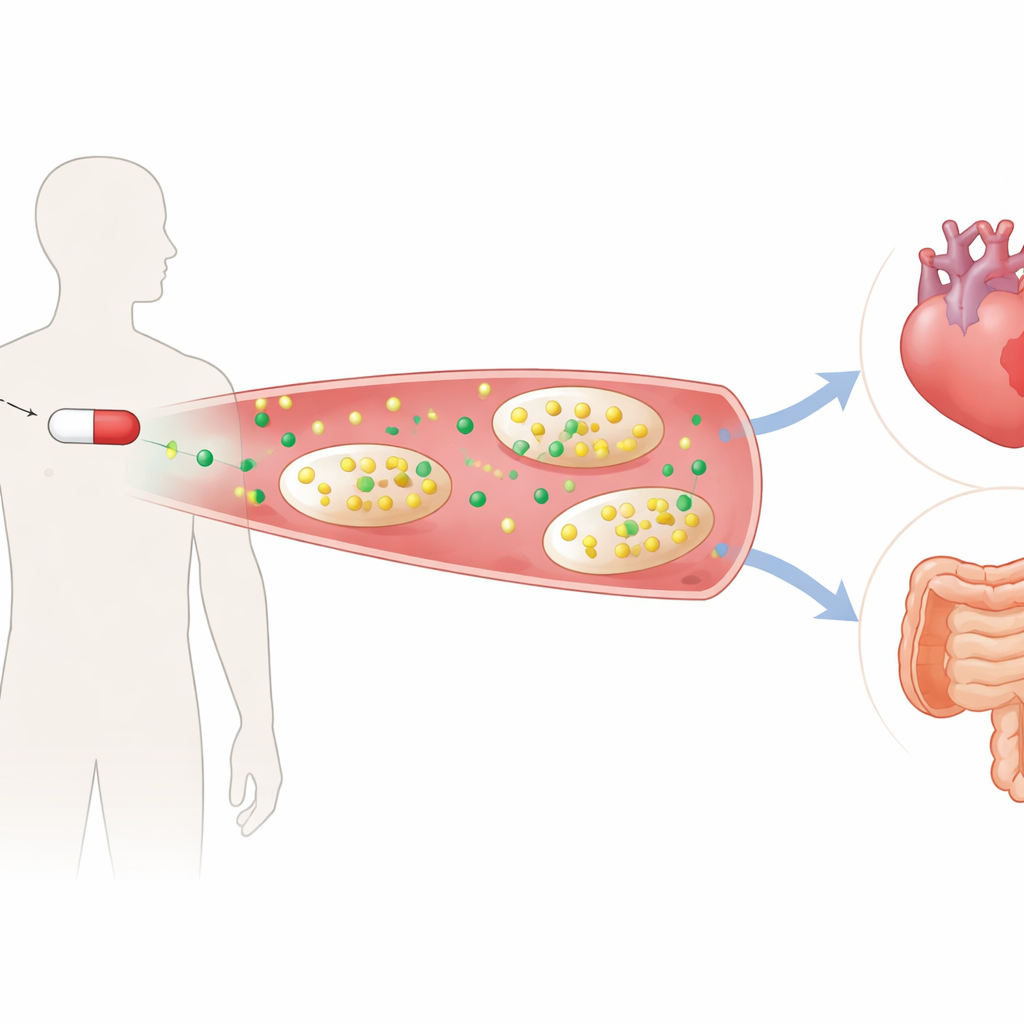
Uno sguardo più ravvicinato a due analgesici simili
I ricercatori hanno confrontato il naprossene, un FANS tradizionale che inibisce due enzimi correlati, con il celecoxib, un farmaco più recente che prende di mira solo uno di essi. Sedici volontari sani hanno assunto ciascun trattamento — naprossene, celecoxib o placebo — per una settimana in uno studio crossover attentamente controllato. Campioni di sangue e urine sono stati poi analizzati con un profilo chimico dettagliato per vedere come migliaia di piccole molecole cambiassero in risposta ai farmaci. Sebbene entrambi i medicinali abbiano ridotto con successo i messaggeri a base di acidi grassi che guidano dolore e febbre, il naprossene si è distinto per aver provocato un chiaro calo del triptofano e del suo principale prodotto di degradazione, la chinurenina, mentre il celecoxib non l’ha fatto. Questo schema suggeriva che il naprossene stesse disturbando una via metabolica importante oltre al suo bersaglio previsto.
Il ruolo sorprendente di un amminoacido quotidiano
Il triptofano è noto soprattutto come il mattoncino che il corpo usa per costruire proteine e certe sostanze chimiche cerebrali, ma alimenta anche una rete di vie collegate all’immunità, alla pressione sanguigna e all’uso di energia. Negli esseri umani e nei topi, il naprossene ha costantemente abbassato il triptofano circolante e la chinurenina, lasciando per lo più inalterate altre molecole correlate. Esperimenti successivi hanno mostrato che questo effetto non dipendeva dall’inibizione degli enzimi che il naprossene è progettato per bloccare. Anche i topi geneticamente modificati privi di quegli enzimi hanno perso triptofano quando hanno ricevuto il farmaco. Invece, il naprossene pareva competere direttamente con il triptofano per i siti di legame sull’albumina, una proteina plasmatica principale che trasporta molte molecole nel corpo. Aggrappandosi più saldamente a questi siti, il naprossene spingeva via il triptofano e la chinurenina dalla proteina e li portava in circolo, dove venivano più facilmente degradati ed eliminati.
I microbi intestinali e gli organi infiammati entrano in gioco
Il gruppo ha anche esplorato come questo cambiamento chimico potesse riverberare nel corpo. Negli esseri umani e nei topi, il trattamento con naprossene ha rimodellato in modo sottile il microbioma intestinale, favorendo alcuni gruppi batterici precedentemente associati alla degradazione del triptofano in composti indolici. Allo stesso tempo, nei topi nutriti con naprossene sono emersi segnali piccoli ma significativi di danno: più sangue occulto nelle feci e attività genica nel cuore e nell’intestino che indicavano infiammazione e lesioni tissutali. Molti di questi segnali di allarme rimandavano a vie guidate dal mediatore immunitario IL-1β e a un complesso molecolare chiamato inflammasoma, entrambi coinvolti in gravi patologie cardiovascolari e intestinali.
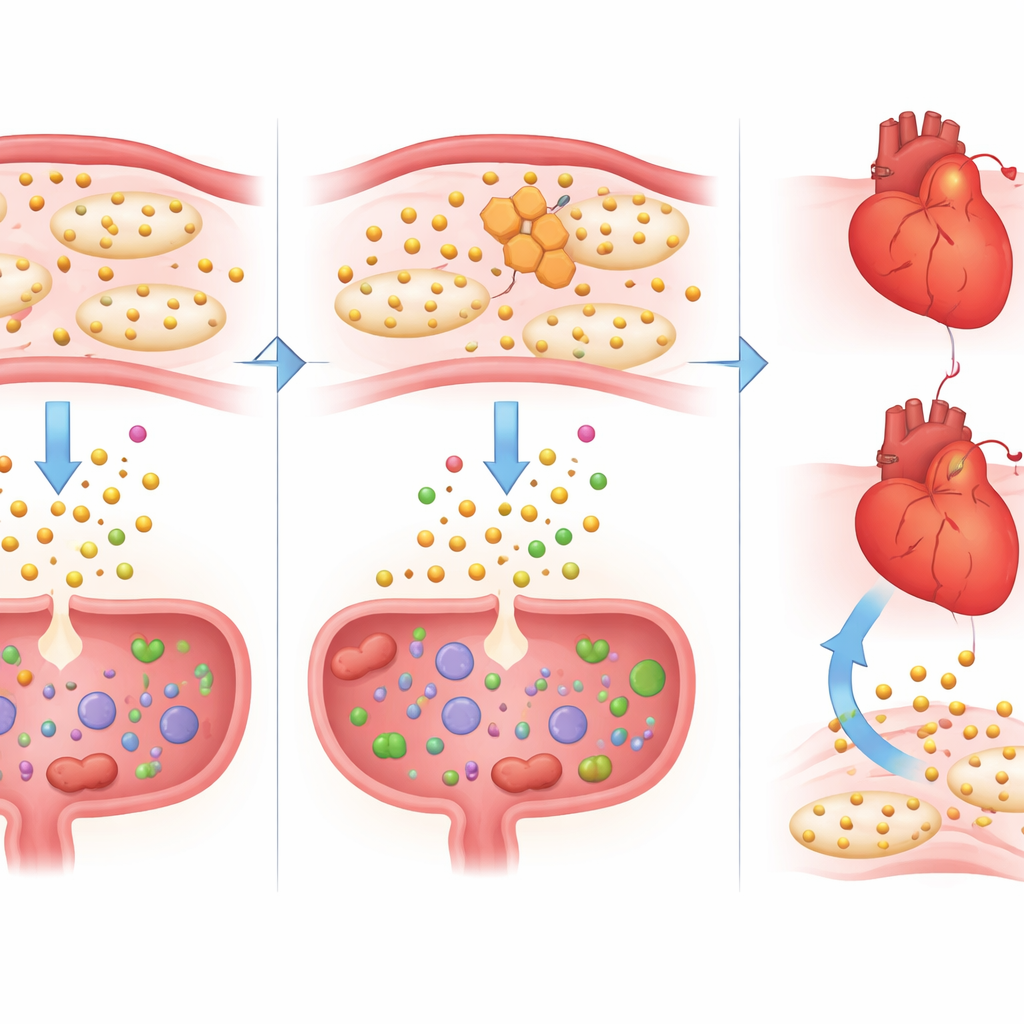
Ripristinare l’equilibrio con un extra di triptofano
Per verificare se la perdita di triptofano fosse parte del problema piuttosto che un effetto collaterale innocuo, gli scienziati hanno somministrato ad alcuni topi trattati con naprossene una dose controllata di triptofano aggiuntivo. Questa supplementazione ha ripristinato i livelli ematici di triptofano alla normalità e ha avuto benefici notevoli. Nel cuore, centinaia di geni che il naprossene aveva spinto verso uno stato più infiammatorio e incline alle lesioni sono tornati verso uno schema più sano. I segnali legati a tempeste di citochine, ingrandimento cardiaco e scarsa funzione di pompaggio si sono attenuati, e l’attività di IL-1β è diminuita sia a livello di RNA sia di proteina. Nell’intestino, il triptofano ha ridotto il sangue nelle feci e ha invertito modifiche nei geni coinvolti nell’integrità della barriera, nella guarigione delle ferite e nel controllo immunitario. È importante notare che questo recupero non ha annullato l’effetto del naprossene sulle piastrine, indicando che ha alleviato il danno senza interferire con l’azione anti‑coagulante voluta.
Cosa significa per chi usa analgesici
Nel loro insieme, questi risultati suggeriscono che la tendenza del naprossene a esaurire il triptofano — e a indirizzarlo verso la degradazione da parte dei microbi intestinali — potrebbe contribuire agli effetti indesiderati del farmaco sul cuore e sul tratto digestivo. Sebbene siano necessari ulteriori studi umani più ampi e prolungati, i risultati lasciano intendere che il monitoraggio del triptofano ematico potrebbe servire come indicatore precoce di rischio e che una supplementazione di triptofano attentamente progettata potrebbe un giorno attenuare i danni collaterali di analgesici ampiamente usati. Per ora, lo studio sottolinea che anche farmaci da banco familiari possono spostare la chimica del nostro corpo in modi inaspettati e che comprendere tali cambiamenti può aprire strade per rendere i medicinali di uso quotidiano più sicuri.
Citazione: Ghosh, S., Lahens, N.F., Barekat, K. et al. Depression of tryptophan may contribute to adverse effects of naproxen. Nat Commun 17, 2776 (2026). https://doi.org/10.1038/s41467-026-69684-7
Parole chiave: naprossene, triptofano, effetti collaterali FANS, microbioma intestinale, infiammazione cardiovascolare