Clear Sky Science · nl
Een daling van tryptofaan kan bijdragen aan nadelige effecten van naproxen
Waarom gewone pijnstillers belangrijk zijn voor je hele lichaam
Miljoenen mensen gebruiken niet-steroïde ontstekingsremmers (NSAID's) zoals naproxen tegen hoofdpijn, gewrichtspijn of blessures en gaan er vaak van uit dat het onschadelijke vrij verkrijgbare hulpmiddelen zijn. Toch kunnen deze middelen het risico op maagbloedingen en hartproblemen stilletjes verhogen. Deze studie stelt een eenvoudige maar belangrijke vraag: wat doen deze geneesmiddelen met de chemie van het lichaam, en zou een natuurlijke voedingsstof genaamd tryptofaan kunnen helpen sommige van hun verborgen gevaren te verklaren — en mogelijk te verzachten?
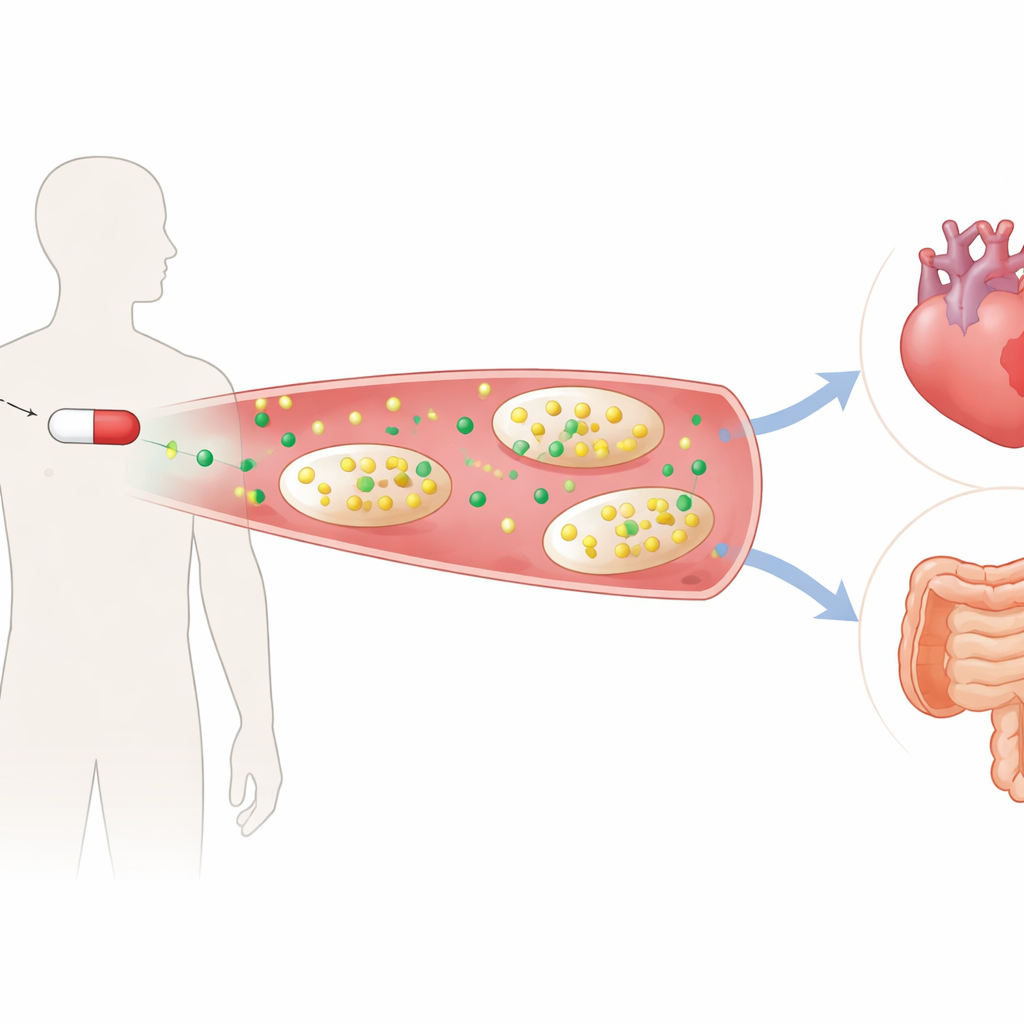
Een nadere blik op twee vergelijkbare pijnstillers
De onderzoekers vergeleken naproxen, een traditionele NSAID die twee verwante enzymen blokkeert, met celecoxib, een nieuwer middel dat slechts één van die enzymen richt. Zestien gezonde vrijwilligers kregen elk tijdens een zorgvuldig gecontroleerde kruisproef elk van de behandelingen — naproxen, celecoxib of een placebo — telkens een week. Bloed- en urinemonsters werden vervolgens geanalyseerd met gedetailleerde chemische profielbepaling om te zien hoe duizenden kleine moleculen veranderden onder invloed van de medicijnen. Hoewel beide middelen de vetzuurboodschappers die pijn en koorts aandrijven effectief verminderden, viel naproxen op doordat het duidelijk tryptofaan en het belangrijkste afbraakproduct, kynurenine, verlaagde, terwijl celecoxib dat niet deed. Dit patroon suggereerde dat naproxen een belangrijk metabool pad verstoorde buiten zijn beoogde doelwit.
De verrassende rol van een alledaam aminozuur
Tryptofaan staat vooral bekend als bouwsteen die het lichaam gebruikt om eiwitten en bepaalde hersenchemicaliën te maken, maar het voedt ook een netwerk van routes die verbonden zijn met immuniteit, bloeddruk en energiegebruik. Zowel bij mensen als bij muizen verlaagde naproxen consequent circulerend tryptofaan en kynurenine, terwijl andere verwante moleculen grotendeels onveranderd bleven. Vervolgexperimenten toonden aan dat dit effect niet afhing van het blokkeren van de enzymen die naproxen bedoeld is te remmen. Zelfs muizen die genetisch zo gemodificeerd waren dat die enzymen ontbraken, verloren tryptofaan bij toediening van het middel. In plaats daarvan leek naproxen direct te concurreren met tryptofaan om bindingsplaatsen op albumine, een belangrijk bloedproteïne dat veel moleculen door het lichaam vervoert. Door zich strakker aan deze plekken te hechten, duwde naproxen tryptofaan en kynurenine van het proteïne af en bracht ze in de circulatie, waar ze gemakkelijker afgebroken en verwijderd werden.
Darmmicroben en ontstoken organen komen in het verhaal
Het team onderzocht ook hoe deze chemische verschuiving zich door het lichaam zou kunnen verspreiden. Bij mensen en muizen herschikte naproxen de darmmicrobiota subtiel en bevorderde bepaalde bacteriegroepen die eerder in verband waren gebracht met de afbraak van tryptofaan naar indoolverbindingen. Tegelijk toonden muizen die naproxen kregen kleine maar veelzeggende tekenen van schade: meer verborgen bloed in hun ontlasting en genactiviteit in het hart en de darm die wees op ontsteking en weefselschade. Veel van deze alarmsignalen waren terug te voeren op routewegen die worden aangedreven door de immuunstuursignaalstof IL-1β en op een moleculair complex dat het inflammasoom wordt genoemd, die beide betrokken zijn bij ernstige cardiovasculaire en darmziekten.
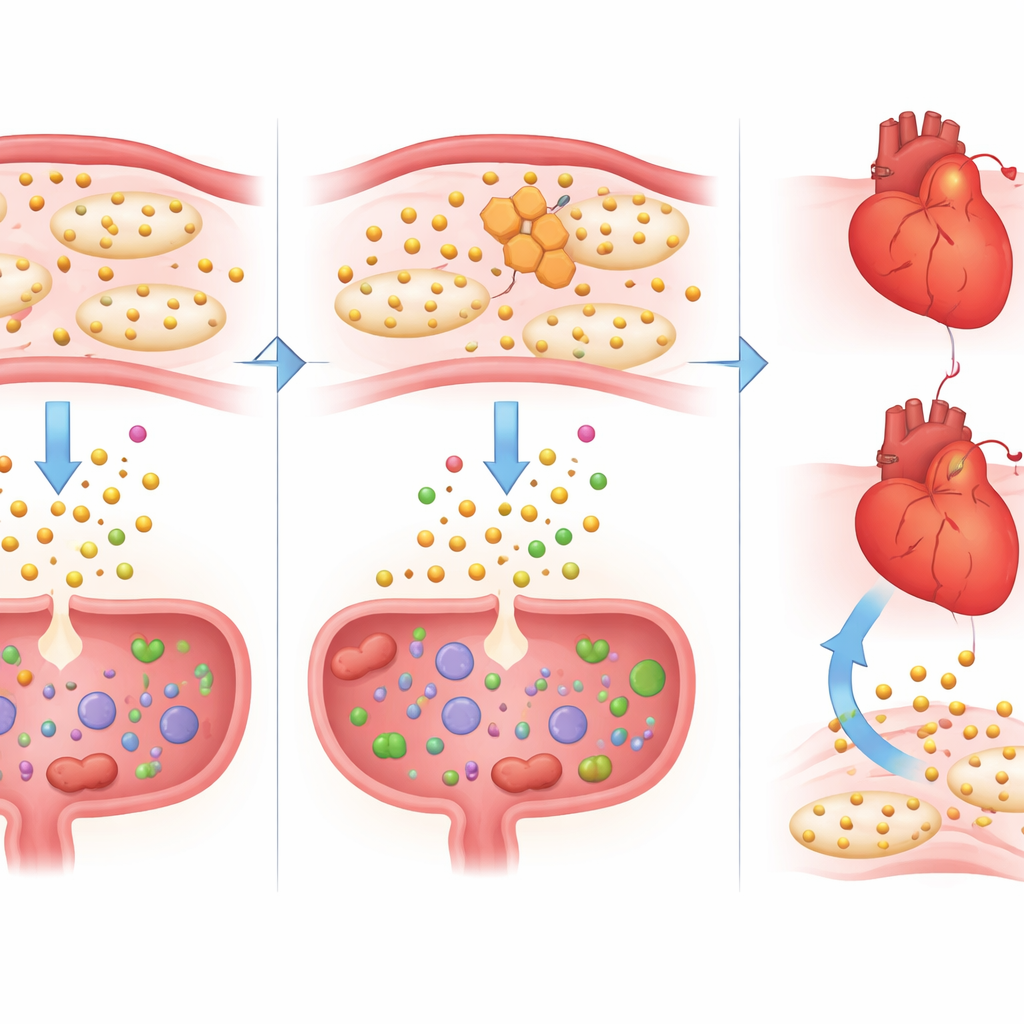
Het herstel van evenwicht met extra tryptofaan
Om te testen of het verlies van tryptofaan deel van het probleem was in plaats van een onschadelijk bijeffect, kregen sommige naproxen-behandelde muizen een gecontroleerde dosis extra tryptofaan. Deze aanvulling bracht het bloedtryptofaan terug naar normale niveaus en had opvallende voordelen. In het hart keerden honderden genen die door naproxen naar een meer inflammatoir, kwetsbaar patroon waren gedrukt terug naar een gezondere expressie. Signalen die verband hielden met cytokinestormen, vergroting van het hart en verminderde pompfunctie namen af, en IL-1β-activiteit daalde zowel op RNA- als eiwitniveau. In de darm verminderde tryptofaan de bloedsporen in de ontlasting en keerde veranderingen in genen die betrokken zijn bij barrièremede, wondgenezing en immuunregulatie om. Opvallend was dat dit herstel de werking van naproxen op bloedplaatjes niet ongedaan maakte, wat aangeeft dat het schade verzachtte zonder het beoogde antistollingseffect te verstoren.
Wat dit betekent voor mensen die pijnstillers gebruiken
Gezamenlijk wijzen deze bevindingen erop dat de neiging van naproxen om tryptofaan uit te putten — en het naar afbraak door darmmicroben te leiden — kan bijdragen aan de ongewenste effecten van het middel op hart en spijsverteringskanaal. Hoewel er meer onderzoek nodig is in grotere, langdurigere humane studies, suggereren de resultaten dat het volgen van bloedtryptofaan als een vroeg waarschuwingsmerker van risico zou kunnen dienen, en dat zorgvuldig ontworpen tryptofaanaanvulling mogelijk ooit de nevenschade van veelgebruikte pijnstillers kan verzachten. Voor nu benadrukt de studie dat zelfs vertrouwde vrij verkrijgbare middelen de chemie van ons lichaam op onverwachte manieren kunnen prikkelen, en dat begrip van die verschuivingen wegen kan openen om alledaagse medicijnen veiliger te maken.
Bronvermelding: Ghosh, S., Lahens, N.F., Barekat, K. et al. Depression of tryptophan may contribute to adverse effects of naproxen. Nat Commun 17, 2776 (2026). https://doi.org/10.1038/s41467-026-69684-7
Trefwoorden: naproxen, tryptofaan, NSAID-bijwerkingen, darmmicrobioom, cardiovasculaire ontsteking