Clear Sky Science · pt
A queda de triptofano pode contribuir para efeitos adversos do naproxeno
Por que analgésicos comuns importam para todo o seu corpo
Milhões de pessoas tomam anti-inflamatórios não esteroides (AINEs) como o naproxeno para dor de cabeça, dores articulares ou lesões, muitas vezes presumindo que são ajudantes inofensivos de venda livre. No entanto, esses medicamentos podem aumentar silenciosamente o risco de sangramento estomacal e problemas cardíacos. Este estudo faz uma pergunta simples, mas importante: o que esses remédios fazem à química do corpo e se um nutriente natural chamado triptofano pode ajudar a explicar — e talvez atenuar — alguns de seus perigos ocultos?
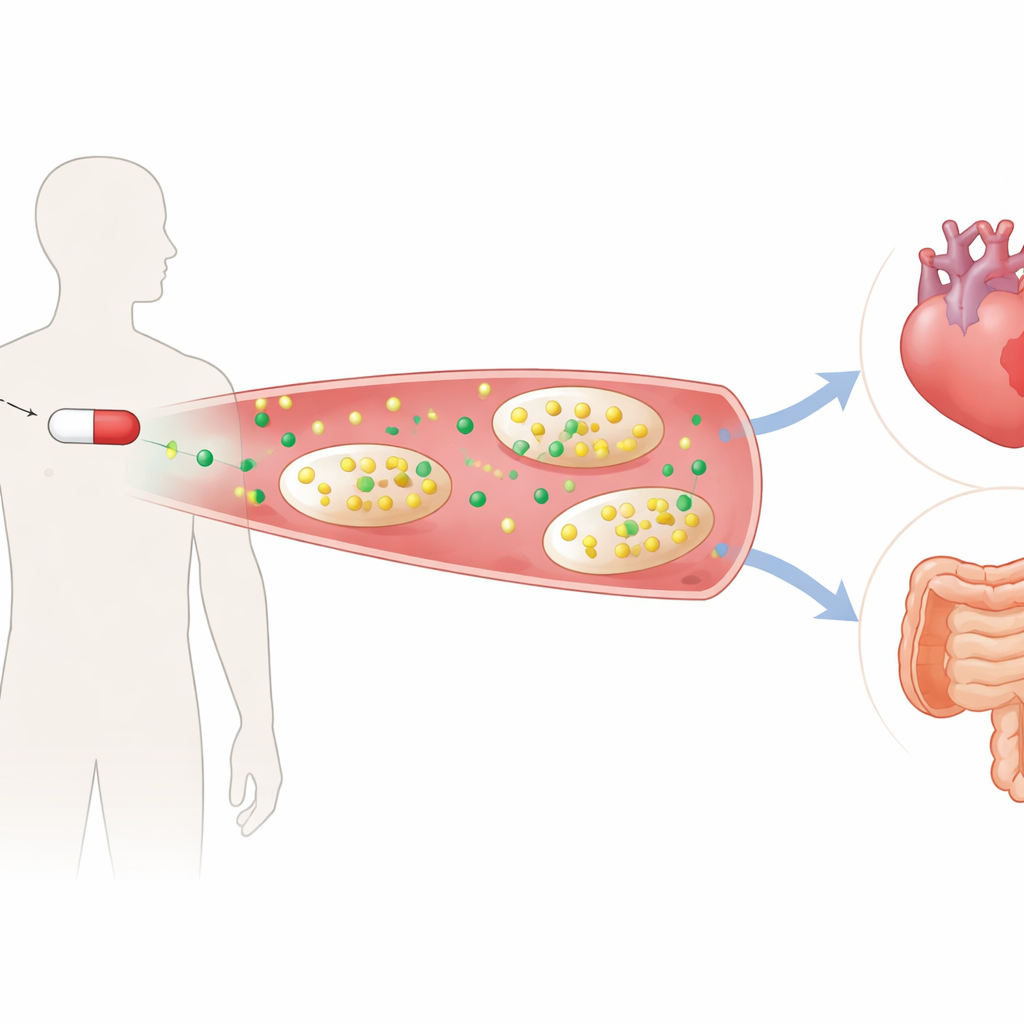
Um olhar mais atento a dois analgésicos similares
Os pesquisadores compararam naproxeno, um AINE tradicional que bloqueia duas enzimas relacionadas, com celecoxibe, um medicamento mais novo que atinge apenas uma delas. Dezesseis voluntários saudáveis receberam cada tratamento — naproxeno, celecoxibe ou placebo — por uma semana em um estudo cruzado cuidadosamente controlado. Amostras de sangue e urina foram então analisadas usando perfilamento químico detalhado para ver como milhares de pequenas moléculas mudaram em resposta aos fármacos. Embora ambos os medicamentos tenham reduzido com sucesso os mensageiros de ácidos graxos que promovem dor e febre, o naproxeno destacou-se por causar uma queda clara no triptofano e em seu principal produto de degradação, a quinurenina, enquanto o celecoxibe não o fez. Esse padrão sugeriu que o naproxeno estava perturbando uma via metabólica importante além de seu alvo pretendido.
O papel surpreendente de um aminoácido cotidiano
O triptofano é mais conhecido como o bloco de construção que o corpo usa para fabricar proteínas e certos neurotransmissores, mas também alimenta uma rede de vias ligadas à imunidade, pressão arterial e uso de energia. Em humanos e camundongos, o naproxeno reduziu consistentemente o triptofano circulante e a quinurenina, enquanto deixou outras moléculas relacionadas amplamente inalteradas. Experimentos de seguimento mostraram que esse efeito não dependia do bloqueio das enzimas que o naproxeno foi projetado para inibir. Mesmo camundongos geneticamente modificados para não ter essas enzimas ainda perderam triptofano quando receberam a droga. Em vez disso, o naproxeno pareceu competir diretamente com o triptofano por locais de ligação na albumina, uma proteína plasmática importante que transporta muitas moléculas pelo corpo. Ao aderir com mais força a esses locais, o naproxeno deslocou o triptofano e a quinurenina da proteína para a circulação, onde foram mais facilmente degradados e eliminados.
Microbios intestinais e órgãos inflamados entram na história
A equipe também explorou como essa mudança química poderia repercutir pelo corpo. Em humanos e camundongos, o tratamento com naproxeno remodelou sutilmente o microbioma intestinal, favorecendo certos grupos bacterianos previamente ligados à degradação do triptofano em compostos indólicos. Ao mesmo tempo, camundongos alimentados com naproxeno mostraram sinais pequenos, mas reveladores, de dano: mais sangue oculto nas fezes e atividade gênica no coração e no intestino apontando para inflamação e lesão tecidual. Muitos desses sinais de alerta se relacionaram com vias impulsionadas pelo mensageiro imunológico IL-1β e por um complexo molecular chamado inflamasoma, ambos envolvidos em doenças cardiovasculares e intestinais graves.
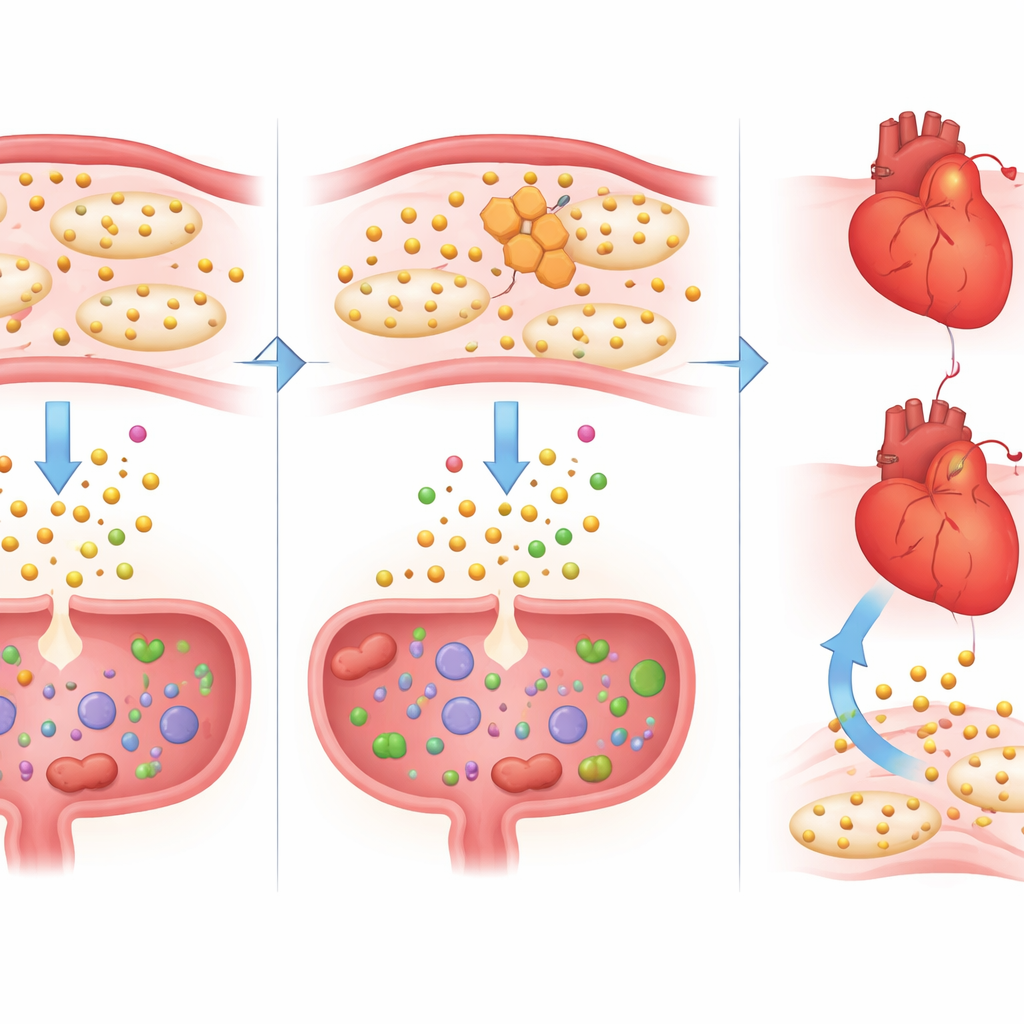
Restaurando o equilíbrio com triptofano extra
Para testar se a perda de triptofano fazia parte do problema em vez de ser um efeito colateral inofensivo, os cientistas deram a alguns camundongos tratados com naproxeno uma dose controlada de triptofano adicional. Essa suplementação restaurou os níveis sanguíneos de triptofano ao normal e teve benefícios notáveis. No coração, centenas de genes que o naproxeno havia empurrado para um estado mais inflamatório e propenso a lesões voltaram a um padrão mais saudável. Sinais associados a tempestades de citocinas, aumento do coração e função de bombeamento prejudicada se acalmaram, e a atividade de IL-1β caiu tanto nos níveis de RNA quanto de proteína. No intestino, o triptofano reduziu o sangue nas fezes e reverteu alterações em genes envolvidos na integridade da barreira, cicatrização de feridas e controle imune. Notavelmente, esse resgate não anulou o efeito do naproxeno nas plaquetas, indicando que amenizou o dano sem interferir na ação antiplaquetária pretendida.
O que isso significa para pessoas que usam analgésicos
Em conjunto, esses achados sugerem que a tendência do naproxeno de esgotar o triptofano — e de canalizá-lo para degradação por microrganismos intestinais — pode ajudar a impulsionar os efeitos indesejados do fármaco no coração e no trato digestivo. Embora sejam necessários mais estudos maiores e mais longos em humanos, os resultados indicam que monitorar o triptofano sanguíneo poderia servir como um marcador de alerta precoce de risco, e que uma suplementação cuidadosamente projetada de triptofano talvez um dia atenue os danos colaterais de analgésicos amplamente usados. Por ora, o estudo reforça que até medicamentos familiares vendidos sem receita podem alterar a química do nosso corpo de maneiras inesperadas, e que compreender essas mudanças pode abrir caminhos para tornar remédios cotidianos mais seguros.
Citação: Ghosh, S., Lahens, N.F., Barekat, K. et al. Depression of tryptophan may contribute to adverse effects of naproxen. Nat Commun 17, 2776 (2026). https://doi.org/10.1038/s41467-026-69684-7
Palavras-chave: naproxeno, triptofano, efeitos colaterais de AINEs, microbioma intestinal, inflamação cardiovascular