Clear Sky Science · ru
Обратный режим NCX1 способствует кальций-зависимому образованию внеклеточных ловушек нейтрофилов и повреждению лёгких при хронической обструктивной болезни лёгких
Почему маленькие клетки в лёгких курильщика важны
Хроническая обструктивная болезнь лёгких (ХОБЛ) — одна из ведущих причин смерти в мире, чаще всего связанная с многолетним курением. Многие пациенты живут с постоянной одышкой и сталкиваются с частыми обострениями, тогда как существующие методы лечения мало замедляют постепенное разрушение лёгочной ткани. В этом исследовании подробно изучается один конкретный тип белых кровяных клеток — нейтрофилы — и один молекулярный «затвор» на их поверхности, чтобы объяснить, как табачный дым превращает полезные иммунные клетки в движущую силу долгосрочного повреждения лёгких. Выявив этот переключатель, авторы показывают потенциальный способ смягчить вредное воспаление, не выключая при этом защитные механизмы организма.
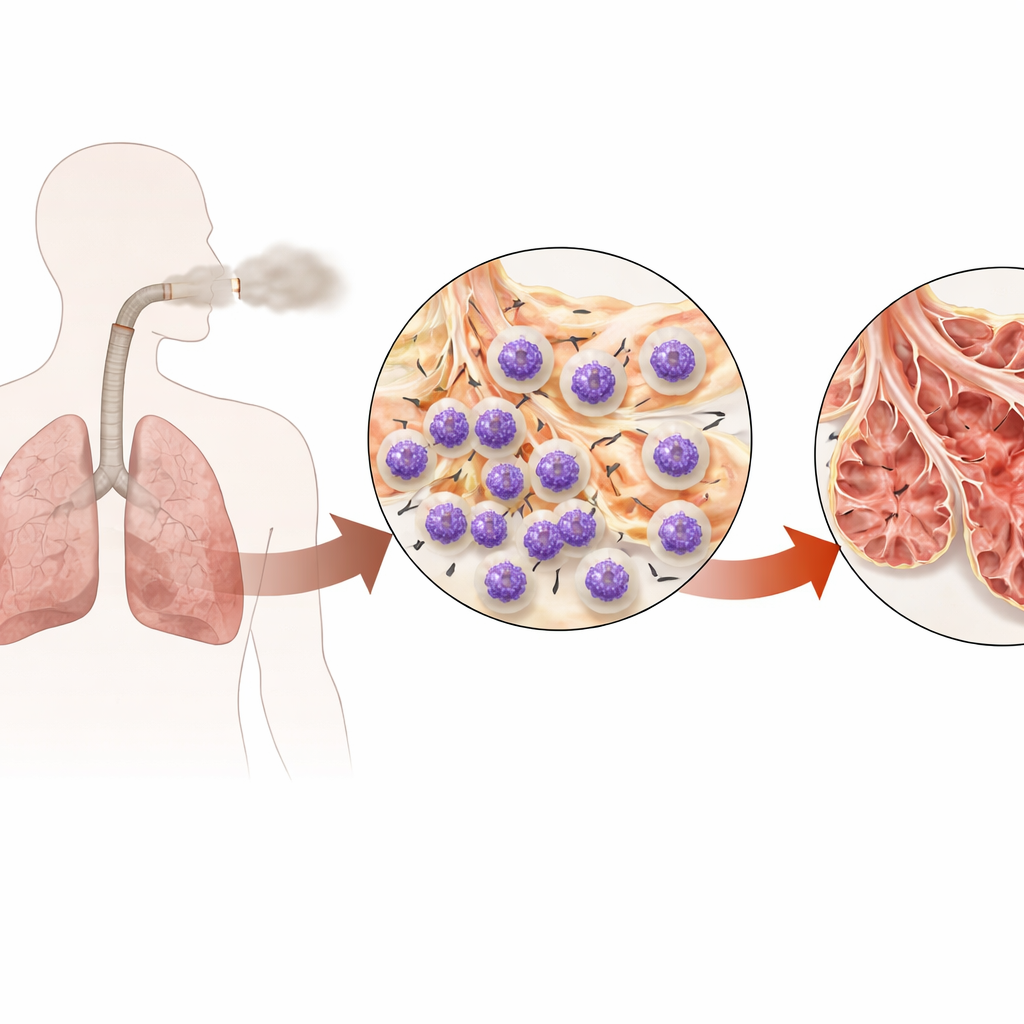
Упрямая болезнь лёгких, подпитываемая гиперактивными защитниками
ХОБЛ постепенно рубцует и разрыхляет лёгкие, оставляя утолщённые дыхательные пути и увеличенные, хрупкие альвеолы. Нейтрофилы — клетки‑первые реагирующие — встречаются в изобилии в мокроте и ткани лёгких у людей с ХОБЛ, и их количество коррелирует с ухудшением потока воздуха и функции лёгких. Но простое подавление нейтрофилов по всему телу сопряжено с риском тяжёлых инфекций. Поэтому авторы задали более прицельный вопрос: существует ли внутри нейтрофилов конкретный внутриклеточный механизм, который табачный дым угоняет, чтобы поддерживать их активацию, скопление в лёгких и длительное повреждение ткани?
Кальциевый «затвор» в нейтрофилах усилен при ХОБЛ
Команда сосредоточилась на NCX1 — белке, который меняет натрий и кальций через клеточную мембрану. В образцах человеческих лёгких, в жидкостях дыхательных путей и в циркулирующей крови уровни NCX1 в нейтрофилах у пациентов с сочетанием хронического бронхита и эмфиземы были заметно выше, чем у людей без хронических заболеваний лёгких. Это повышение тесно коррелировало с маркёрами активации нейтрофилов, что указывает на то, что NCX1 может быть не просто наблюдателем. У мышей, подвергшихся длительному воздействию табачного дыма, нейтрофилы в лёгких также показали повышенный уровень NCX1, повторяя человеческие наблюдения.
Как дым подталкивает нейтрофилы к разрушительному состоянию
Используя модели на мышах и культуры клеток, исследователи выяснили, как NCX1 помогает превращать воздействие табачного дыма в повреждающее воспаление. В норме NCX1 может выносить кальций из клетки; при определённых условиях он «переворачивается» и вносит кальций внутрь. Экстракт табачного дыма сильно сдвигал нейтрофилы в этот «обратный режим», вызывая всплеск внутриклеточного кальция. Это кальциевое перегружение было необходимым для образования внеклеточных ловушек нейтрофилов (NETs) — сетей ДНК, усыпанных токсичными ферментами, которые способны удерживать микробы, но также разрушать окружающие ткани. Когда NCX1 был генетически удалён только в нейтрофилах или когда его обратная активность блокировалась лекарством, нейтрофилы, подвергшиеся действию дыма, демонстрировали значительно меньший приток кальция и выделяли гораздо меньше NETs.
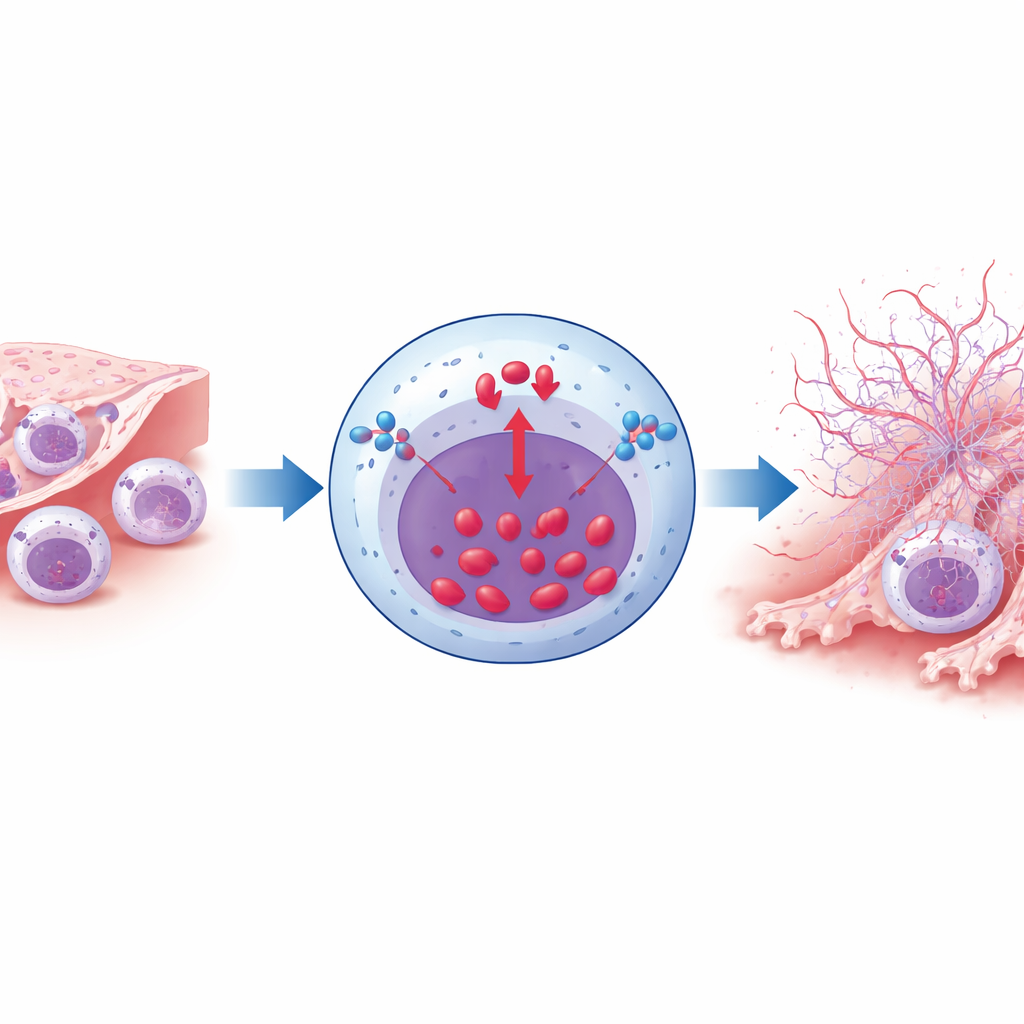
Меньше ловушек — меньше рубцевания — лучше лёгкие
Последствия уменьшения образования NETs, вызванного NCX1, были впечатляющими. У мышей, подвергшихся дымовой экспозиции, удаление NCX1 только в нейтрофилах приводило к меньшему скоплению нейтрофилов в лёгких, меньшему отложению коллагена и утолщению гладкой мускулатуры вокруг дыхательных путей, а также к менее выраженному разрушению альвеол. Показатели функции лёгких, включая поток воздуха и способность лёгких расширяться, частично сохранялись по сравнению с контрольными животными. Независимая блокада NETs другим препаратом, Cl‑amidine, давала сходные преимущества: меньше нейтрофилов, меньше структурного повреждения и лучшая дыхательная механика. Важно, что удаление NCX1 из нейтрофилов не влияло на их нормальное развитие, миграцию или фагоцитоз бактерий, что говорит о том, что вмешательство в основном сдерживает их патологическое поведение в среде, насыщенной дымом.
Новая, более точная цель для лечения ХОБЛ
Для неспециалиста суть в том, что исследование выявило ключевой молекулярный переключатель — работу NCX1 в обратном направлении — который помогает объяснить, почему нейтрофилы задерживаются и причиняют постоянный вред в лёгких курильщиков. Подводя в эти клетки избыток кальция, NCX1 способствует высвобождению липких, покрытых ферментами ДНК‑сетей, которые повреждают структуры лёгких и поддерживают химическую среду, привлекающую новые нейтрофилы. Понижение активности этого переключателя, либо путём удаления NCX1 из нейтрофилов, либо блокируя его обратную работу, разрывает этот порочный круг у мышей и защищает функцию лёгких без широкого ослабления иммунной системы. Хотя нужны дополнительные исследования, чтобы точно установить, какие компоненты табачного дыма переводят NCX1 в обратный режим, и чтобы проверить безопасность у людей, результаты указывают на NCX1 и образование NETs как перспективные, более селективные мишени для препаратов, замедляющих или предотвращающих повреждение лёгких при ХОБЛ.
Цитирование: Liao, SX., Wang, YW., Shi, LM. et al. NCX1 reverse mode promotes calcium-dependent Neutrophil Extracellular Trap formation and lung damage in chronic obstructive pulmonary disease. Nat Commun 17, 3801 (2026). https://doi.org/10.1038/s41467-026-69636-1
Ключевые слова: ХОБЛ, нейтрофилы, кальциевая сигнализация, NETs, табачный дым