Clear Sky Science · fr
Le mode inverse de NCX1 favorise la formation dépendante du calcium de filets extracellulaires de neutrophiles et les lésions pulmonaires dans la maladie pulmonaire obstructive chronique
Pourquoi de minuscules cellules dans les poumons des fumeurs comptent
La maladie pulmonaire obstructive chronique (MPOC) est une des principales causes de mortalité dans le monde, le plus souvent liée à des années de tabagisme. De nombreux patients vivent avec un essoufflement quotidien et des exacerbations fréquentes, et pourtant les traitements actuels font peu pour arrêter la destruction progressive du tissu pulmonaire. Cette étude examine en profondeur un type particulier de globule blanc — les neutrophiles — et une seule « porte » moléculaire à leur surface pour expliquer comment la fumée de cigarette transforme des cellules immunitaires utiles en moteurs de lésions pulmonaires persistantes. En identifiant cet interrupteur, les chercheurs révèlent une voie potentielle pour calmer l’inflammation nuisible sans neutraliser les défenses de l’organisme.
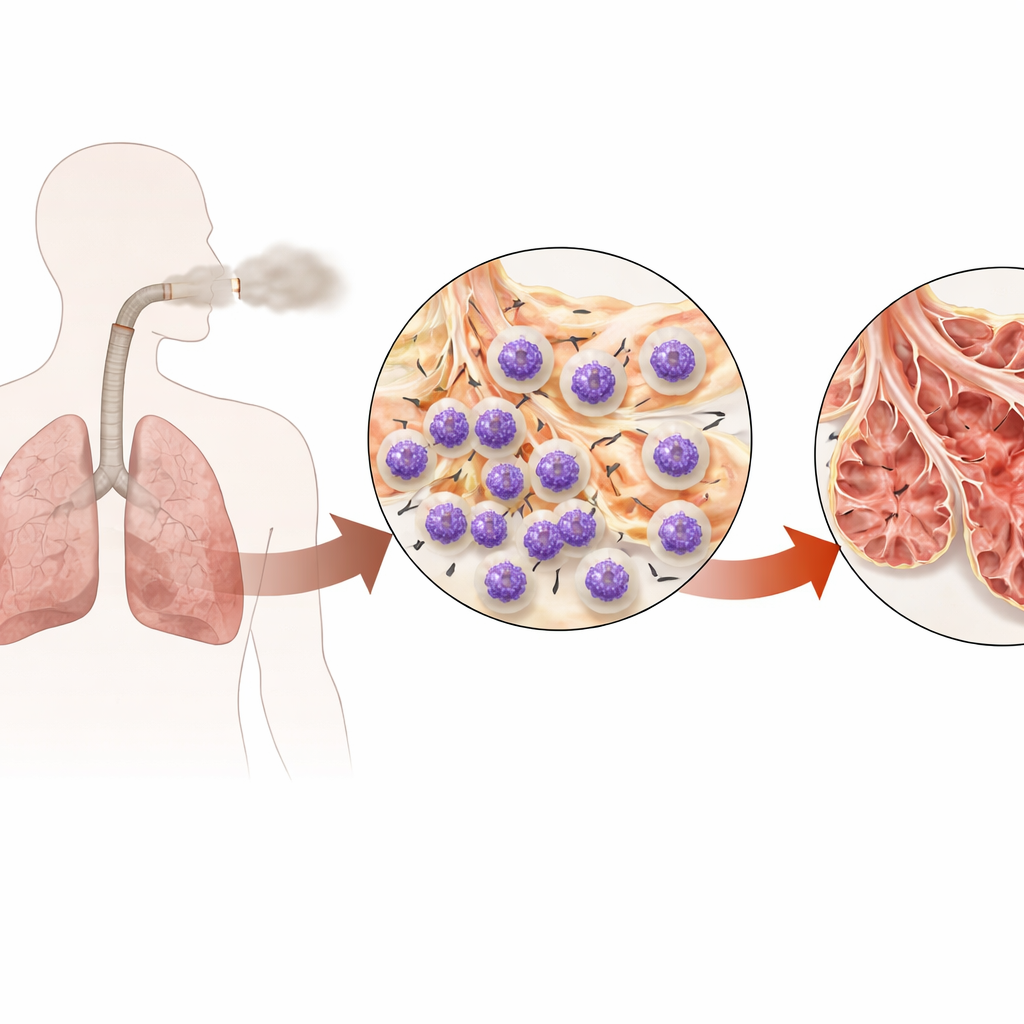
Une maladie pulmonaire tenace alimentée par des défenseurs hyperactifs
La MPOC cicatrise et creuse lentement les poumons, laissant des voies aériennes épaissies et des alvéoles agrandies et fragiles. Les neutrophiles, cellules immunitaires de première ligne, sont abondants dans les expectorations et le tissu pulmonaire des personnes atteintes de MPOC, et leur présence corrèle avec une altération du flux d’air et de la fonction pulmonaire. Mais simplement atténuer les neutrophiles dans tout l’organisme expose à des infections graves. Les auteurs ont donc posé une question plus ciblée : existe‑t‑il un contrôle interne spécifique aux neutrophiles que la fumée de cigarette détourne pour les maintenir activés, regroupés dans les poumons et nuisibles au tissu à long terme ?
Une « porte » calcique dans les neutrophiles est activée dans la MPOC
L’équipe s’est concentrée sur NCX1, une protéine qui échange des ions sodium et calcium à travers la membrane cellulaire. Dans des échantillons pulmonaires humains, le liquide des voies aériennes et le sang circulant, les niveaux de NCX1 étaient nettement plus élevés dans les neutrophiles de patients présentant une bronchite chronique mixte et un emphysème que chez des personnes sans maladie pulmonaire chronique. Cette augmentation suivait de près des marqueurs d’activation des neutrophiles, ce qui suggère que NCX1 pourrait être plus qu’un simple spectateur. Chez des souris exposées à la fumée de cigarette à long terme, les neutrophiles pulmonaires présentaient également une élévation de NCX1, reflétant les observations humaines.
Comment la fumée pousse les neutrophiles vers un état destructeur
À l’aide de modèles murins et de cellules en culture, les chercheurs ont dévoilé comment NCX1 aide à convertir l’exposition à la fumée de cigarette en inflammation dommageable. Normalement, NCX1 peut expulser le calcium des cellules ; dans certaines conditions il s’inverse et fait entrer du calcium. L’extrait de fumée de cigarette a fortement poussé les neutrophiles vers ce mode « inverse », provoquant une montée de calcium à l’intérieur des cellules. Cette surcharge calcique était essentielle à la formation de filets extracellulaires de neutrophiles (NETs) — des réseaux d’ADN garnis d’enzymes toxiques qui peuvent piéger des microbes mais aussi déchirer les tissus voisins. Lorsque NCX1 était supprimé génétiquement uniquement dans les neutrophiles, ou lorsque son activité en mode inverse était bloquée par un médicament, les neutrophiles exposés à la fumée montraient beaucoup moins d’entrée de calcium et libéraient bien moins de NETs.
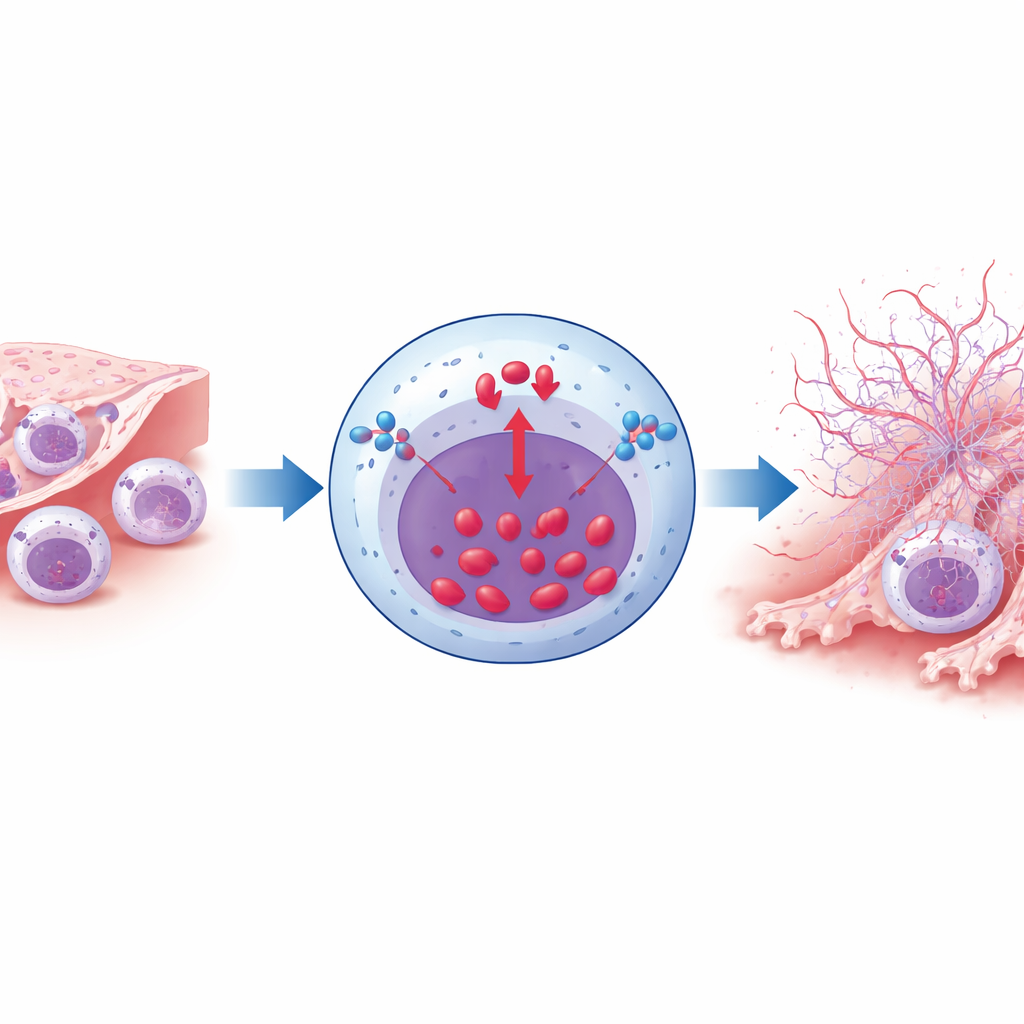
Moins de pièges, moins de cicatrisation, des poumons meilleurs
Les effets en aval de la réduction de la formation de NETs pilotée par NCX1 étaient frappants. Chez les souris exposées à la fumée, la suppression spécifique de NCX1 dans les neutrophiles a entraîné moins de neutrophiles obstruant les poumons, moins d’accumulation de collagène et d’épaississement du muscle lisse autour des voies aériennes, et une destruction des alvéoles moins sévère. Les mesures de la fonction pulmonaire, y compris le débit d’air et la capacité d’expansion des poumons, étaient partiellement préservées par rapport aux animaux témoins. Le blocage indépendant des NETs avec un autre médicament, la Cl‑amidine, a produit des bénéfices similaires : moins de neutrophiles, moins de dommages structurels et une meilleure mécanique respiratoire. Il est important de noter que la suppression de NCX1 dans les neutrophiles n’a pas modifié la façon dont ces cellules se développaient, migraient ou phagocytaient des bactéries dans des conditions normales, ce qui suggère que l’intervention freine principalement leur comportement pathologique dans un environnement chargé de fumée.
Une nouvelle cible plus précise pour le traitement de la MPOC
Pour le lecteur non spécialiste, le message est que l’étude a identifié un interrupteur moléculaire clé — NCX1 fonctionnant en sens inverse — qui aide à expliquer pourquoi les neutrophiles persistent et causent des dommages continus dans les poumons des fumeurs. En apportant un excès de calcium à ces cellules, NCX1 favorise la libération de filets d’ADN collants recouverts d’enzymes qui blessent les structures pulmonaires et entretiennent un environnement chimique qui attire encore les neutrophiles. Diminuer l’activité de cet interrupteur, soit en supprimant NCX1 des neutrophiles soit en bloquant son mode inverse, rompt ce cercle vicieux chez la souris et protège la fonction pulmonaire sans affaiblir globalement le système immunitaire. Bien que des travaux supplémentaires soient nécessaires pour comprendre précisément comment les composants de la cigarette inversent NCX1 et pour tester la sécurité chez l’humain, ces résultats désignent NCX1 et la formation de NETs comme des cibles médicamenteuses prometteuses et plus sélectives pour ralentir ou prévenir les lésions pulmonaires liées à la MPOC.
Citation: Liao, SX., Wang, YW., Shi, LM. et al. NCX1 reverse mode promotes calcium-dependent Neutrophil Extracellular Trap formation and lung damage in chronic obstructive pulmonary disease. Nat Commun 17, 3801 (2026). https://doi.org/10.1038/s41467-026-69636-1
Mots-clés: MPOC, neutrophiles, signalisation calcique, NETs, fumée de cigarette