Clear Sky Science · de
Der NCX1‑Reverse‑Modus fördert calciumabhängige Bildung neutrophiler extrazellulärer Netze und Lungenschaden bei chronisch obstruktiver Lungenerkrankung
Warum winzige Zellen in den Lungen von Rauchern wichtig sind
Die chronisch obstruktive Lungenerkrankung (COPD) ist eine der führenden Todesursachen weltweit und steht meist im Zusammenhang mit jahrelangem Zigarettenrauchen. Viele Betroffene leben mit täglicher Atemnot und häufigen Schüben, doch die verfügbaren Therapien verlangsamen kaum den schleichenden Abbau des Lungengewebes. Diese Studie geht einer bestimmten Art von weißen Blutkörperchen — den Neutrophilen — und einem einzelnen molekularen „Tor“ in ihrer Membran nach, um zu erklären, wie Zigarettenrauch nützliche Immunzellen in Treiber langfristiger Lungenschäden verwandelt. Durch die Identifikation dieses Schalters zeigen die Forschenden einen potenziellen Weg auf, schädliche Entzündungen zu dämpfen, ohne die Abwehrkräfte des Körpers zu kappen.
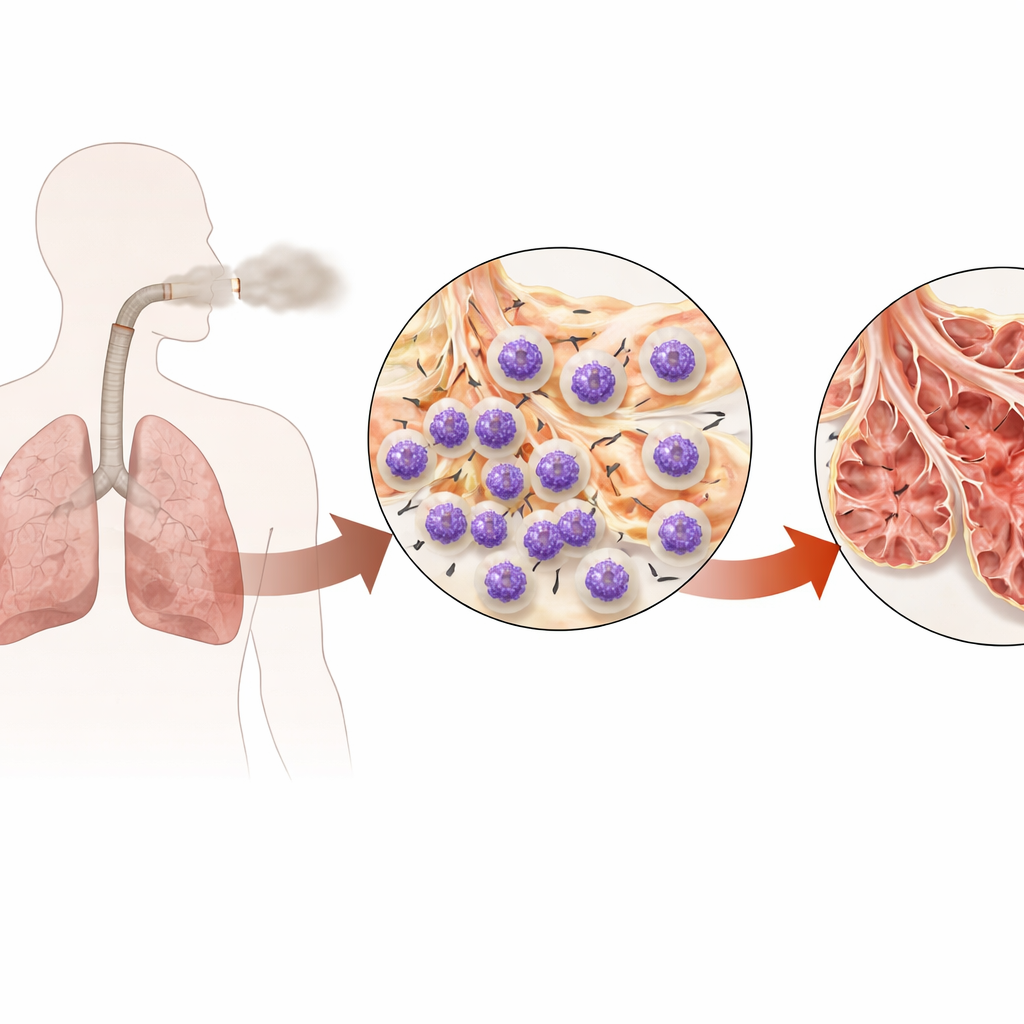
Eine hartnäckige Lungenerkrankung, genährt von überaktiven Verteidigern
COPD vernarbt und hohlraumt die Lunge allmählich, führt zu verdickten Atemwegen und vergrößerten, fragilen Lungenbläschen. Neutrophile, die schnellen Ersthelfer des Immunsystems, finden sich in großer Zahl im Sputum und Lungengewebe von Menschen mit COPD, und ihr Auftreten korreliert mit schlechterer Luftströmung und Lungenfunktion. Neutrophile einfach systemisch zu dämpfen würde jedoch ernste Infektionen begünstigen. Die Autorinnen und Autoren stellten daher eine gezieltere Frage: Gibt es eine spezifische interne Steuerung in Neutrophilen, die Zigarettenrauch kapert, sodass sie aktiviert bleiben, sich in der Lunge ansammeln und langfristig Gewebe schädigen?
Ein Calcium‑Tor in Neutrophilen ist bei COPD hochreguliert
Das Team konzentrierte sich auf NCX1, ein Protein, das Natrium‑ und Calciumionen über die Zellmembran austauscht. In menschlichen Lungenproben, in Flüssigkeit aus den Atemwegen und im zirkulierenden Blut waren die NCX1‑Spiegel in Neutrophilen von Patientinnen und Patienten mit kombiniertem chronischem Bronchitis‑ und Emphysembild deutlich höher als bei Personen ohne chronische Lungenerkrankung. Dieser Anstieg korrelierte eng mit Markern für Neutrophilenaktivierung, was darauf hindeutet, dass NCX1 mehr als ein Zuschauer sein könnte. Bei Mäusen, die langfristig Zigarettenrauch ausgesetzt waren, zeigten Neutrophile in der Lunge ebenfalls erhöhte NCX1‑Werte und spiegelten damit die Humanbefunde wider.
Wie Rauch Neutrophile in einen zerstörerischen Zustand treibt
Mithilfe von Mausmodellen und kultivierten Zellen enthüllten die Forschenden, wie NCX1 dazu beiträgt, Rauchexposition in schädliche Entzündung umzusetzen. Normalerweise kann NCX1 Calcium aus Zellen herausbefördern; unter bestimmten Bedingungen kehrt sich die Richtung um und er bringt Calcium hinein. Zigarettenrauch‑Extrakt trieb Neutrophile stark in diesen „Reverse‑Modus“ und löste einen Calciumanstieg innerhalb der Zellen aus. Diese Calciumüberladung war essentiell für die Bildung neutrophiler extrazellulärer Netze (NETs) — DNA‑Netze mit toxischen Enzymen, die zwar Mikroben fangen, aber auch angrenzendes Gewebe zerreißen können. Wurde NCX1 genetisch nur in Neutrophilen entfernt oder seine Reverse‑Aktivität mit einem Wirkstoff blockiert, zeigten rauchexponierte Neutrophile deutlich weniger Calciumzufluss und setzten deutlich weniger NETs frei.
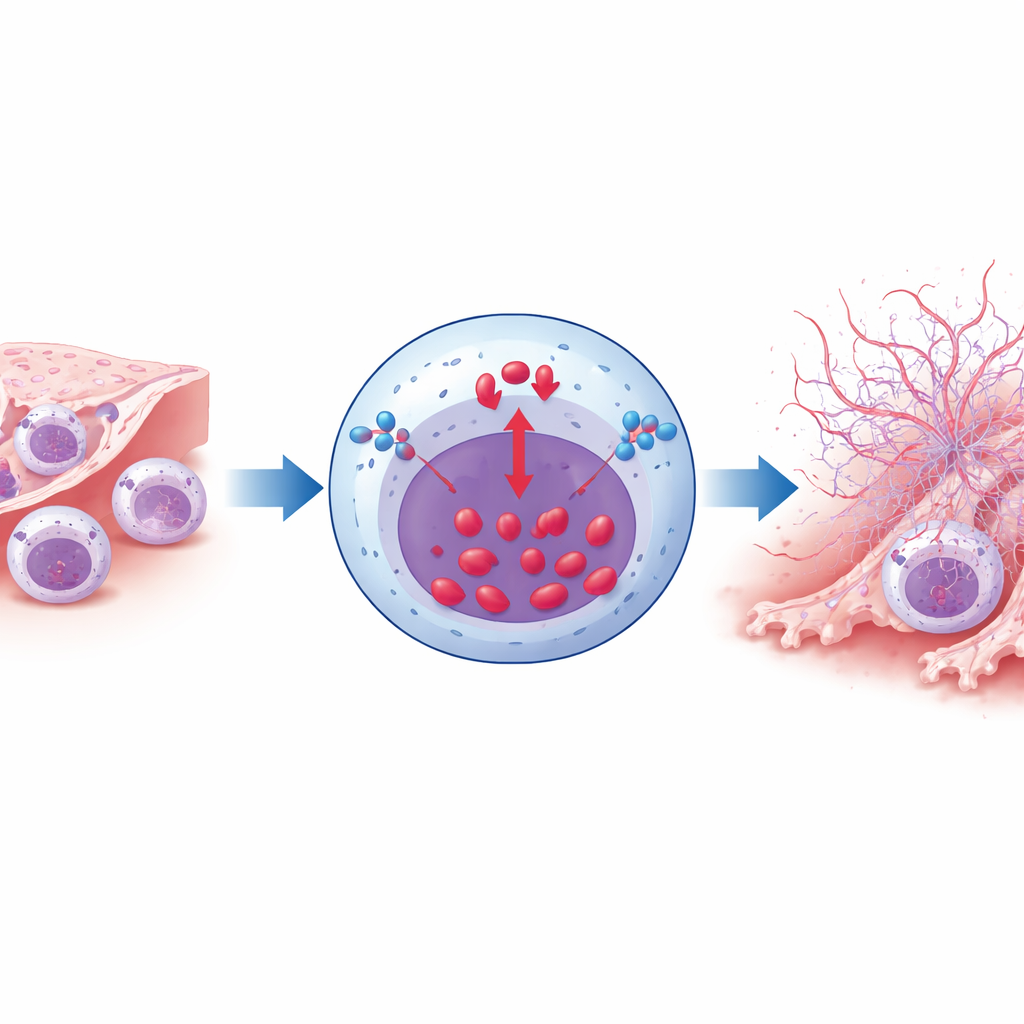
Weniger Fänge, weniger Vernarbung, bessere Lunge
Die downstream Effekte der Reduktion NCX1‑getriebener NET‑Bildung waren eindrücklich. Bei rauchexponierten Mäusen führte die neutrophil‑spezifische NCX1‑Deletion zu weniger in der Lunge verstopfenden Neutrophilen, geringerem Kollagenaufbau und weniger Verdickung der glatten Muskulatur um die Atemwege sowie zu milderer Zerstörung der Lungenbläschen. Messgrößen der Lungenfunktion, einschließlich Luftstrom und Dehnbarkeit der Lunge, blieben im Vergleich zu Kontrolltieren teilweise erhalten. Unabhängig davon führte die Blockade von NETs mit einem anderen Wirkstoff, Cl‑amidin, zu ähnlichen Vorteilen: weniger Neutrophile, weniger strukturelle Schäden und bessere Atemmechanik. Wichtig ist, dass das Entfernen von NCX1 aus Neutrophilen deren Entwicklung, Wanderung oder Phagozytose von Bakterien unter normalen Bedingungen nicht veränderte, was nahelegt, dass die Intervention hauptsächlich ihr pathologisches Verhalten in einer rauchgefüllten Umgebung eindämmt.
Ein neues, präziseres Ziel für die COPD‑Behandlung
Für eine interessierte Leserschaft fasst die Studie zusammen: Sie hat einen zentralen molekularen Schalter identifiziert — NCX1 im Reverse‑Betrieb — der erklärt, warum Neutrophile in den Lungen von Rauchern verharren und fortlaufend Schaden anrichten. Indem NCX1 überschüssiges Calcium in diese Zellen pumpt, fördert es die Freisetzung klebriger, enzymbeschichteter DNA‑Netze, die Lungenstrukturen verletzen und ein chemisches Milieu erhalten, das Neutrophile immer wieder anzieht. Das Herunterregeln dieses Schalters, sei es durch Entfernen von NCX1 aus Neutrophilen oder durch Blockade seiner Reverse‑Aktivität, durchbricht diesen Teufelskreis in Mäusen und schützt die Lungenfunktion, ohne das Immunsystem breit zu schwächen. Während weitere Arbeiten nötig sind, um genau zu verstehen, wie Komponenten des Zigarettenrauchs NCX1 in den Reverse‑Modus kippen und um die Sicherheit beim Menschen zu prüfen, deuten die Befunde darauf hin, dass NCX1 und die NET‑Bildung vielversprechende, selektivere Wirkziele zum Verlangsamen oder Verhindern COPD‑bedingter Lungenschädigung sind.
Zitation: Liao, SX., Wang, YW., Shi, LM. et al. NCX1 reverse mode promotes calcium-dependent Neutrophil Extracellular Trap formation and lung damage in chronic obstructive pulmonary disease. Nat Commun 17, 3801 (2026). https://doi.org/10.1038/s41467-026-69636-1
Schlüsselwörter: COPD, Neutrophile, Calcium‑Signalgebung, NETs, Zigarettenrauch