Clear Sky Science · nl
NCX1 omgekeerde modus bevordert calcium‑afhankelijke vorming van neutrofiele extracellulaire vallen en longschade bij chronische obstructieve longziekte
Waarom kleine cellen in de longen van rokers ertoe doen
Chronische obstructieve longziekte (COPD) is een belangrijke doodsoorzaak wereldwijd, meestal gerelateerd aan jaren van roken. Veel patiënten leven met voortdurende kortademigheid en hebben vaak terugvallen, terwijl de huidige behandelingen weinig doen om de langzame vernietiging van longweefsel te stoppen. Deze studie verdiept zich in één specifiek type witte bloedcel—neutrofielen—en één moleculaire “poort” in hun membraan om uit te leggen hoe sigarettenrook nuttige immuuncellen verandert in motoren van langdurige longschade. Door deze schakel bloot te leggen, tonen de onderzoekers een mogelijke manier om schadelijke ontsteking te temperen zonder de afweer van het lichaam uit te schakelen.
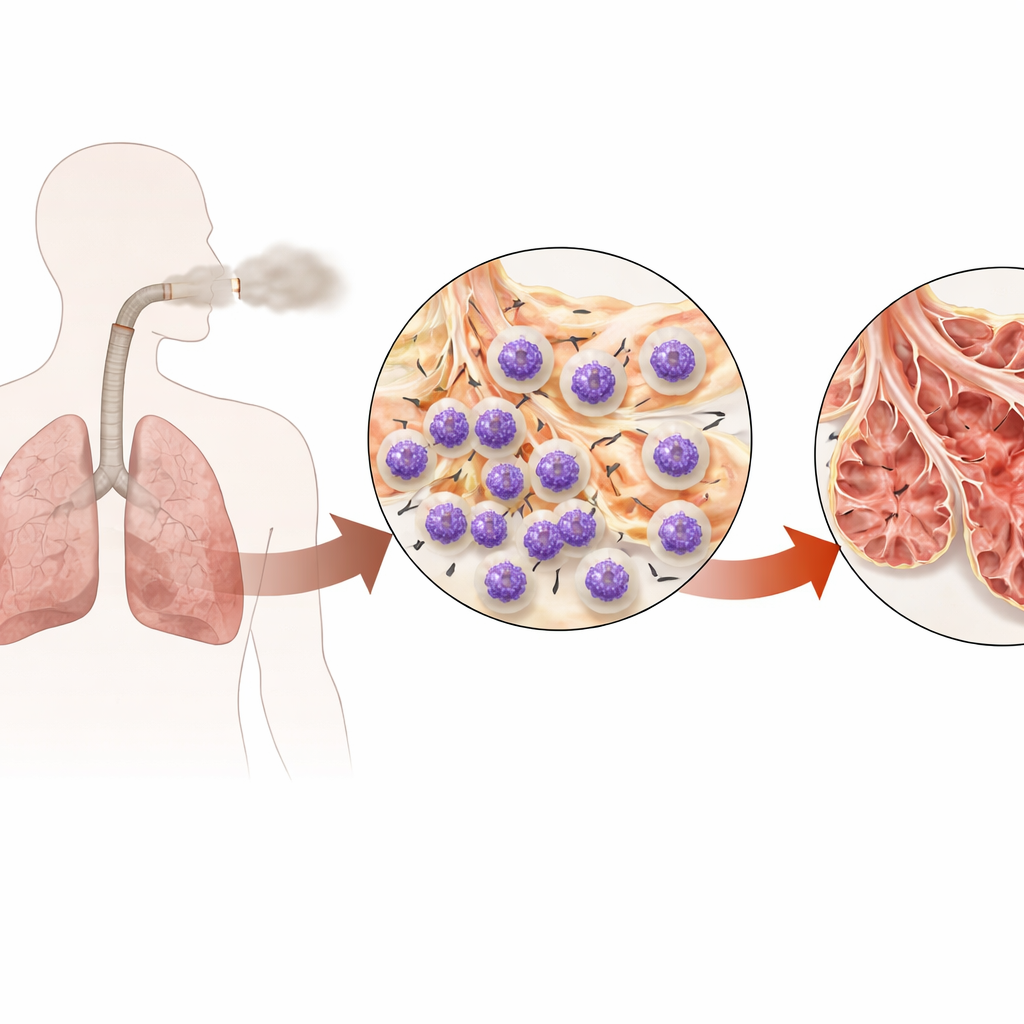
Een hardnekkige longziekte aangedreven door overactieve verdedigers
COPD littekent en holt de longen geleidelijk uit, waardoor luchtwegen verdikt raken en luchtzakjes vergroot en kwetsbaar worden. Neutrofielen, eerstelijns immuuncellen, zijn in overvloed aanwezig in het sputum en longweefsel van mensen met COPD, en hun aanwezigheid correleert met slechtere luchtstroom en longfunctie. Maar neutrofielen simpelweg overal onderdrukken verhoogt het risico op ernstige infecties. De auteurs stelden daarom een gerichtere vraag: is er een specifiek intern regelmechanisme in neutrofielen dat sigarettenrook kaapt om ze geactiveerd, in de longen verzameld en langdurig weefselbeschadigend te houden?
Een calciumpoort in neutrofielen staat op hoger in COPD
Het team richtte zich op NCX1, een eiwit dat natrium- en calciumionen over het celmembraan ruilt. In menselijke longmonsters, luchtwegvocht en circulerend bloed waren NCX1-niveaus opvallend hoger in neutrofielen van patiënten met gemengde chronische bronchitis en emfyseem dan in mensen zonder chronische longziekte. Deze toename correleerde sterk met markers van neutrofielactivatie, wat suggereert dat NCX1 meer dan een voorbijganger kan zijn. Bij muizen die langdurig aan sigarettenrook werden blootgesteld, vertoonden neutrofielen in de longen eveneens verhoogde NCX1, wat de humane bevindingen weerspiegelde.
Hoe rook neutrofielen duwt in een destructieve toestand
Met muismodellen en gekweekte cellen ontdekten de onderzoekers hoe NCX1 helpt om blootstelling aan sigarettenrook om te zetten in schadelijke ontsteking. Normaal kan NCX1 calcium uit cellen verplaatsen; onder bepaalde omstandigheden keert het om en brengt het calcium naar binnen. Sigarettenrookextract dreef neutrofielen krachtig in deze “omgekeerde modus”, wat een piek van intracellulair calcium veroorzaakte. Deze calciumoverbelasting was essentieel voor de vorming van neutrofiele extracellulaire vallen (NETs)—DNA-webben bezaaid met toxische enzymen die microben kunnen vangen maar ook nabijgelegen weefsel kunnen verscheuren. Wanneer NCX1 alleen in neutrofielen genetisch werd verwijderd, of wanneer zijn omgekeerde activiteit met een geneesmiddel werd geblokkeerd, vertoonden rookblootgestelde neutrofielen veel minder calciuminstroom en produceerden ze veel minder NETs.
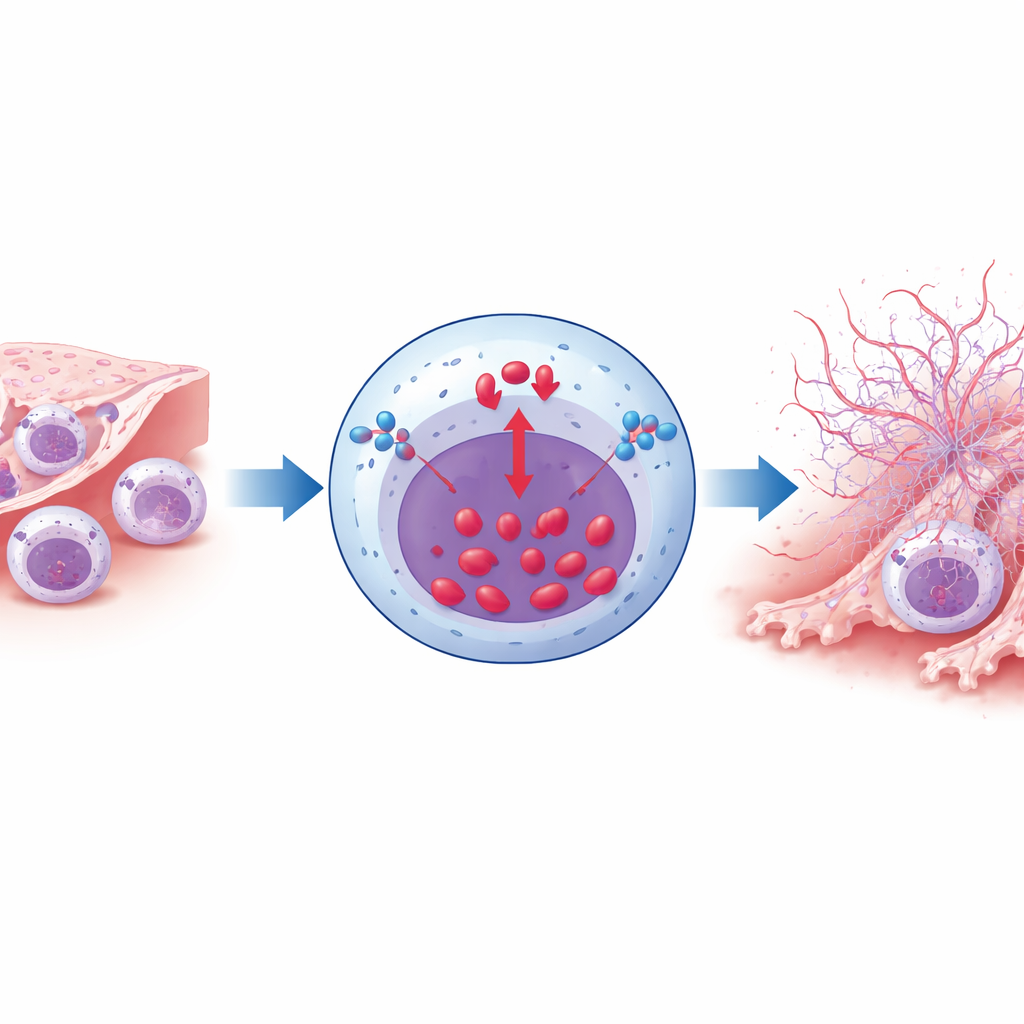
Minder vallen, minder littekenvorming, betere longen
De downstream-effecten van het verminderen van NCX1‑gedreven NET-vorming waren opvallend. Bij rookblootgestelde muizen leidde neutrofiel‑specifieke NCX1‑verwijdering tot minder door neutrofielen verstopte longen, minder collageenophoping en minder verdikking van glad spierweefsel rond de luchtwegen, en milder verlies van luchtzakjes. Maatstaven van longfunctie, waaronder luchtstroom en de rekbaarheid van de longen, werden deels behouden vergeleken met controledieren. Het onafhankelijk blokkeren van NETs met een ander middel, Cl‑amidine, leverde vergelijkbare voordelen op: minder neutrofielen, minder structurele schade en betere ademhalingsmechanica. Belangrijk is dat het verwijderen van NCX1 uit neutrofielen niet beïnvloedde hoe deze cellen zich ontwikkelden, migreerden of bacteriën opnamen onder normale omstandigheden, wat suggereert dat de interventie vooral hun pathologische gedrag in een rookrijke omgeving beperkt.
Een nieuw, preciezer doel voor COPD‑behandeling
Voor de niet‑specialist is de kernboodschap dat de studie een belangrijke moleculaire schakel heeft geïdentificeerd—NCX1 die in omgekeerde richting werkt—die helpt verklaren waarom neutrofielen blijven hangen en voortdurende schade veroorzaken in de longen van rokers. Door overtollig calcium in deze cellen te pompen, bevordert NCX1 de afgifte van plakkerige, door enzymen bedekte DNA‑netten die longstructuren beschadigen en een chemische omgeving in stand houden die neutrofielen blijft aantrekken. Het terugdraaien van deze schakel, hetzij door NCX1 uit neutrofielen te verwijderen of door zijn omgekeerde activiteit te blokkeren, doorbreekt deze vicieuze cirkel bij muizen en beschermt de longfunctie zonder het immuunsysteem breed te verzwakken. Hoewel meer werk nodig is om precies te begrijpen hoe componenten van sigaretten NCX1 in omgekeerde modus schakelen en om de veiligheid bij mensen te testen, wijzen de bevindingen op NCX1 en NET‑vorming als veelbelovende, selectievere medicijntargets om COPD‑gerelateerde longschade te vertragen of te voorkomen.
Bronvermelding: Liao, SX., Wang, YW., Shi, LM. et al. NCX1 reverse mode promotes calcium-dependent Neutrophil Extracellular Trap formation and lung damage in chronic obstructive pulmonary disease. Nat Commun 17, 3801 (2026). https://doi.org/10.1038/s41467-026-69636-1
Trefwoorden: COPD, neutrofielen, calciumsignalering, NETs, sigarettenrook