Clear Sky Science · es
El modo inverso de NCX1 promueve la formación de trampas extracelulares de neutrófilos dependiente del calcio y el daño pulmonar en la enfermedad pulmonar obstructiva crónica
Por qué importan las células diminutas en los pulmones de los fumadores
La enfermedad pulmonar obstructiva crónica (EPOC) es una de las principales causas de muerte en todo el mundo, y con frecuencia está vinculada a años de tabaquismo. Muchos pacientes viven con disnea diaria y sufren exacerbaciones frecuentes, pero los tratamientos actuales hacen poco para detener la lenta destrucción del tejido pulmonar. Este estudio profundiza en un tipo particular de glóbulo blanco —los neutrófilos— y en una única “puerta” molecular de su membrana para explicar cómo el humo del cigarrillo convierte células inmunitarias útiles en motores de daño pulmonar persistente. Al identificar este interruptor, los investigadores revelan una posible forma de calmar la inflamación dañina sin apagar las defensas del organismo.
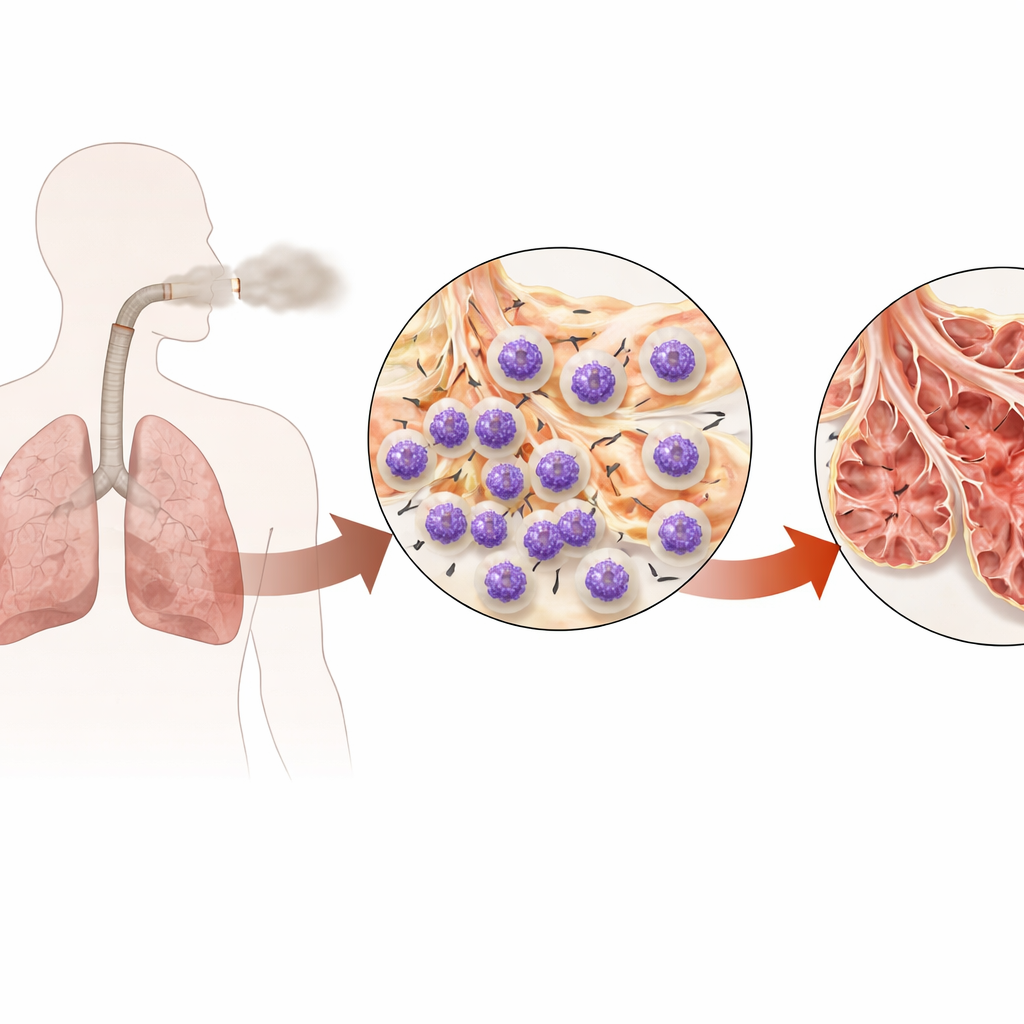
Una enfermedad pulmonar tenaz alimentada por defensores hiperactivos
La EPOC cicatriza y vacía los pulmones de forma progresiva, dejando vías aéreas engrosadas y sacos alveolares agrandados y frágiles. Los neutrófilos, células inmunitarias de primera respuesta, son abundantes en el esputo y el tejido pulmonar de personas con EPOC, y su presencia se asocia con peor flujo aéreo y función pulmonar. Pero atenuar los neutrófilos en todo el organismo conlleva el riesgo de infecciones graves. Por eso los autores plantearon una pregunta más específica: ¿existe un control interno en los neutrófilos que el humo del cigarrillo secuestra para mantenerlos activados, agrupados en los pulmones y lesionando el tejido a largo plazo?
Una puerta de calcio en los neutrófilos está activada en la EPOC
El equipo se centró en NCX1, una proteína que intercambia iones sodio y calcio a través de la membrana celular. En muestras humanas de pulmón, líquido de las vías respiratorias y sangre circulante, los niveles de NCX1 eran notablemente más altos en neutrófilos de pacientes con bronquitis crónica y enfisema mixtos que en personas sin enfermedad pulmonar crónica. Este aumento se correlacionó estrechamente con marcadores de activación neutrofílica, lo que sugiere que NCX1 podría ser más que un mero espectador. En ratones expuestos a humo de cigarrillo a largo plazo, los neutrófilos pulmonares también mostraron NCX1 elevado, reflejando los hallazgos humanos.
Cómo el humo empuja a los neutrófilos hacia un estado destructivo
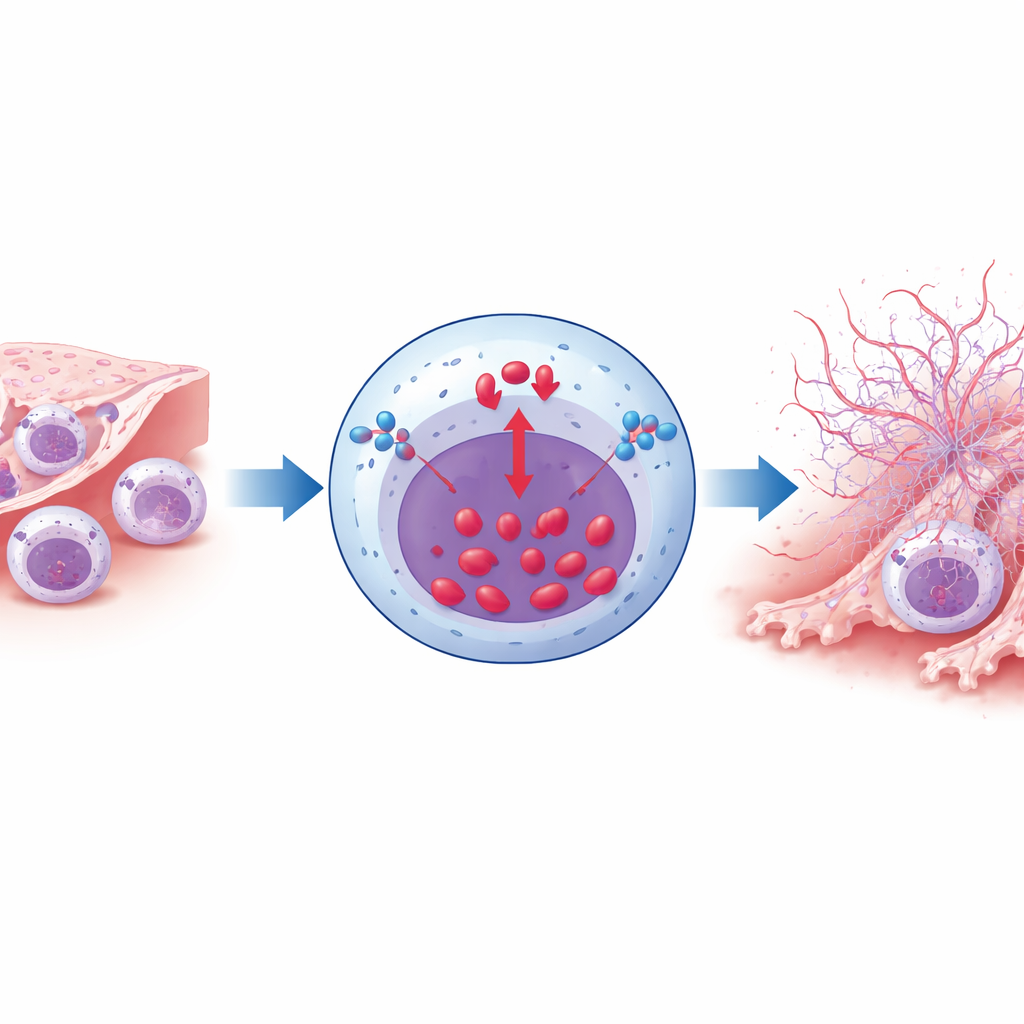
Usando modelos de ratón y células en cultivo, los investigadores desentrañaron cómo NCX1 ayuda a convertir la exposición al humo de cigarrillo en inflamación dañina. Normalmente, NCX1 puede mover calcio fuera de las células; bajo ciertas condiciones invierte su funcionamiento y aporta calcio hacia dentro. El extracto de humo de cigarrillo empujó con fuerza a los neutrófilos hacia este “modo inverso”, provocando una oleada de calcio intracelular. Esta sobrecarga de calcio fue esencial para la formación de trampas extracelulares de neutrófilos (NETs): redes de ADN salpicadas de enzimas tóxicas que pueden atrapar microbios pero también desgarrar el tejido cercano. Cuando NCX1 se eliminó genéticamente solo en neutrófilos, o cuando su actividad inversa se bloqueó con un fármaco, los neutrófilos expuestos al humo mostraron mucho menos influjo de calcio y liberaron muchas menos NETs.
Menos trampas, menos cicatrización, pulmones mejores
Los efectos posteriores de reducir la formación de NETs impulsada por NCX1 fueron llamativos. En ratones expuestos al humo, la eliminación específica de NCX1 en neutrófilos condujo a menos neutrófilos obstruyendo los pulmones, menor acumulación de colágeno y engrosamiento de la musculatura lisa alrededor de las vías respiratorias, y una destrucción más moderada de los sacos alveolares. Las medidas de función pulmonar, incluido el flujo aéreo y la capacidad de expansión de los pulmones, se preservaron parcialmente en comparación con los animales control. Bloquear las NETs de forma independiente con otro fármaco, Cl‑amidine, produjo beneficios similares: menos neutrófilos, menos daño estructural y mejor mecánica respiratoria. Es importante que eliminar NCX1 de los neutrófilos no alteró cómo se desarrollaban, migraban o fagocitaban bacterias en condiciones normales, lo que sugiere que la intervención frena principalmente su comportamiento patológico en un entorno expuesto al humo.
Un objetivo nuevo y más preciso para el tratamiento de la EPOC
Para un lector no especializado, el mensaje es que el estudio ha identificado un interruptor molecular clave —NCX1 funcionando en reversa— que ayuda a explicar por qué los neutrófilos se mantienen y causan daño continuo en los pulmones de los fumadores. Al introducir calcio en exceso en estas células, NCX1 promueve la liberación de redes pegajosas de ADN recubiertas de enzimas que lesionan las estructuras pulmonares y mantienen un entorno químico que atrae a más neutrófilos. Atajar este interruptor, ya sea eliminando NCX1 de los neutrófilos o bloqueando su actividad inversa, rompe este ciclo vicioso en ratones y protege la función pulmonar sin debilitar ampliamente el sistema inmune. Aunque se necesita más trabajo para entender exactamente cómo los componentes del cigarrillo invierten NCX1 y para evaluar la seguridad en humanos, los hallazgos señalan a NCX1 y a la formación de NETs como objetivos farmacológicos prometedores y más selectivos para ralentizar o prevenir el daño pulmonar relacionado con la EPOC.
Cita: Liao, SX., Wang, YW., Shi, LM. et al. NCX1 reverse mode promotes calcium-dependent Neutrophil Extracellular Trap formation and lung damage in chronic obstructive pulmonary disease. Nat Commun 17, 3801 (2026). https://doi.org/10.1038/s41467-026-69636-1
Palabras clave: EPOC, neutrófilos, señalización del calcio, NETs, humo de cigarrillo