Clear Sky Science · pl
Tryb odwrotny NCX1 sprzyja zależnemu od wapnia tworzeniu neutrofilowych pułapek zewnątrzkomórkowych i uszkodzeniom płuc w przewlekłej obturacyjnej chorobie płuc
Dlaczego małe komórki w płucach palacza mają znaczenie
Przewlekła obturacyjna choroba płuc (POChP) jest jedną z głównych przyczyn zgonów na świecie, najczęściej związana z wieloletnim paleniem papierosów. Wielu pacjentów cierpi na codzienną duszność i częste zaostrzenia, a obecne terapie niewiele robią, by zatrzymać stopniowe niszczenie tkanki płucnej. Badanie to zagłębia się w jeden konkretny rodzaj białej krwi — neutrofile — oraz w pojedynczą molekularną „bramę” na ich powierzchni, aby wyjaśnić, jak dym papierosowy zmienia pomocne komórki odpornościowe w silniki długotrwałych uszkodzeń płuc. Wskazując na ten przełącznik, badacze ujawniają potencjalny sposób złagodzenia szkodliwego zapalenia bez wyłączania obrony organizmu.
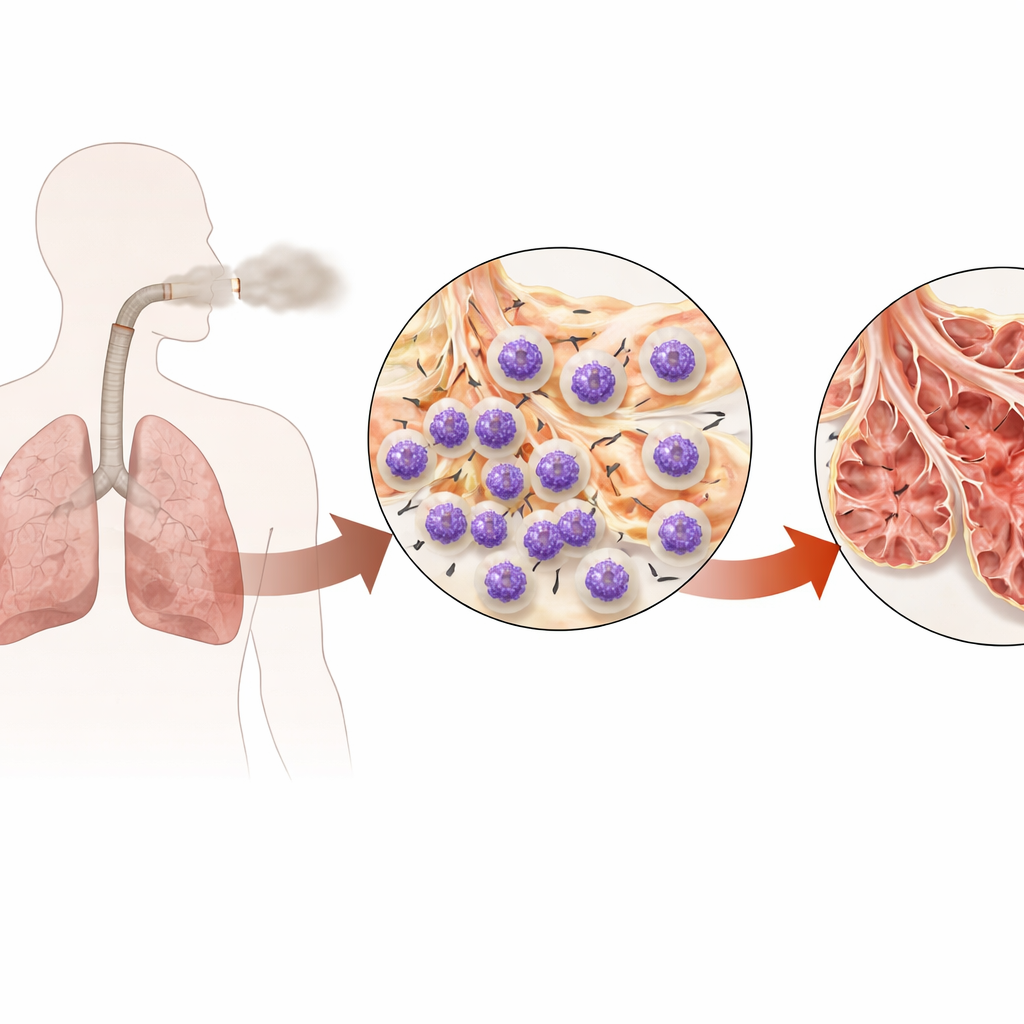
Uparta choroba płuc napędzana przez nadaktywne komórki obronne
POChP stopniowo bliznuje i wydrąża płuca, pozostawiając pogrubione drogi oddechowe i powiększone, kruche pęcherzyki płucne. Neutrofile, komórki odpornościowe działające jako pierwsze, są obfite w plwocinie i tkance płucnej osób z POChP, a ich obecność koreluje z gorszym przepływem powietrza i funkcją płuc. Jednak proste tłumienie neutrofili w całym organizmie niesie ryzyko poważnych zakażeń. Autorzy postawili więc bardziej ukierunkowane pytanie: czy istnieje specyficzny wewnętrzny mechanizm w neutrofilach, który dym papierosowy zawłaszcza, utrzymując je w stanie aktywacji, skupiskach w płucach i długotrwałym uszkadzaniu tkanek?
W neutrofilach wzrasta aktywność bramki wapniowej w POChP
Zespół skupił się na NCX1, białku wymieniającym jony sodu i wapnia przez błonę komórkową. W ludzkich próbkach płuc, płynach z dróg oddechowych i krwi obwodowej poziomy NCX1 były wyraźnie wyższe w neutrofilach pacjentów z mieszanym przewlekłym zapaleniem oskrzeli i rozedmą niż u osób bez przewlekłej choroby płuc. Ten wzrost silnie korelował z markerami aktywacji neutrofili, co sugeruje, że NCX1 może być czymś więcej niż biernym obserwatorem. U myszy wystawionych na długotrwałe działanie dymu papierosowego neutrofile w płucach również wykazywały podwyższony poziom NCX1, odzwierciedlając wyniki ludzkie.
Jak dym popycha neutrofile w stronę destrukcji
Wykorzystując modele mysie i hodowle komórkowe, badacze odkryli, jak NCX1 pomaga przekształcić ekspozycję na dym w szkodliwe zapalenie. Zwykle NCX1 może wypompowywać wapń z komórek; w określonych warunkach odwraca kierunek i sprowadza wapń do wnętrza. Ekstrakt z dymu papierosowego silnie wymuszał „tryb odwrotny” NCX1 w neutrofilach, powodując nagły napływ wapnia do komórek. To przeciążenie wapniem było kluczowe dla tworzenia neutrofilowych pułapek zewnątrzkomórkowych (NETów) — sieci DNA obłożonych toksycznymi enzymami, które mogą unieruchamiać drobnoustroje, ale też niszczą sąsiednie tkanki. Gdy NCX1 został genetycznie usunięty tylko w neutrofilach, lub gdy jego odwrotna aktywność została zablokowana lekiem, neutrofile wystawione na dym wykazywały znacznie mniejszy napływ wapnia i uwalniały znacznie mniej NETów.
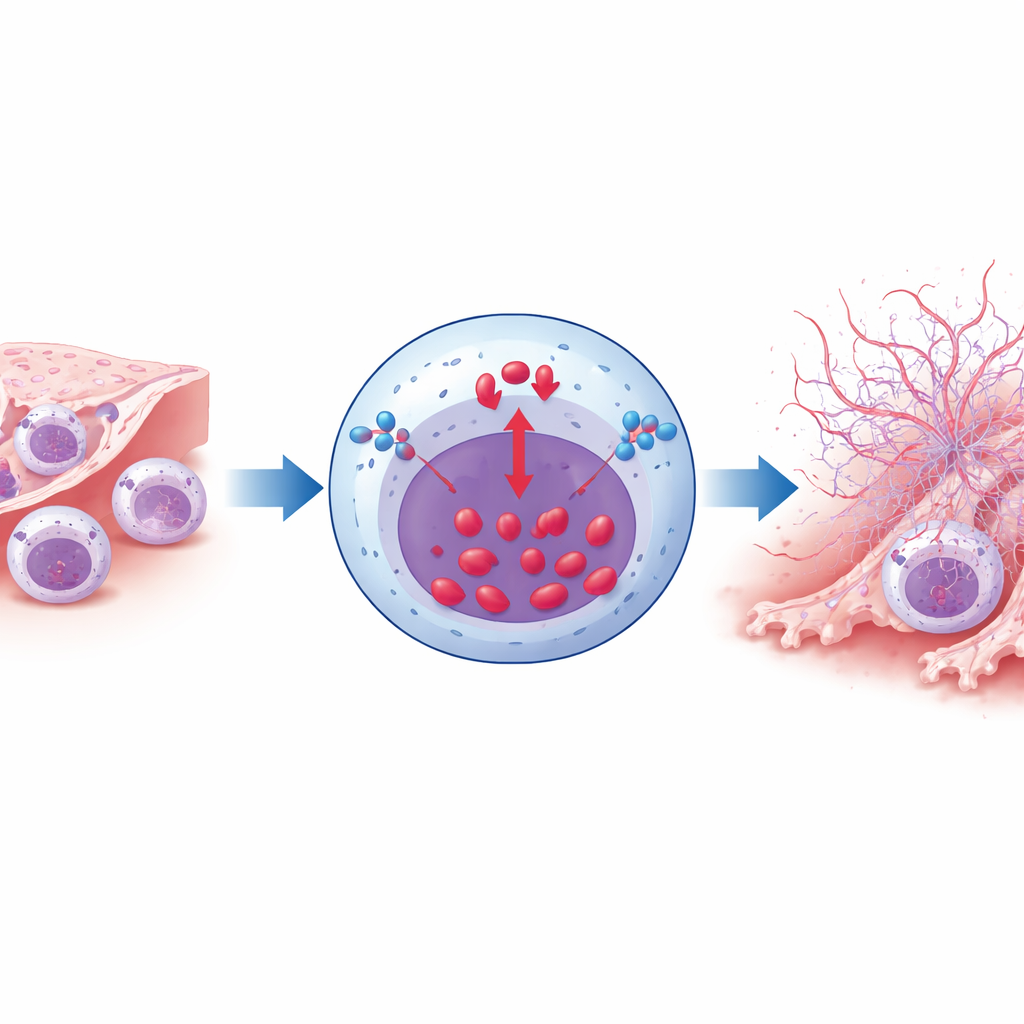
Mniej pułapek, mniej bliznowacenia, lepsze płuca
Skutki zmniejszenia tworzenia NETów napędzanego przez NCX1 były uderzające. U myszy narażonych na dym usunięcie NCX1 specyficznie w neutrofilach prowadziło do mniejszej liczby neutrofili zalegających w płucach, mniejszego odkładania kolagenu i pogrubienia mięśni gładkich wokół dróg oddechowych oraz łagodniejszego niszczenia pęcherzyków płucnych. Parametry funkcji płuc, w tym przepływ powietrza i zdolność płuc do rozprężania się, były częściowo zachowane w porównaniu z kontrolnymi zwierzętami. Niezależne blokowanie NETów innym lekiem, Cl‑amidiną, dało podobne korzyści: mniej neutrofili, mniej uszkodzeń strukturalnych i lepsza mechanika oddychania. Co ważne, usunięcie NCX1 z neutrofili nie zmieniało w normalnych warunkach ich dojrzewania, migracji ani fagocytozy bakterii, co sugeruje, że interwencja głównie ogranicza ich patologiczne zachowanie w środowisku wypełnionym dymem.
Nowy, bardziej precyzyjny cel w leczeniu POChP
Dla czytelnika nieznającego tematu przekaz jest taki: badanie zidentyfikowało kluczowy molekularny przełącznik — NCX1 pracujący w trybie odwrotnym — który pomaga wyjaśnić, dlaczego neutrofile utrzymują się i powodują ciągłe szkody w płucach palaczy. Wpychając nadmiar wapnia do tych komórek, NCX1 sprzyja uwalnianiu lepkawego DNA pokrytego enzymami, które uszkadzają struktury płuc i utrzymują chemiczne środowisko przyciągające kolejne neutrofile. Przygaszenie tego przełącznika, poprzez usunięcie NCX1 z neutrofili lub zablokowanie jego odwrotnej aktywności, przerywa ten błędne koło u myszy i chroni funkcję płuc bez szerokiego osłabiania układu odpornościowego. Choć potrzebne są dalsze badania, by dokładnie zrozumieć, które składniki dymu odwracają NCX1 i by ocenić bezpieczeństwo u ludzi, wyniki wskazują na NCX1 i tworzenie NETów jako obiecujące, bardziej selektywne cele farmakologiczne do spowolnienia lub zapobiegania uszkodzeniom płuc związanym z POChP.
Cytowanie: Liao, SX., Wang, YW., Shi, LM. et al. NCX1 reverse mode promotes calcium-dependent Neutrophil Extracellular Trap formation and lung damage in chronic obstructive pulmonary disease. Nat Commun 17, 3801 (2026). https://doi.org/10.1038/s41467-026-69636-1
Słowa kluczowe: POChP, neutrofile, sygnalizacja wapniowa, NETy, dym tytoniowy