Clear Sky Science · ru
Когнитивные траектории у пациентов с болезнью Паркинсона: обзор влияния глубокой стимуляции таламуса субталамического ядра (STN-DBS) и новых адаптивных стратегий
Почему стимуляция мозга при болезни Паркинсона важна
Болезнь Паркинсона наиболее известна тремором и замедлением движений, но многих людей не меньше беспокоят провалы в памяти, трудности с подбором слов и проблемы с концентрацией. Чтобы облегчить двигательные нарушения, врачи всё чаще применяют глубокую стимуляцию мозга (DBS), при которой тонкие электроды имплантируют в глубокие структуры мозга. Этот обзор отвечает на вопрос, который часто задают пациенты и их близкие: как это лечение влияет на мышление и настроение в долгосрочной перспективе и могут ли новые «умные» варианты DBS защищать разум так же, как и тело?
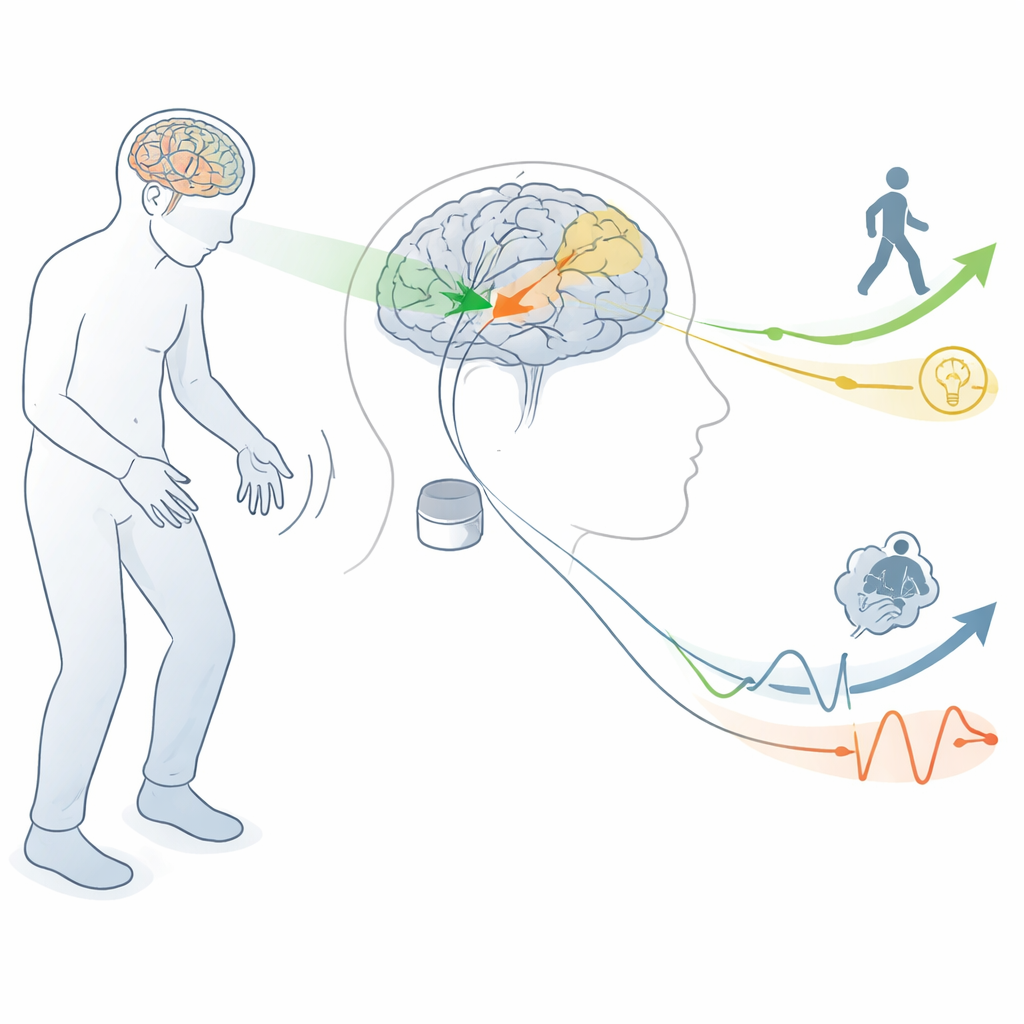
Цепь в мозге, отвечающая за движение и мышление
Авторы начинают с объяснения того, как болезнь Паркинсона нарушает мозговые цепи, которые обычно помогают нам инициировать и контролировать движения. Небольшая область, называемая субталамическим ядром, глубоко в мозге, становится гиперактивной при потере нейромедиатора дофамина. Высокочастотная DBS этой области (STN‑DBS) может успокаивать патологическую активность и значительно улучшать тремор, ригидность и непроизвольные движения. Однако та же область также связана с участками мозга, поддерживающими речь, планирование, эмоции и мотивацию. Такое совпадение означает, что при стимуляции для улучшения движения врачи неизбежно затрагивают цепи, вовлечённые в мышление и чувствование.
Что происходит с мышлением после DBS
Опираясь на рандомизированные исследования, долгосрочные наблюдения и мета‑анализы, обзор выявляет ясную картину. Общий уровень интеллекта и повседневные мыслительные навыки обычно сохраняются, и многие пациенты отмечают улучшение эмоционального состояния после операции. Тем не менее постоянно выявляется одна специфическая слабость: затруднение быстрого подбора слов, навык, проверяемый просьбой назвать как можно больше предметов из заданной категории. Некоторые исследования также сообщают о лёгких изменениях в планировании, гибкости мышления и памяти в течение многих лет. Эти эффекты, как правило, умеренные, и многие пациенты по‑прежнему отмечают улучшение качества жизни за счёт лучшей подвижности и настроения. Важно, что долгосрочные данные указывают на то, что более широкое снижение мыслительных функций в основном отражает естественное прогрессирование болезни Паркинсона, а не саму стимуляцию.
Почему эффекты отличаются у разных людей
Не у всех пациентов наблюдаются одинаковые когнитивные изменения после STN‑DBS. Обзор выделяет несколько причин такой вариабельности. Имеют значение возраст и исходный уровень когнитивных функций: у пожилых людей и у тех, у кого уже есть лёгкие когнитивные нарушения, более высокий риск последующего ухудшения. Ключевое значение также имеет точное положение электрода в субталамическом ядре. Контакты, расположенные ближе к областям, связанным с речью и настроением, с большей вероятностью влияют на подбор слов и эмоциональное состояние. Помимо хирургии и стимуляции, на уязвимость влияют особенности самой болезни — такие как подтип Паркинсона, нарушения сна, перекрывающиеся патологии мозга, гены и общее состояние мозга. Депрессия, тревога и изменения в медикаментозной терапии могут дополнительно усложнять картину, поэтому тщательная предоперационная оценка и последующее наблюдение крайне важны.
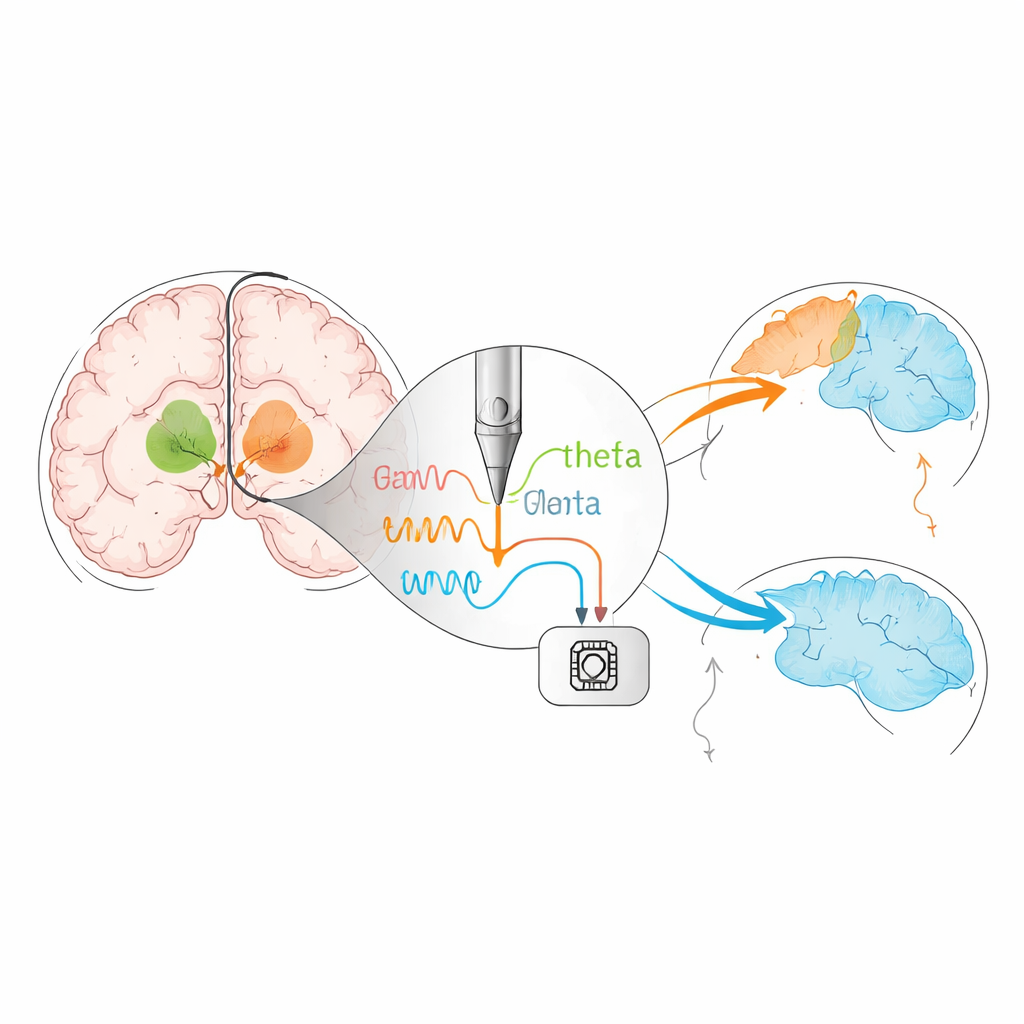
От фиксированной стимуляции к «умной»
Традиционная DBS подаёт равноинтервальные импульсы круглосуточно, независимо от того, чем занят человек и как меняется активность его мозга. В обзоре описан следующий шаг: замкнутая, или адаптивная, DBS. В этом подходе устройство «слушает» собственные электрические ритмы мозга и в реальном времени корректирует стимуляцию. Ранние системы отслеживают бета‑диапазон активности — ритм мозга, связанный с ригидностью и замедлением — чтобы более точно подбирать стимуляцию для двигательной функции. Новые исследования указывают, что другие ритмы, например более медленные тета‑волны, могут отражать внимание, самоконтроль или состояние сна. Тщательно синхронизированная стимуляция на этих частотах в небольших исследованиях показала, что решения становятся более осторожными и улучшается рабочая память без вреда для движений, что наводит на мысль, что в будущем устройства могут облегчать когнитивные и проблемы со сном наряду с моторными симптомами.
Перспективы и препятствия в защите ума
Авторы приходят к выводу, что для большинства людей с болезнью Паркинсона STN‑DBS приносит явные и стойкие двигательные преимущества, а изменения в мышлении, как правило, ограничиваются специфическими навыками, такими как быстрый подбор слов. Истинная перспектива заключается в применении более умной, основанной на обратной связи стимуляции, чтобы лучше сбалансировать моторные выгоды и защиту настроения и когниций. Для этого исследователям необходимо выявить надёжные мозговые сигналы, отражающие немоторные симптомы, усовершенствовать методы визуализации и хирургические техники, чтобы сохранять чувствительные цепи, и провести долгосрочные испытания, отслеживающие как двигательную, так и психическую динамику. Если эти задачи будут решены, будущие системы DBS смогут не только стабилизировать тело, но и помогать сохранять независимость, память, речь и способность принимать решения в ходе болезни Паркинсона.
Цитирование: Almeida, V., Herz, D.M., Blech, J. et al. Cognitive trajectories in Parkinson’s disease patients, a review on the impact of subthalamic deep brain stimulation (STN-DBS) and emerging adaptive strategies. Transl Psychiatry 16, 233 (2026). https://doi.org/10.1038/s41398-026-04013-6
Ключевые слова: Болезнь Паркинсона, глубокая стимуляция мозга, когниция, замкнутая нейромодуляция, субталамическое ядро