Clear Sky Science · fr
Trajectoires cognitives chez les patients atteints de maladie de Parkinson : revue de l’impact de la stimulation cérébrale profonde sous‑thalamique (STN‑DBS) et des stratégies adaptatives émergentes
Pourquoi la stimulation cérébrale dans la maladie de Parkinson compte
La maladie de Parkinson est surtout connue pour les tremblements et la lenteur des mouvements, mais nombre de personnes sont tout aussi gênées par des oublis, des difficultés à trouver leurs mots et des problèmes de concentration. Pour atténuer les troubles moteurs, les médecins recourent de plus en plus à la stimulation cérébrale profonde (DBS), qui consiste à implanter de fines électrodes dans des zones profondes du cerveau. Cette revue aborde une question souvent posée par les patients et leurs familles : quel est l’effet de ce traitement sur les fonctions cognitives et l’humeur à long terme, et les formes « intelligentes » de DBS pourraient‑elles protéger l’esprit autant que le corps ?
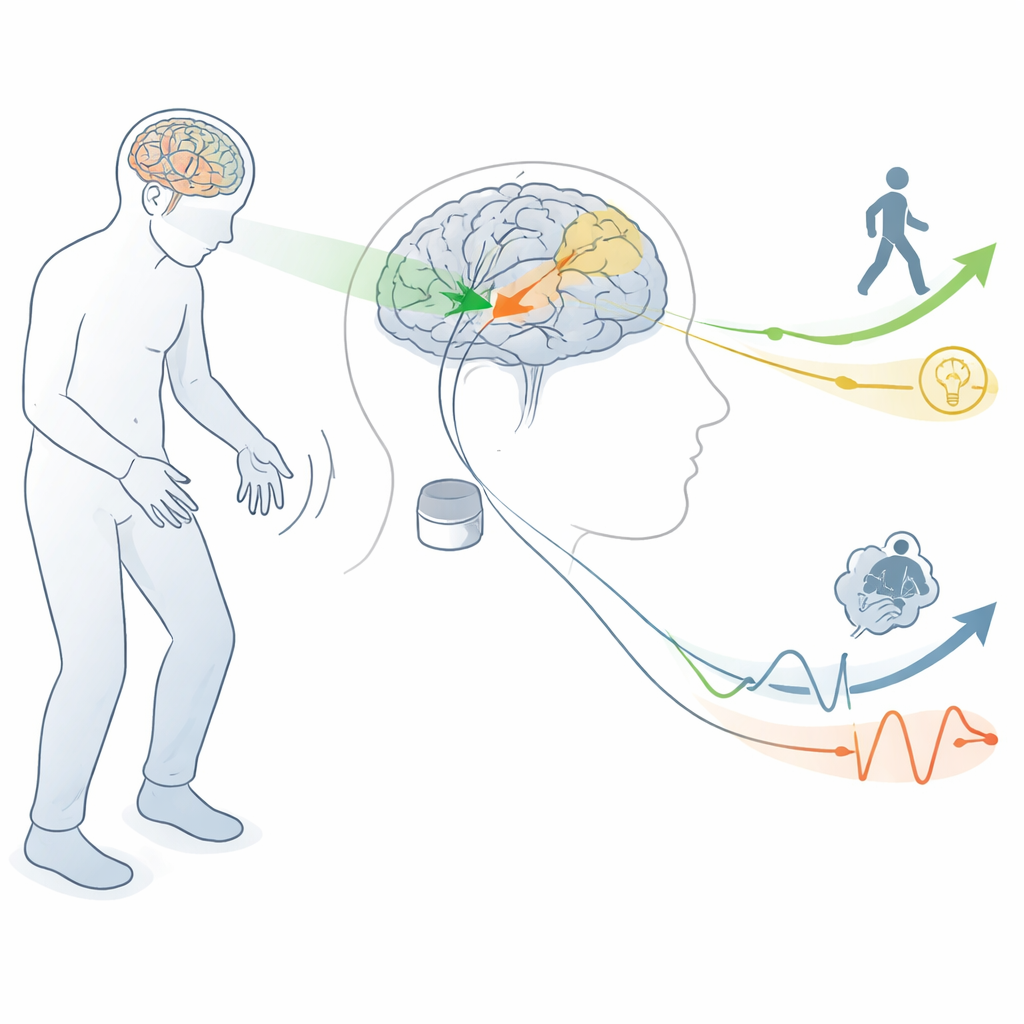
Le circuit cérébral derrière le mouvement et la pensée
Les auteurs commencent par expliquer comment la maladie de Parkinson perturbe les circuits cérébraux qui nous aident normalement à initier et contrôler le mouvement. Une petite région appelée noyau sous‑thalamique, enfouie en profondeur, devient hyperactive quand le messager chimique dopamine disparaît. La stimulation haute fréquence de cette région (STN‑DBS) peut calmer cette activité anormale et améliorer considérablement les tremblements, la raideur et les mouvements involontaires. Mais cette même zone est aussi connectée à des régions impliquées dans le langage, la planification, les émotions et la motivation. Ce chevauchement signifie que lorsque les médecins stimulent pour aider le mouvement, ils peuvent aussi influer sur les circuits liés à la pensée et au ressenti.
Que devient la cognition après la DBS
S’appuyant sur des essais randomisés, des suivis à long terme et des méta‑analyses, la revue identifie un schéma clair. L’intelligence globale et les capacités cognitives de la vie quotidienne sont généralement préservées, et de nombreux patients se sentent mieux sur le plan émotionnel après la chirurgie. Toutefois, une faiblesse spécifique revient systématiquement : la difficulté à trouver rapidement des mots, compétence évaluée en demandant aux personnes de citer le plus d’items possible d’une catégorie. Certaines études rapportent aussi des changements modestes dans la planification, la flexibilité mentale et la mémoire sur plusieurs années. Ces effets sont en règle générale limités, et beaucoup de patients signalent une meilleure qualité de vie car leurs troubles moteurs et leur humeur se sont améliorés. De façon importante, les données à long terme suggèrent que le déclin cognitif plus large reflète surtout la progression naturelle de la maladie plutôt que la stimulation elle‑même.
Pourquoi les effets varient d’une personne à l’autre
Les patients ne présentent pas tous les mêmes changements cognitifs après une STN‑DBS. La revue met en lumière plusieurs raisons à cette variabilité. L’âge et le niveau cognitif de départ comptent : les personnes plus âgées et celles présentant déjà des troubles cognitifs légers sont plus susceptibles de décliner ensuite. L’emplacement précis de l’électrode dans le noyau sous‑thalamique est également crucial. Des contacts plus proches de régions liées au langage et à l’humeur ont plus de chances d’affecter la recherche de mots et l’état émotionnel. Au‑delà de la chirurgie et de la stimulation, des caractéristiques de la maladie elle‑même — sous‑type de Parkinson, troubles du sommeil, pathologies cérébrales superposées, facteurs génétiques et état général du cerveau — déterminent la vulnérabilité. La dépression, l’anxiété et les modifications médicamenteuses peuvent encore compliquer l’évaluation, rendant essentielle une évaluation pré‑chirurgicale et un suivi attentifs.
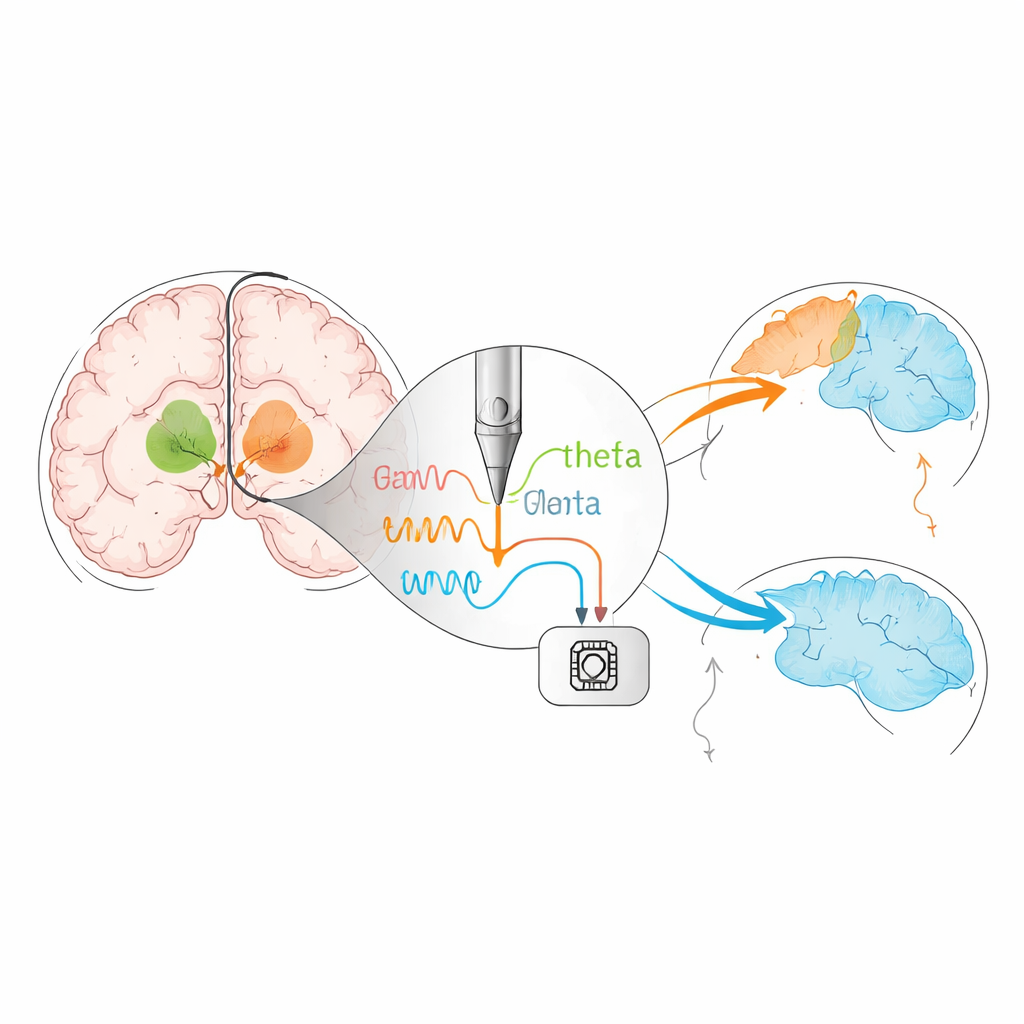
De la stimulation fixe à la stimulation « intelligente »
La DBS traditionnelle délivre des impulsions constantes en permanence, quelle que soit l’activité de la personne ou les variations de l’activité cérébrale. La revue décrit une étape suivante : la DBS en boucle fermée, ou adaptative. Dans cette approche, l’appareil écoute les rythmes électriques du cerveau et ajuste la stimulation en temps réel. Les premiers systèmes suivent l’activité en bande bêta, un rythme cérébral associé à la raideur et à la lenteur, pour ajuster la stimulation en fonction des symptômes moteurs. Des travaux plus récents suggèrent que d’autres rythmes, comme des ondes thêta plus lentes, pourraient refléter l’attention, le contrôle de soi ou l’état de sommeil. Une stimulation soigneusement synchronisée sur ces fréquences a montré dans de petites études qu’elle rendait les décisions plus prudentes et améliorait la mémoire de travail sans nuire au mouvement, laissant penser que des dispositifs futurs pourraient atténuer les troubles cognitifs et du sommeil aussi bien que les symptômes moteurs.
Promesses et obstacles pour protéger l’esprit
Les auteurs concluent que, pour la plupart des personnes atteintes de Parkinson, la STN‑DBS apporte des bénéfices moteurs nets et durables, avec des modifications cognitives généralement limitées à des compétences spécifiques comme la génération rapide de mots. La véritable opportunité réside dans l’utilisation d’une stimulation plus intelligente et guidée par le feedback pour mieux concilier gains moteurs et préservation de l’humeur et des fonctions cognitives. Pour y parvenir, les chercheurs doivent identifier des signaux cérébraux fiables reflétant les symptômes non moteurs, affiner les techniques d’imagerie et chirurgicales pour épargner les circuits sensibles, et mener des essais à long terme qui suivent à la fois les résultats moteurs et cognitifs. Si ces défis sont relevés, les systèmes de DBS futurs pourraient non seulement stabiliser le corps, mais aussi contribuer à préserver l’autonomie, la mémoire, le langage et la prise de décision au cours de la maladie de Parkinson.
Citation: Almeida, V., Herz, D.M., Blech, J. et al. Cognitive trajectories in Parkinson’s disease patients, a review on the impact of subthalamic deep brain stimulation (STN-DBS) and emerging adaptive strategies. Transl Psychiatry 16, 233 (2026). https://doi.org/10.1038/s41398-026-04013-6
Mots-clés: Maladie de Parkinson, stimulation cérébrale profonde, cognition, neuromodulation en boucle fermée, noyau sous‑thalamique