Clear Sky Science · es
Trayectorias cognitivas en pacientes con enfermedad de Parkinson: una revisión sobre el impacto de la estimulación cerebral profunda subtalámica (STN-DBS) y estrategias adaptativas emergentes
Por qué importa la estimulación cerebral en el Parkinson
La enfermedad de Parkinson es más conocida por el temblor y la lentitud de movimientos, pero muchas personas se ven igual de afectadas por fallos de memoria, problemas para encontrar palabras y dificultades para mantener la atención. Para aliviar los problemas de movimiento, los médicos utilizan cada vez más la estimulación cerebral profunda (DBS), en la que se implantan finos electrodos en lo profundo del cerebro. Esta revisión plantea una pregunta que pacientes y familias suelen hacerse: ¿qué hace este tratamiento al pensamiento y al estado de ánimo a largo plazo, y podrían las nuevas formas “inteligentes” de DBS ayudar a proteger la mente además del cuerpo?
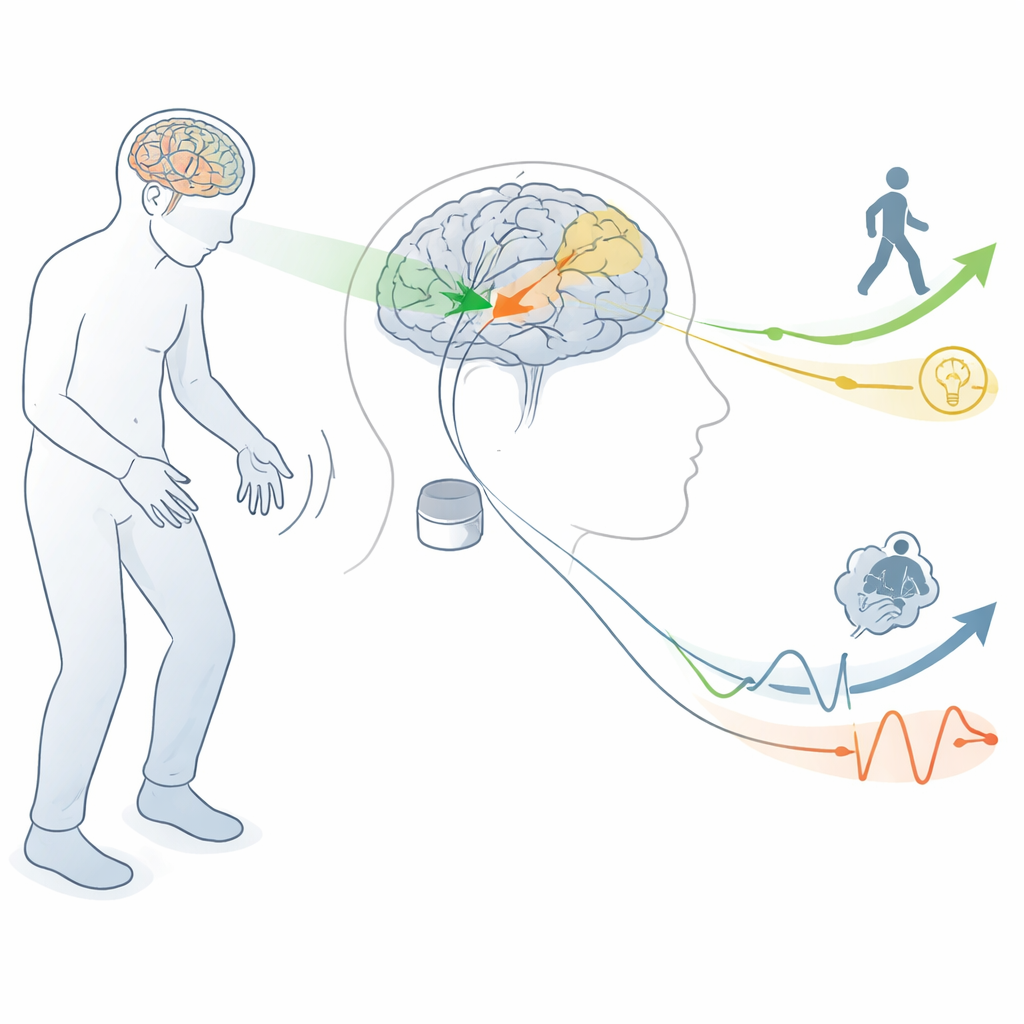
El circuito cerebral detrás del movimiento y el pensamiento
Los autores comienzan explicando cómo el Parkinson interrumpe circuitos cerebrales que normalmente nos ayudan a iniciar y controlar el movimiento. Una pequeña región llamada núcleo subtalámico, enterrada en lo profundo del cerebro, se vuelve hiperactiva cuando se pierde el mensajero químico dopamina. La DBS de alta frecuencia en esta región (STN-DBS) puede calmar la actividad anómala y mejorar considerablemente el temblor, la rigidez y los movimientos no deseados. Pero esta misma área también se conecta con regiones cerebrales que sostienen el lenguaje, la planificación, la emoción y la motivación. Ese solapamiento significa que cuando los médicos estimulan para ayudar el movimiento, también pueden influir en circuitos implicados en el pensamiento y los sentimientos.
Qué ocurre con el pensamiento tras la DBS
Basándose en ensayos aleatorizados, seguimientos a largo plazo y metanálisis, la revisión encuentra un patrón claro. La inteligencia general y el pensamiento en la vida diaria suelen conservarse, y muchos pacientes se sienten mejor emocionalmente después de la cirugía. Sin embargo, una debilidad específica aparece una y otra vez: dificultad para encontrar palabras con rapidez, una habilidad que se evalúa pidiendo a las personas que nombren la mayor cantidad de elementos posible de una categoría. Algunos estudios también informan cambios leves en la planificación, la flexibilidad mental y la memoria a lo largo de muchos años. Estos efectos suelen ser modestos, y muchos pacientes siguen informando una mejor calidad de vida porque su movilidad y su ánimo han mejorado. De forma importante, los datos a largo plazo sugieren que el deterioro más amplio del pensamiento refleja principalmente la progresión natural del Parkinson y no tanto la estimulación en sí misma.
Por qué los efectos difieren entre personas
No todos los pacientes muestran los mismos cambios cognitivos tras la STN-DBS. La revisión destaca varias razones para esta variabilidad. La edad y las habilidades cognitivas basales importan: las personas mayores y quienes ya muestran problemas cognitivos leves tienen más probabilidades de empeorar con el tiempo. La localización precisa del electrodo en el núcleo subtalámico también es crucial. Los contactos más cercanos a regiones vinculadas con el lenguaje y el estado de ánimo tienen más probabilidad de afectar la fluidez verbal y el estado emocional. Más allá de la cirugía y la estimulación, características de la propia enfermedad —como el subtipo de Parkinson, problemas del sueño, patologías cerebrales superpuestas, genética y salud cerebral general— determinan la vulnerabilidad de cada persona. La depresión, la ansiedad y los cambios en la medicación pueden además enturbiar el panorama, por lo que una evaluación prequirúrgica cuidadosa y un seguimiento son esenciales.
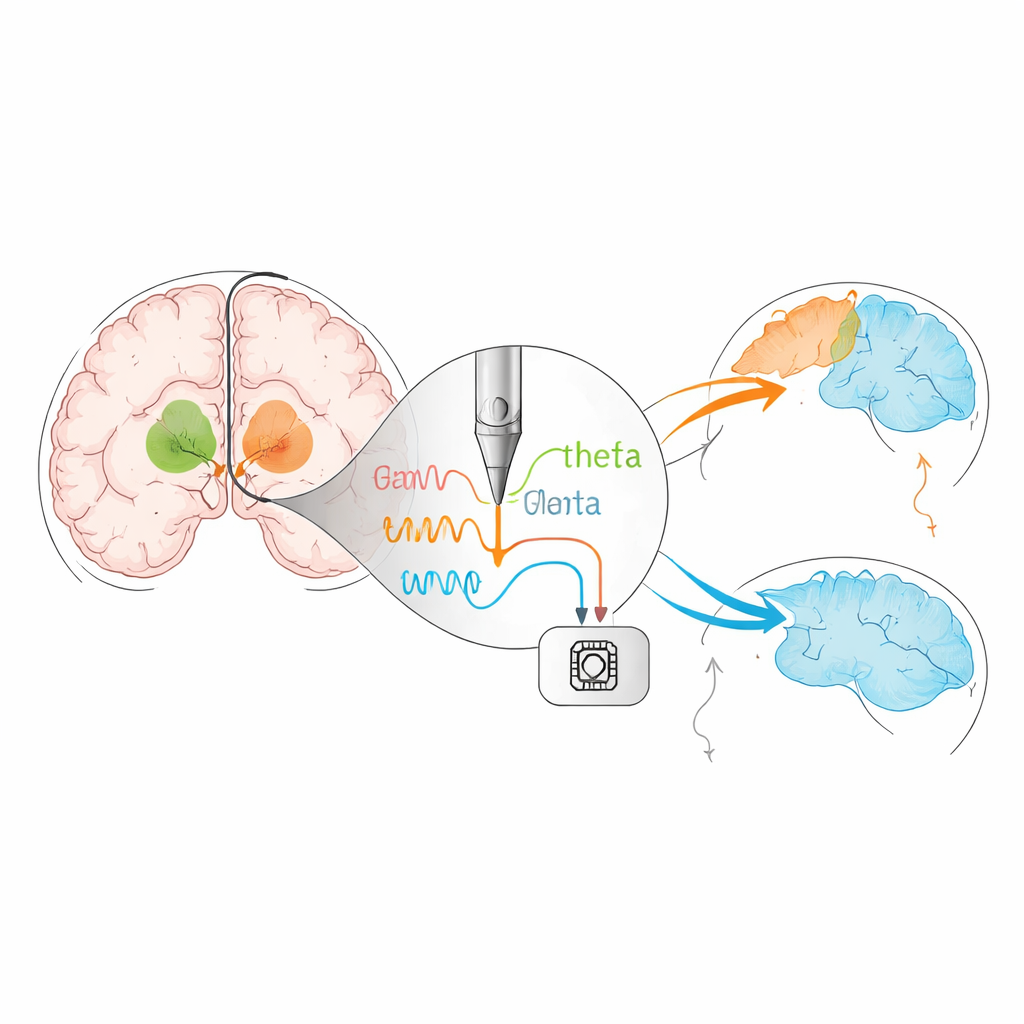
De la estimulación fija a la “inteligente”
La DBS tradicional entrega pulsos constantes las 24 horas, independientemente de lo que la persona esté haciendo o de cómo cambie su actividad cerebral. La revisión describe el siguiente paso: la DBS en bucle cerrado, o adaptativa. En este enfoque, el dispositivo escucha los ritmos eléctricos del propio cerebro y ajusta la estimulación en tiempo real. Los primeros sistemas siguen la actividad en la banda beta, un ritmo cerebral vinculado a la rigidez y la lentitud, para afinar la estimulación orientada al movimiento. Trabajos más recientes sugieren que otros ritmos, como las ondas theta más lentas, pueden reflejar la atención, el autocontrol o el estado de sueño. La estimulación cuidadosamente cronometrada a estas frecuencias ha mostrado en pequeños estudios que puede hacer que las decisiones sean más prudentes y mejorar la memoria de trabajo sin dañar el movimiento, lo que apunta a que dispositivos futuros podrían aliviar problemas cognitivos y del sueño además de los síntomas motores.
Promesas y obstáculos para proteger la mente
Los autores concluyen que para la mayoría de las personas con Parkinson, la STN-DBS aporta beneficios motores claros y duraderos, con cambios cognitivos que suelen limitarse a habilidades concretas como la generación rápida de palabras. La oportunidad real que se abre consiste en usar una estimulación más inteligente, guiada por retroalimentación, para equilibrar mejor las ganancias motoras con la protección del estado de ánimo y la cognición. Para lograrlo, los investigadores deben identificar señales cerebrales fiables que reflejen síntomas no motores, mejorar las técnicas de imagen y quirúrgicas para preservar circuitos sensibles, y realizar ensayos a largo plazo que registren tanto los resultados motores como los mentales. Si se superan estos retos, los futuros sistemas de DBS pueden no solo estabilizar el cuerpo sino también ayudar a preservar la autonomía, la memoria, el lenguaje y la toma de decisiones a lo largo de la enfermedad de Parkinson.
Cita: Almeida, V., Herz, D.M., Blech, J. et al. Cognitive trajectories in Parkinson’s disease patients, a review on the impact of subthalamic deep brain stimulation (STN-DBS) and emerging adaptive strategies. Transl Psychiatry 16, 233 (2026). https://doi.org/10.1038/s41398-026-04013-6
Palabras clave: enfermedad de Parkinson, estimulación cerebral profunda, cognición, neuromodulación en bucle cerrado, núcleo subtalámico