Clear Sky Science · it
Traiettorie cognitive nei pazienti con malattia di Parkinson: una rassegna sull’impatto della stimolazione cerebrale profonda del nucleo subtalamico (STN‑DBS) e sulle strategie adattive emergenti
Perché la stimolazione cerebrale nella malattia di Parkinson è importante
La malattia di Parkinson è più nota per il tremore e il rallentamento dei movimenti, ma molte persone sono altrettanto disturbate da lapsus di memoria, difficoltà a trovare le parole e problemi di attenzione. Per alleviare i disturbi del movimento, i medici ricorrono sempre più spesso alla stimolazione cerebrale profonda (DBS), in cui sottili elettrodi vengono impiantati in profondità nel cervello. Questa rassegna affronta una domanda che pazienti e famiglie si pongono spesso: cosa fa questo trattamento al pensiero e all’umore nel lungo periodo, e le nuove forme “intelligenti” di DBS potrebbero proteggere la mente oltre che il corpo?
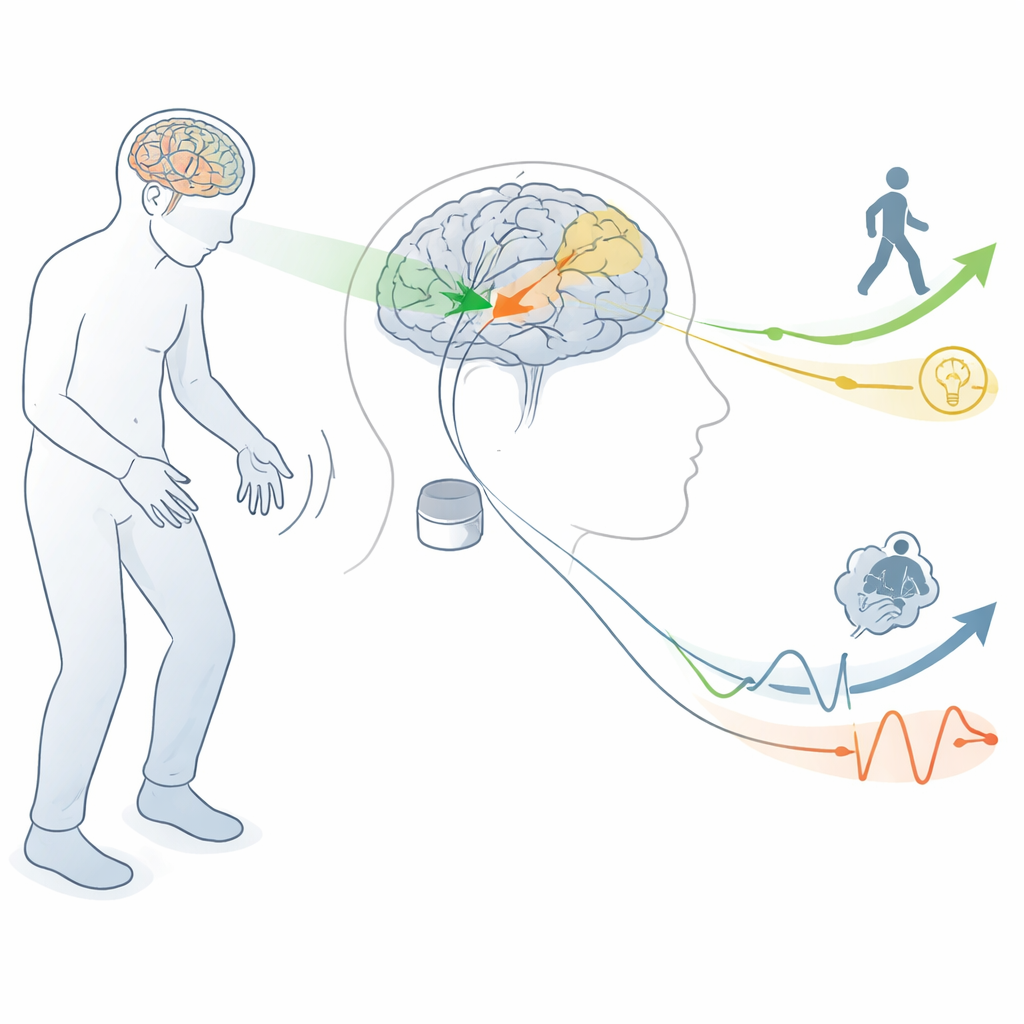
Il circuito cerebrale dietro movimento e pensiero
Gli autori iniziano spiegando come la malattia di Parkinson alteri i circuiti cerebrali che normalmente ci aiutano ad avviare e controllare il movimento. Una piccola area chiamata nucleo subtalamico, situata in profondità nel cervello, diventa iperattiva quando il messaggero chimico dopamina viene a mancare. La DBS ad alta frequenza di questa regione (STN‑DBS) può calmare l’attività anomala e migliorare notevolmente tremore, rigidità e movimenti involontari. Ma la stessa area si connette anche a regioni cerebrali che sostengono linguaggio, pianificazione, emozione e motivazione. Questa sovrapposizione significa che quando i medici stimolano per migliorare il movimento, possono anche influenzare i circuiti coinvolti nel pensiero e nelle emozioni.
Cosa accade al pensiero dopo la DBS
Basandosi su trial randomizzati, follow‑up a lungo termine e meta‑analisi, la rassegna individua un quadro chiaro. L’intelligenza complessiva e il funzionamento cognitivo nella vita quotidiana sono di solito preservati, e molti pazienti riferiscono un miglioramento dell’umore dopo l’intervento. Tuttavia, una debolezza specifica ricorre frequentemente: difficoltà a trovare parole rapidamente, una abilità valutata chiedendo alle persone di elencare il maggior numero possibile di elementi di una categoria. Alcuni studi segnalano anche lievi cambiamenti nella pianificazione, nella flessibilità mentale e nella memoria sul lungo periodo. Questi effetti sono generalmente modesti, e molti pazienti riferiscono comunque un miglioramento della qualità di vita grazie al beneficio sul movimento e sull’umore. È importante sottolineare che i dati a lungo termine suggeriscono che un declino cognitivo più ampio riflette principalmente la progressione naturale del Parkinson piuttosto che la stimolazione in sé.
Perché gli effetti variano da persona a persona
Non tutti i pazienti mostrano gli stessi cambiamenti cognitivi dopo la STN‑DBS. La rassegna mette in evidenza diverse ragioni di questa variabilità. L’età e le abilità cognitive di base contano: le persone più anziane e quelle che presentano già problemi cognitivi lievi sono più a rischio di un peggioramento successivo. Anche il punto preciso in cui si trova l’elettrodo nel nucleo subtalamico è cruciale. I contatti più vicini a regioni connesse al linguaggio e all’umore sono più propensi a influenzare la ricerca delle parole e lo stato emotivo. Oltre alla chirurgia e alla stimolazione, caratteristiche intrinseche della malattia — come il sottotipo di Parkinson, i disturbi del sonno, patologie cerebrali sovrapposte, fattori genetici e lo stato generale di salute cerebrale — determinano la vulnerabilità individuale. Depressione, ansia e cambiamenti farmacologici possono ulteriormente complicare il quadro, rendendo essenziali valutazioni pre‑operatorie accurate e un follow‑up attento.
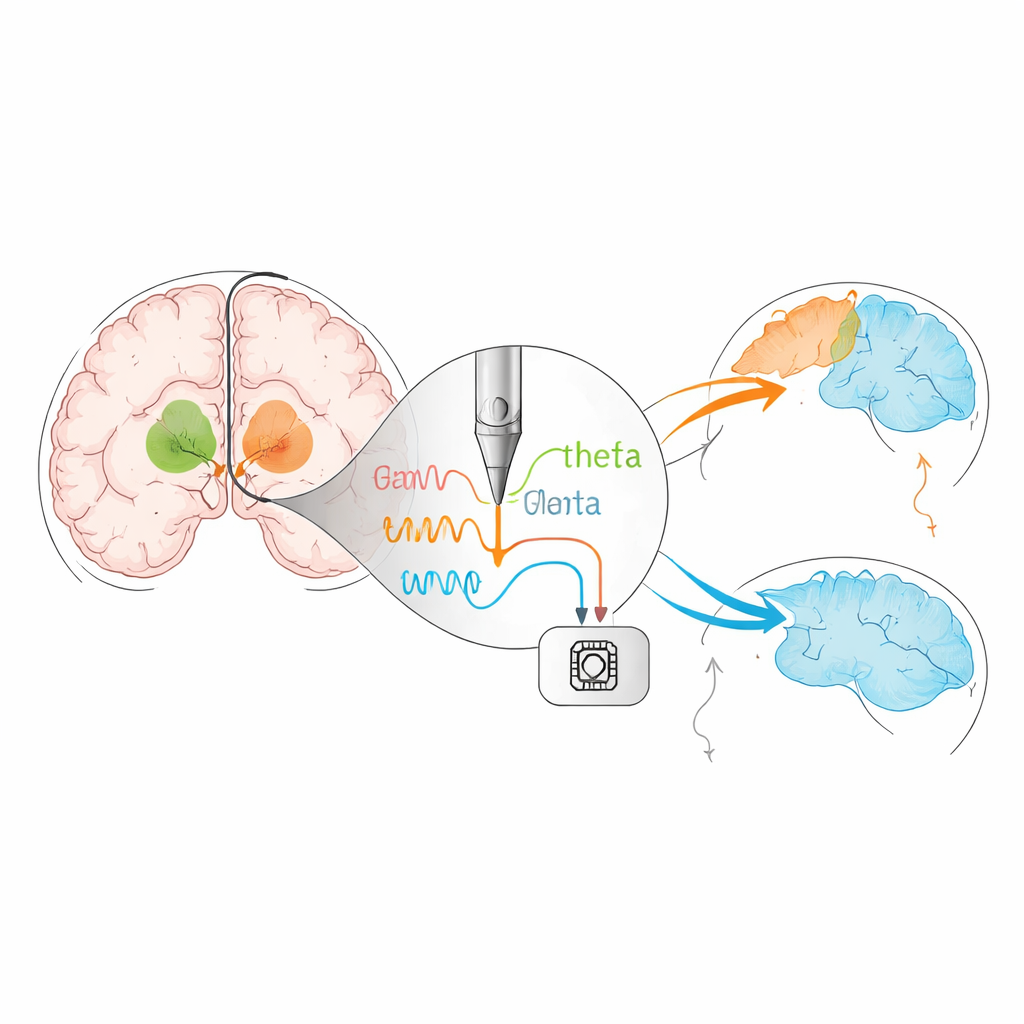
Dalla stimolazione fissa alla stimolazione “intelligente”
La DBS tradizionale eroga impulsi costanti 24 ore su 24, indipendentemente da ciò che la persona sta facendo o da come cambia l’attività cerebrale. La rassegna descrive il passo successivo: la DBS in circuito chiuso, o adattiva. In questo approccio il dispositivo ascolta i ritmi elettrici del cervello e regola la stimolazione in tempo reale. I primi sistemi monitorano l’attività nella banda beta, un ritmo cerebrale associato a rigidità e lentezza, per tarare la stimolazione sul movimento. Lavori più recenti suggeriscono che altri ritmi, come onde più lente nella banda theta, possano riflettere attenzione, autocontrollo o stato di sonno. Stimolazioni temporizzate con attenzione a queste frequenze hanno mostrato in piccoli studi di rendere le decisioni più caute e migliorare la memoria di lavoro senza danneggiare il movimento, suggerendo che dispositivi futuri potrebbero attenuare anche problemi cognitivi e del sonno oltre ai sintomi motori.
Promesse e ostacoli per la protezione della mente
Gli autori concludono che, per la maggior parte delle persone con Parkinson, la STN‑DBS offre benefici motori chiari e duraturi, con cambiamenti cognitivi di solito limitati a abilità specifiche come la generazione rapida di parole. La vera opportunità futura risiede nell’uso di stimolazione più intelligente e guidata dal feedback per bilanciare meglio i guadagni motori con la protezione dell’umore e della cognizione. Per arrivarci, i ricercatori devono identificare segnali cerebrali affidabili che riflettano i sintomi non motori, perfezionare le tecniche di imaging e chirurgia per risparmiare i circuiti sensibili e condurre trial a lungo termine che valutino sia gli esiti motori sia quelli mentali. Se queste sfide verranno superate, i futuri sistemi DBS potrebbero non solo stabilizzare il corpo ma anche contribuire a preservare l’indipendenza, la memoria, il linguaggio e la capacità decisionale nel corso della malattia di Parkinson.
Citazione: Almeida, V., Herz, D.M., Blech, J. et al. Cognitive trajectories in Parkinson’s disease patients, a review on the impact of subthalamic deep brain stimulation (STN-DBS) and emerging adaptive strategies. Transl Psychiatry 16, 233 (2026). https://doi.org/10.1038/s41398-026-04013-6
Parole chiave: malattia di Parkinson, stimolazione cerebrale profonda, cognizione, neuromodulazione in circuito chiuso, nucleo subtalamico