Clear Sky Science · de
Kognitive Verläufe bei Parkinson‑Patienten, eine Übersicht über die Auswirkungen der subthalamischen Tiefenhirnstimulation (STN‑DBS) und aufkommende adaptive Strategien
Warum Hirnstimulation bei Parkinson wichtig ist
Parkinson‑Krankheit ist vor allem für Zittern und verlangsamte Bewegung bekannt, doch viele Betroffene leiden ebenso stark unter Gedächtnislücken, Wortfindungsstörungen und Problemen bei der Konzentration. Um Bewegungsstörungen zu lindern, setzen Ärztinnen und Ärzte zunehmend Tiefenhirnstimulation (DBS) ein, bei der dünne Elektroden tief ins Gehirn implantiert werden. Diese Übersichtsarbeit stellt eine Frage, die Patientinnen, Patienten und ihre Angehörigen häufig bewegt: Was bewirkt diese Behandlung langfristig für Denken und Stimmung, und könnten neue „intelligente“ Formen der DBS dazu beitragen, den Geist ebenso zu schützen wie den Körper?
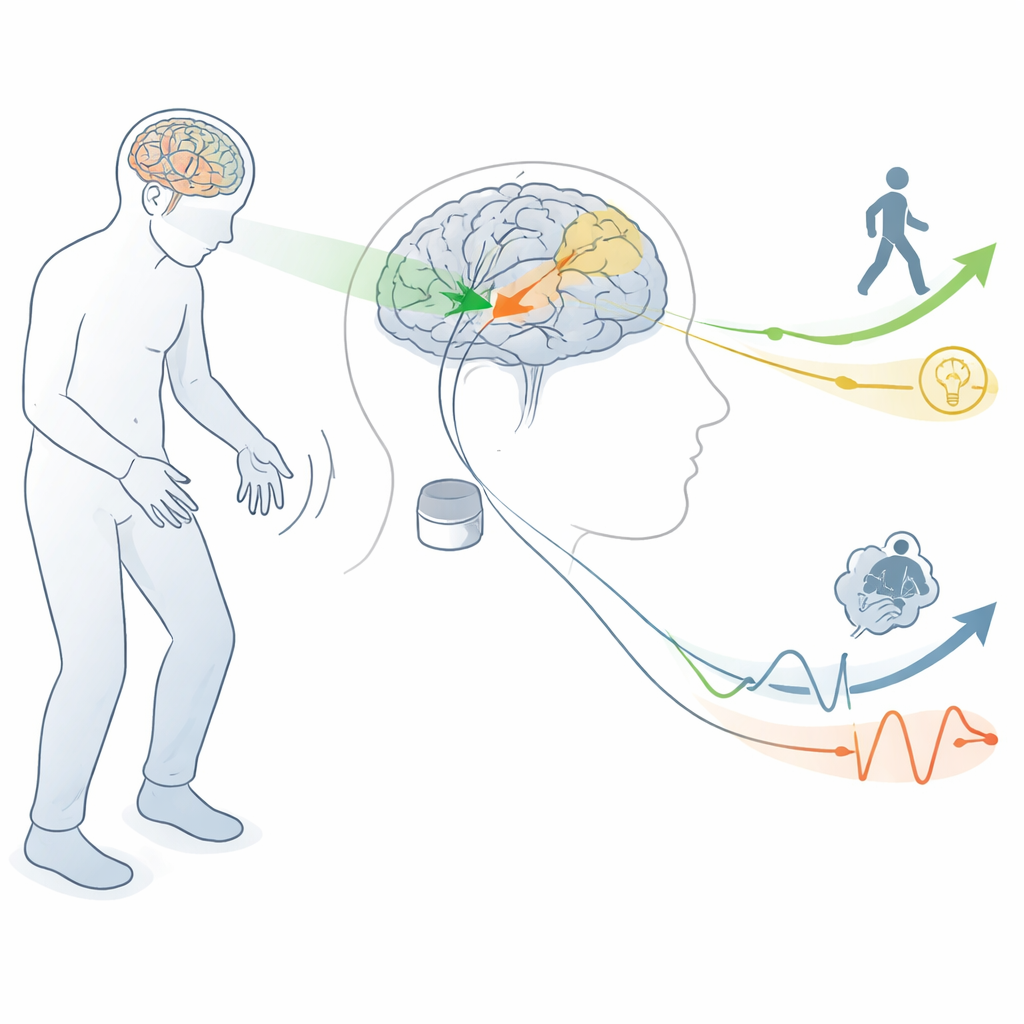
Der Hirnkreis hinter Bewegung und Denken
Die Autorinnen und Autoren beginnen mit der Erklärung, wie Parkinson Hirnnetzwerke stört, die uns normalerweise beim Einleiten und Kontrollieren von Bewegungen helfen. Eine kleine Region, der subthalamische Nukleus, tief im Gehirn gelegen, wird überaktiv, wenn der Botenstoff Dopamin verloren geht. Hochfrequente DBS dieses Bereichs (STN‑DBS) kann die abnorme Aktivität dämpfen und Tremor, Steifheit und unerwünschte Bewegungen deutlich verbessern. Derselbe Bereich ist jedoch auch mit Hirnregionen verbunden, die Sprache, Planung, Emotion und Motivation unterstützen. Diese Überlappung bedeutet, dass die Stimulation zur Verbesserung der Motorik auch Schaltkreise beeinflussen kann, die bei Denken und Fühlen eine Rolle spielen.
Was nach DBS mit dem Denken passiert
Aus randomisierten Studien, Langzeitnachbeobachtungen und Metaanalysen ergibt die Übersichtsarbeit ein klares Bild. Allgemeine Intelligenz und Alltagskognition bleiben meist erhalten, und viele Patientinnen und Patienten berichten nach der Operation von einer emotionalen Verbesserung. Wiederholt zeigt sich jedoch eine spezifische Schwäche: Schwierigkeiten, schnell die passenden Wörter zu finden — getestet etwa durch Aufgaben, in denen so viele Begriffe wie möglich aus einer Kategorie genannt werden sollen. Einige Studien berichten außerdem über leichte Veränderungen in Planung, mentaler Flexibilität und Gedächtnis über mehrere Jahre. Diese Effekte sind typischerweise moderat, und viele Betroffene berichten weiterhin von einer besseren Lebensqualität, weil Motorik und Stimmung sich gebessert haben. Wichtig ist: Langzeitdaten deuten darauf hin, dass breitere kognitive Verschlechterungen größtenteils den natürlichen Verlauf der Parkinson‑Krankheit widerspiegeln und nicht primär der Stimulation zuzuschreiben sind.
Warum die Effekte von Person zu Person variieren
Nicht alle Patientinnen und Patienten zeigen nach STN‑DBS dieselben kognitiven Veränderungen. Die Übersichtsarbeit hebt mehrere Gründe für diese Variabilität hervor. Alter und Ausgangsleistung in kognitiven Tests spielen eine Rolle: Ältere Menschen und solche mit bereits leichten kognitiven Beeinträchtigungen neigen eher zu späteren Verschlechterungen. Entscheidend ist auch die genaue Lage der Elektrode im subthalamischen Nukleus: Kontakte, die näher an Regionen liegen, die mit Sprache und Stimmung verknüpft sind, beeinflussen eher Wortfindung und emotionale Befindlichkeit. Neben Operation und Stimulation formen Merkmale der Erkrankung selbst — etwa der Parkinson‑Subtyp, Schlafstörungen, überlappende Gehirnpathologien, genetische Faktoren und die allgemeine Hirngesundheit — die Anfälligkeit. Depression, Angst und Medikamentenänderungen können das Bild zusätzlich verkomplizieren, weshalb sorgfältige präoperative Beurteilung und Nachsorge unerlässlich sind.
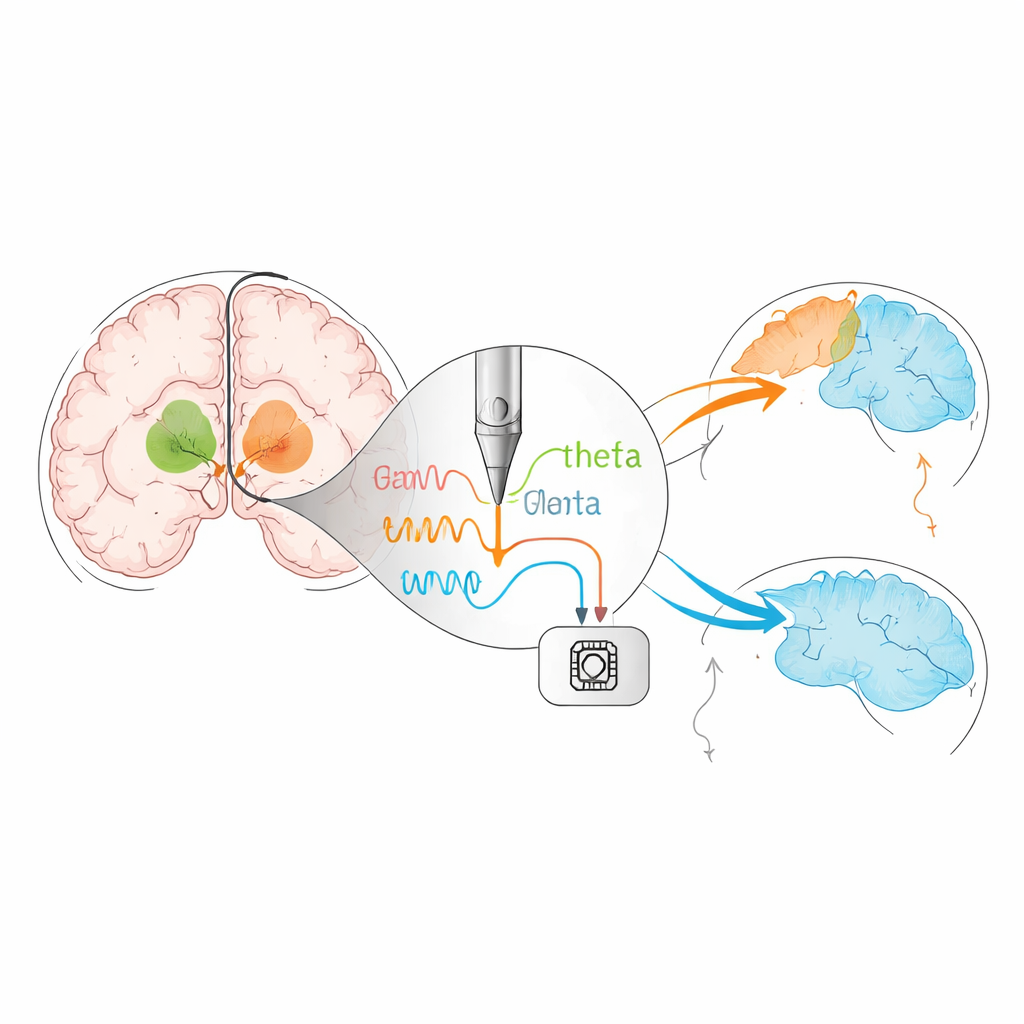
Von fester zu „intelligenter“ Stimulation
Traditionelle DBS liefert rund um die Uhr gleichmäßige Impulse, unabhängig davon, was die Person gerade tut oder wie sich ihre Hirnaktivität verändert. Die Übersichtsarbeit beschreibt einen nächsten Schritt: Closed‑Loop‑ bzw. adaptive DBS. Bei diesem Ansatz hört das Gerät die elektrischen Rhythmen des Gehirns und passt die Stimulation in Echtzeit an. Erste Systeme verfolgen Beta‑Band‑Aktivität, eine Hirnfrequenz, die mit Steifheit und Verlangsamung verknüpft ist, um die Stimulation für die Motorik zu optimieren. Neuere Arbeiten deuten darauf hin, dass andere Rhythmen, etwa langsamere Theta‑Wellen, Aufmerksamkeit, Selbstkontrolle oder Schlafzustand widerspiegeln können. Zeitlich genau getimte Stimulation in diesen Frequenzen hat in kleinen Studien gezeigt, dass Entscheidungen vorsichtiger werden und das Arbeitsgedächtnis sich verbessern kann, ohne die Motorik zu beeinträchtigen — ein Hinweis darauf, dass künftige Geräte kognitive und Schlafprobleme ebenso wie motorische Symptome lindern könnten.
Versprechen und Hürden zum Schutz des Geistes
Die Autorinnen und Autoren schließen, dass STN‑DBS den meisten Menschen mit Parkinson klare und anhaltende motorische Vorteile bringt, während kognitive Veränderungen meist auf spezifische Fähigkeiten wie schnelles Wortabrufen beschränkt sind. Die wirkliche Chance liegt darin, durch intelligentere, rückkopplungsgesteuerte Stimulation motorische Verbesserungen besser mit dem Schutz von Stimmung und Kognition auszubalancieren. Dafür müssen Forschende zuverlässige Hirnsignale identifizieren, die nichtmotorische Symptome abbilden, Bildgebungs‑ und Operationstechniken verfeinern, um empfindliche Schaltkreise zu schonen, und langfristige Studien durchführen, die sowohl Bewegungs‑ als auch mentale Ergebnisse verfolgen. Können diese Herausforderungen gemeistert werden, könnten künftige DBS‑Systeme nicht nur den Körper stabilisieren, sondern auch dazu beitragen, Unabhängigkeit, Gedächtnis, Sprache und Entscheidungsfähigkeit im Verlauf der Parkinson‑Krankheit zu erhalten.
Zitation: Almeida, V., Herz, D.M., Blech, J. et al. Cognitive trajectories in Parkinson’s disease patients, a review on the impact of subthalamic deep brain stimulation (STN-DBS) and emerging adaptive strategies. Transl Psychiatry 16, 233 (2026). https://doi.org/10.1038/s41398-026-04013-6
Schlüsselwörter: Parkinson‑Krankheit, Tiefenhirnstimulation, Kognition, Closed‑Loop‑Neuromodulation, subthalamischer Nukleus