Clear Sky Science · ru
Открытие терапевтических нуклеозидных гидрогелей с помощью машинного обучения для лечения пародонтита
Почему «умные» гели важны при болезнях десен
Заболевания десен — одна из самых распространенных проблем со здоровьем в мире, однако нынешние методы лечения часто испытывают трудности с доставкой лекарств точно в нужное место и удержанием их там достаточное время для действия. В этом исследовании описано, как ученые использовали инструменты машинного обучения, чтобы спроектировать крошечные, похожие на лекарства строительные блоки, способные собираться в мягкие гели. Эти гели помещают вокруг зубов, чтобы бороться с вредными ротовыми бактериями и защищать кость, которая удерживает зубы.
От случайных испытаний к направленной разработке
Мягкие водосодержащие гели из малых молекул давно рассматриваются как перспективные материалы для доставки лекарств и восстановления тканей. В частности, гели, построенные из нуклеозидов — той же семьи молекул, что формируют ДНК и РНК — привлекательны тем, что хорошо сочетаются с живыми тканями и могут восстанавливать незначительные повреждения своей структуры. До сих пор полезные варианты таких гелей часто находили случайно или путём медленного изменения химических групп, что было медленным и неопределенным процессом. Авторы поставили цель заменить большую часть этого метода проб и ошибок более систематическим подходом, который предсказывает, какие нуклеозиды могут формировать гели и как они будут вести себя в организме.
Обучение компьютеров распознавать полезные молекулы
Команда собрала большие публичные наборы данных, описывающие, как тысячи малых молекул ведут себя в биологических тестах, включая токсичность, антимикробную активность, противовирусное действие, противовоспалительные эффекты и активность против опухолевых клеток. Для каждой молекулы они вычислили тысячи числовых признаков, кодирующих аспекты её структуры. С использованием нескольких типов моделей машинного обучения они обучали компьютеры связывать эти структурные признаки с девятью разными биологическими активностями. Чтобы избежать переобучения и улучшить точность, они тщательно фильтровали и отбирали наиболее информативные признаки перед построением моделей.
Баланс безопасности, прочности и антимикробной силы
Проектирование геля для лечения десен требует не только уничтожения микробов. Материал должен быть безопасен для клеток человека и уметь формировать стабильный, вводимый шприцем гель, который может оставаться в пародонтальном кармане. Чтобы увязать эти требования, исследователи ввели два новых инструмента оценки. Индекс специфичности молекулярной биологической активности (Molecular Bioactivity Specificity Index) выделяет, в какой одной конкретной активности молекула особенно хороша — например, нацеливание на ключевую бактерию пародонтита при слабой активности в других областях. Композитный балл молекулярных свойств (Composite Molecular Attribute Score) взвешивает несколько свойств одновременно, ранжируя молекулы, которые лучше всего сочетают способность к формированию геля, низкую токсичность и высокую антимикробную потенцию.
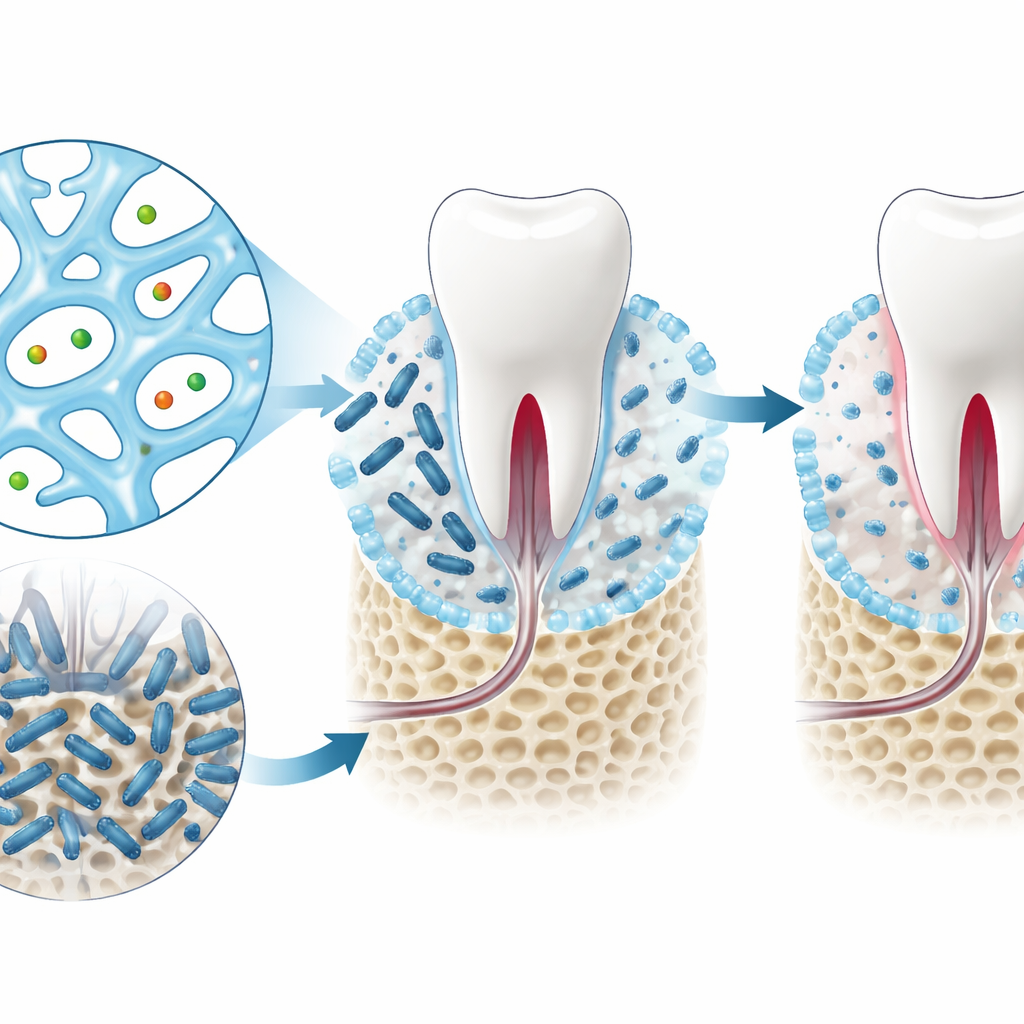
От компьютерных хитов к рабочим гидрогелям
Используя свои модели и систему оценок, авторы просcreenировали более семи тысяч нуклеозидных кандидатов и сократили список до четырех соединений, которые реально можно синтезировать в лаборатории. Среди них два родственных соединения, известные как GMP и dGMP, выделились при тестировании. В смеси с ионами серебра они образовывали мягкие пористые гели с хорошей механической прочностью и способностью восстанавливать свою структуру после нарушения. В лабораторных чашках как свободные молекулы, так и их гелеобразные формы значительно подавляли рост Porphyromonas gingivalis — ключевой бактерии, связанной с пародонтитом — при этом оставались щадящими для клеток млекопитающих.
Испытания защиты десен в живых животных
Далее исследователи протестировали гели на мышиных моделях пародонтита. В одном наборе экспериментов они лечили уже установленный пародонтит, вводя гели в пародонтальные карманы после инфекции P. gingivalis. В другом — применяли гели вскоре после инфекции, чтобы проверить, смогут ли они предотвратить развитие повреждений. В обоих случаях сканирование челюстной кости показало, что у обработанных мышей было меньше потерь поддерживающей кости вокруг зубов и сохранялась более плотная, здоровая костная структура. Срезы тканей десен показали уменьшение признаков воспаления и повышенные уровни маркеров, связанных с заживлением и восстановлением тканей. Важно, что проверки основных органов и мест инъекций не выявили явного повреждения тканей или продолжающегося воспаления.
Что это значит для будущего ухода за полостью рта
Для непрофессионального читателя ключевое сообщение состоит в том, что команда создала более умный способ проектирования мягких гелей, несущих лекарства для ротовой полости, позволяя компьютерам учиться на больших химических и биологических наборах данных. Их подход указал на два нуклеозидных геля, которые безопасно борются с важной бактерией пародонтита и помогают сохранять кость вокруг зубов у мышей. Хотя прежде чем эти материалы попадут в клинику потребуется ещё много работы, исследование показывает, что разработка под руководством машинного обучения может ускорить создание целевых терапий для заболеваний десен и, возможно, других оральных состояний.
Цитирование: Li, W., Wen, Y., Huang, Z. et al. Machine learning-driven discovery of therapeutic nucleoside hydrogels for periodontitis. Int J Oral Sci 18, 41 (2026). https://doi.org/10.1038/s41368-026-00438-3
Ключевые слова: машинное обучение, пародонтит, гидрогели, оральный микробиом, биоматериалы