Clear Sky Science · fr
Découverte assistée par apprentissage automatique d'hydrogels thérapeutiques à base de nucléosides pour la parodontite
Pourquoi des gels « intelligents » pour les gencives sensibles comptent
La maladie des gencives est l’un des problèmes de santé les plus répandus dans le monde, pourtant les traitements actuels peinent souvent à délivrer le médicament exactement là où il faut et à le maintenir suffisamment longtemps pour être efficace. Cette étude décrit comment des chercheurs ont utilisé des outils d’apprentissage informatique pour concevoir de petits blocs de construction aux propriétés médicamenteuses capables de s’assembler en gels mous. Ces gels sont placés autour des dents pour combattre les bactéries buccales nuisibles et protéger l’os qui soutient les dents.
Du tâtonnement aléatoire à la conception guidée
Les gels hydratés à base de petites molécules sont depuis longtemps perçus comme des matériaux prometteurs pour l’administration de médicaments et la réparation tissulaire. En particulier, les gels à base de nucléosides, la même famille de molécules qui compose l’ADN et l’ARN, sont attractifs car ils s’intègrent bien aux tissus vivants et peuvent réparer de légères altérations de leur structure. Jusqu’à présent, les versions utiles de ces gels étaient souvent découvertes par hasard ou par modification lente de groupes chimiques, un processus long et incertain. Les auteurs ont cherché à remplacer une grande partie de ce tâtonnement par une voie plus systématique capable de prédire quelles molécules de nucléosides peuvent former des gels et comment elles se comporteraient dans l’organisme.
Apprendre aux ordinateurs à repérer les molécules utiles
L’équipe a rassemblé de vastes jeux de données publics décrivant le comportement de milliers de petites molécules dans des tests biologiques, incluant la toxicité, l’activité antibactérienne, l’action antivirale, les effets anti-inflammatoires et l’activité contre des cellules tumorales. Pour chaque molécule, ils ont calculé des milliers de descripteurs numériques qui codent des aspects de sa structure. En utilisant plusieurs types de modèles d’apprentissage automatique, ils ont entraîné des ordinateurs à relier ces caractéristiques structurales à neuf activités biologiques différentes. Pour éviter le surapprentissage et améliorer la précision, ils ont soigneusement filtré et sélectionné les descripteurs les plus informatifs avant de construire les modèles.
Équilibrer sécurité, solidité et pouvoir antibactérien
Concevoir un gel pour la maladie des gencives exige plus que l’élimination des germes. Le matériau doit être sûr pour les cellules humaines et capable de former un gel stable et injectable qui puisse rester dans la poche gingivale. Pour concilier ces exigences, les chercheurs ont introduit deux nouveaux outils de notation. L’Indice de Spécificité de la Bioactivité Moléculaire met en évidence l’activité unique pour laquelle une molécule est particulièrement performante, par exemple cibler une bactérie clé de la parodontite tout en restant inactive sur d’autres fronts. Le Score Composé d’Attributs Moléculaires pèse plusieurs propriétés simultanément, classant les molécules qui combinent le mieux formation de gel robuste, faible toxicité et fort potentiel antibactérien.
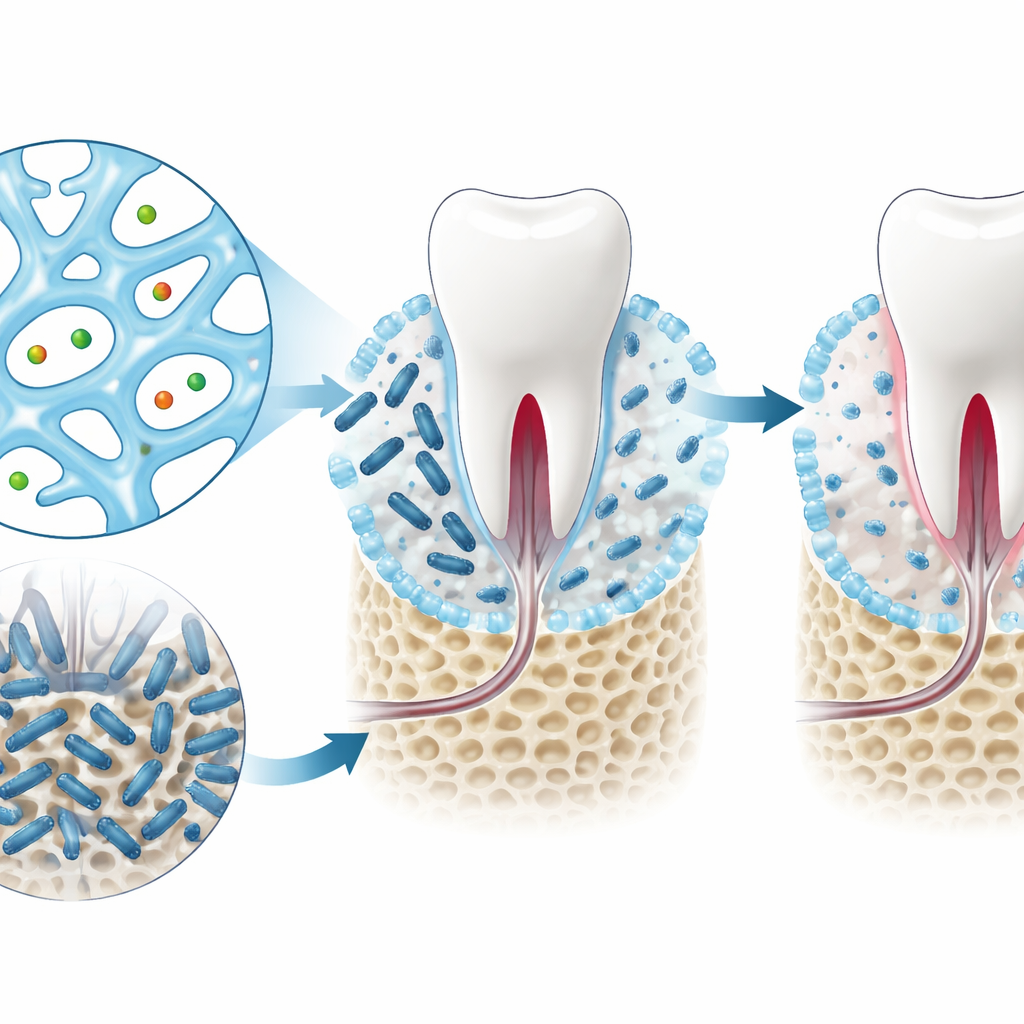
Des « hits » informatiques aux hydrogels fonctionnels
À l’aide de leurs modèles et de leur système de notation, les auteurs ont dépisté plus de sept mille candidats à base de nucléosides et réduit la liste à quatre composés réalisables en laboratoire. Parmi eux, deux composés apparentés, connus sous les noms de GMP et dGMP, se sont distingués après tests. Mélangés avec des ions argent, ils ont formé des gels mous et poreux présentant une bonne résistance mécanique et la capacité de récupérer leur structure après perturbation. En cultures cellulaires, aussi bien les molécules libres que leurs formes en gel ont fortement réduit la croissance de Porphyromonas gingivalis, une bactérie majeure associée à la parodontite, tout en restant compatibles avec des cellules de mammifères.
Tester la protection des gencives chez des animaux vivants
Les chercheurs ont ensuite testé les gels dans des modèles murins de maladie des gencives. Dans une série d’expériences, ils ont traité une parodontite établie en injectant les gels dans les poches gingivales après infection par P. gingivalis. Dans une autre, ils ont utilisé les gels peu après l’infection pour voir s’ils pouvaient prévenir l’apparition des lésions. Dans les deux cas, les scans de l’os mandibulaire ont montré que les souris traitées perdaient moins d’os de soutien autour de leurs dents et maintenaient une structure osseuse plus dense et plus saine. Les coupes tissulaires des gencives ont révélé une réduction des signes d’inflammation et des niveaux plus élevés de marqueurs associés à la cicatrisation et à la réparation tissulaire. Fait important, les contrôles des organes majeurs et des sites d’injection n’ont montré aucun dommage tissulaire évident ni inflammation persistante.
Ce que cela signifie pour les soins buccaux futurs
Pour un lecteur non spécialiste, le message principal est que l’équipe a mis au point une méthode plus intelligente pour concevoir des gels mous transportant des médicaments pour la bouche en laissant les ordinateurs apprendre à partir de larges jeux de données chimiques et biologiques. Leur approche a permis d’identifier deux gels à base de nucléosides capables de combattre en toute sécurité une bactérie majeure de la parodontite et d’aider à préserver l’os autour des dents chez la souris. Bien que des travaux supplémentaires soient nécessaires avant que ces matériaux n’atteignent la clinique, l’étude suggère que la conception guidée par apprentissage automatique pourrait accélérer le développement de traitements ciblés pour la maladie des gencives et peut‑être d’autres affections buccales.
Citation: Li, W., Wen, Y., Huang, Z. et al. Machine learning-driven discovery of therapeutic nucleoside hydrogels for periodontitis. Int J Oral Sci 18, 41 (2026). https://doi.org/10.1038/s41368-026-00438-3
Mots-clés: apprentissage automatique, parodontite, hydrogels, microbiote buccal, biomatériaux