Clear Sky Science · pl
Odkrycie terapeutycznych hydrożeli nukleozydowych napędzane przez uczenie maszynowe w leczeniu zapalenia przyzębia
Dlaczego inteligentne żele na bolące dziąsła mają znaczenie
Choroby dziąseł należą do najpowszechniejszych problemów zdrowotnych na świecie, a jednocześnie dostępne terapie często mają trudności, by dostarczyć lek dokładnie tam, gdzie jest potrzebny, i utrzymać go wystarczająco długo, aby zadziałał. W tym badaniu opisano, jak badacze wykorzystali narzędzia komputerowego uczenia się do zaprojektowania malutkich, przypominających leki bloków budulcowych, które mogą samoistnie składać się w miękkie żele. Te żele umieszcza się wokół zębów, aby zwalczać szkodliwe bakterie jamy ustnej i chronić kość utrzymującą zęby.
Od losowych prób do projektowania z przewodnikiem
Miękkie, wodniste żele z małych cząsteczek od dawna postrzegane są jako obiecujące materiały do dostarczania leków i naprawy tkanek. W szczególności żele zbudowane z nukleozydów, tej samej rodziny cząsteczek, które tworzą DNA i RNA, są atrakcyjne, ponieważ dobrze współgrają z tkankami żywymi i mogą naprawiać drobne uszkodzenia swojej struktury. Do tej pory użyteczne wersje tych żeli często znajdowano przypadkiem lub przez powolne modyfikowanie grup chemicznych — proces wolny i niepewny. Autorzy postanowili zastąpić dużą część tego zgadywania bardziej systematyczną ścieżką, która przewiduje, które nukleozydy mogą tworzyć żele i jak mogą się zachowywać w organizmie.
Nauczanie komputerów rozpoznawania użytecznych cząsteczek
Zespół zgromadził obszerne publiczne zbiory danych opisujące zachowanie tysięcy małych cząsteczek w testach biologicznych, obejmujące toksyczność, działanie przeciwbakteryjne, przeciwwirusowe, przeciwzapalne oraz aktywność wobec komórek nowotworowych. Dla każdej cząsteczki obliczono tysiące cech numerycznych kodujących aspekty jej struktury. Korzystając z kilku typów modeli uczenia maszynowego, wyszkolono komputery do łączenia tych cech strukturalnych z dziewięcioma różnymi aktywnościami biologicznymi. Aby uniknąć przeuczenia i poprawić dokładność, starannie przefiltrowano i wybrano najbardziej informacyjne cechy przed zbudowaniem modeli.
Równoważenie bezpieczeństwa, wytrzymałości i mocy antybakteryjnej
Projektowanie żelu na choroby dziąseł to coś więcej niż zabijanie zarazków. Materiał musi być bezpieczny dla komórek ludzkich i zdolny do utworzenia stabilnego, wstrzykiwalnego żelu, który utrzyma się w kieszeni dziąsłowej. Aby pogodzić te wymagania, badacze wprowadzili dwa nowe narzędzia ocen. Wskaźnik Specyficzności Bioaktywności Molekularnej podkreśla, w której pojedynczej aktywności cząsteczka jest szczególnie dobra, na przykład celowanie w kluczowego bakteryjnego sprawcę choroby przy minimalnym działaniu na inne fronty. Złożony Wskaźnik Atrybutów Molekularnych waży jednocześnie kilka właściwości, klasyfikując cząsteczki, które najlepiej łączą silne tworzenie żelu, niską toksyczność i wysokie potencjały antybakteryjne.
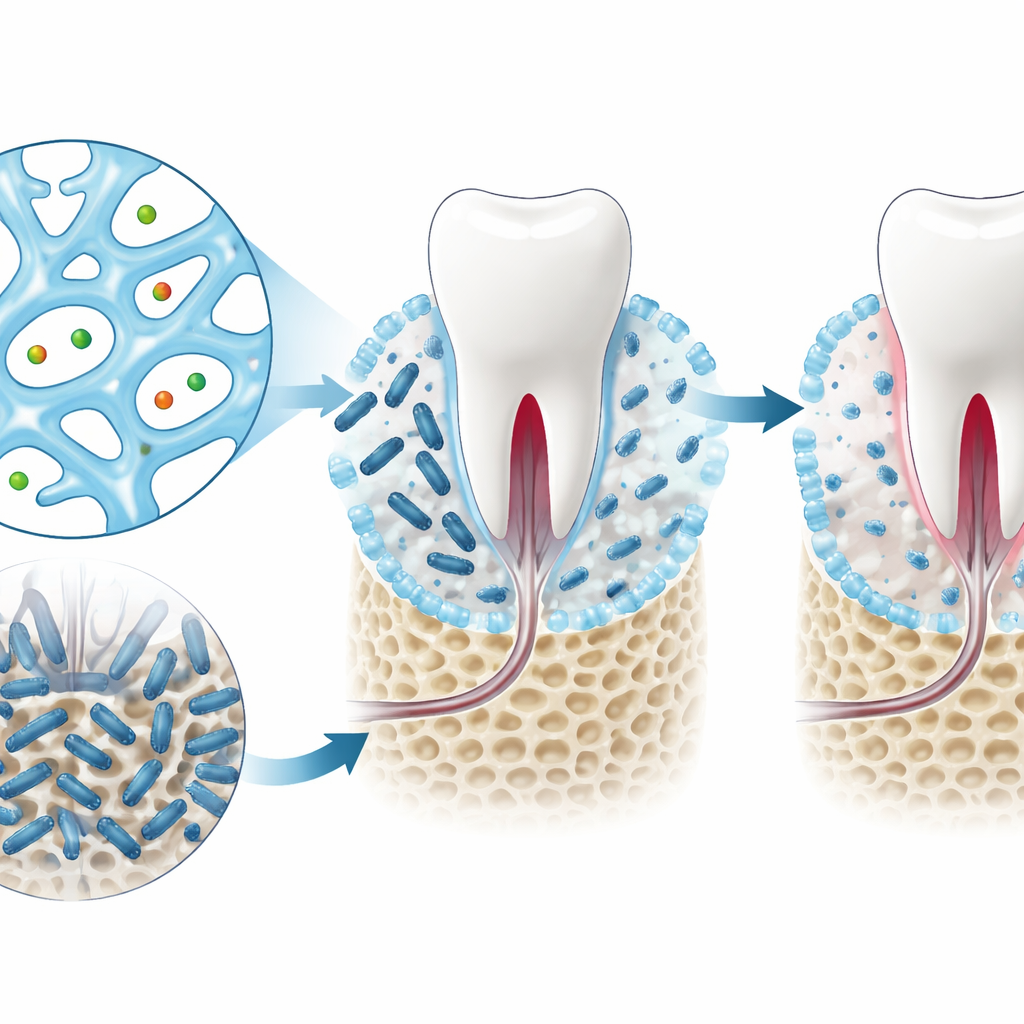
Od komputerowych trafień do działających hydrożeli
Używając swoich modeli i systemu punktowania, autorzy przeskanowali ponad siedem tysięcy kandydatów opartych na nukleozydach i zawęzili listę do czterech, które można realistycznie wytworzyć w laboratorium. Wśród nich dwie spokrewnione związki, znane jako GMP i dGMP, wyróżniły się po testach. W zmieszaniu z jonami srebra utworzyły miękkie, porowate żele o dobrej wytrzymałości mechanicznej i zdolności do odzyskiwania struktury po zakłóceniu. W hodowlach laboratoryjnych zarówno wolne cząsteczki, jak i ich żelowe formy znacząco zmniejszały wzrost Porphyromonas gingivalis, głównej bakterii powiązanej z zapaleniem przyzębia, pozostając jednocześnie łagodnymi dla komórek ssaków.
Testowanie ochrony dziąseł na żywych zwierzętach
Następnie badacze przetestowali żele w modelach mysich chorób dziąseł. W jednym zestawie eksperymentów leczyli ustalone zapalenie przyzębia przez wstrzykiwanie żeli do kieszonek dziąsłowych po zakażeniu P. gingivalis. W innym stosowali żele wkrótce po zakażeniu, aby sprawdzić, czy można zapobiec rozwojowi uszkodzeń. W obu przypadkach skany kości szczęki wykazały, że myszy leczone traciły mniej kości wspierającej zęby i zachowywały gęstszą, zdrowszą strukturę kostną. Plastry tkanek z dziąseł ujawniły zmniejszone objawy zapalenia i wyższe poziomy markerów związanych z gojeniem i naprawą tkanek. Co ważne, kontrole głównych narządów i miejsc wstrzyknięć nie wykazały wyraźnych uszkodzeń tkanek ani utrzymującego się stanu zapalnego.
Co to oznacza dla przyszłej opieki jamy ustnej
Dla czytelnika niebędącego specjalistą kluczowy przekaz jest taki, że zespół stworzył inteligentniejszy sposób projektowania miękkich, nośnikowych żeli do jamy ustnej, pozwalając komputerom uczyć się na podstawie dużych zbiorów danych chemicznych i biologicznych. Ich podejście wskazało dwa hydrożele oparte na nukleozydach, które mogą bezpiecznie zwalczać główną bakterię wywołującą chorobę dziąseł i pomagać zachować kość wokół zębów u myszy. Choć przed wprowadzeniem tych materiałów do klinik potrzebne są dalsze prace, badanie sugeruje, że projektowanie wspomagane uczeniem maszynowym może przyspieszyć rozwój ukierunkowanych terapii na choroby dziąseł, a być może także innych schorzeń jamy ustnej.
Cytowanie: Li, W., Wen, Y., Huang, Z. et al. Machine learning-driven discovery of therapeutic nucleoside hydrogels for periodontitis. Int J Oral Sci 18, 41 (2026). https://doi.org/10.1038/s41368-026-00438-3
Słowa kluczowe: uczenie maszynowe, zapalenie przyzębia, hydrożele, mikrobiom jamy ustnej, biomateriały