Clear Sky Science · es
Descubrimiento impulsado por aprendizaje automático de hidrogeles terapéuticos de nucleósidos para la periodontitis
Por qué importan los geles inteligentes para las encías inflamadas
La enfermedad de las encías es uno de los problemas de salud más comunes en todo el mundo, pero los tratamientos actuales a menudo tienen dificultades para llevar el medicamento exactamente donde hace falta y mantenerlo el tiempo suficiente para que funcione. Este estudio describe cómo los investigadores emplearon herramientas de aprendizaje por ordenador para diseñar diminutos bloques constructores similares a fármacos que pueden ensamblarse en geles blandos. Estos geles se colocan alrededor de los dientes para combatir bacterias nocivas de la boca y proteger el hueso que sostiene los dientes.
De la prueba aleatoria al diseño guiado
Los geles blandos ricos en agua hechos a partir de pequeñas moléculas han sido vistos durante mucho tiempo como materiales prometedores para la liberación de fármacos y la reparación de tejidos. En particular, los geles formados por nucleósidos, la misma familia de moléculas que forman el ADN y el ARN, resultan atractivos porque se integran bien con el tejido vivo y pueden reparar daños menores en su estructura. Hasta ahora, las versiones útiles de estos geles se hallaban con frecuencia por casualidad o mediante ajustes lentos de grupos químicos, un proceso lento e incierto. Los autores se propusieron reemplazar gran parte de esta conjetura por una ruta más sistemática que prediga qué moléculas de nucleósidos pueden formar geles y cómo podrían comportarse en el cuerpo.
Enseñar a las computadoras a detectar moléculas útiles
El equipo reunió grandes conjuntos de datos públicos que describen cómo se comportan miles de pequeñas moléculas en pruebas biológicas, incluidas toxicidad, poder antibacteriano, acción antiviral, efectos antiinflamatorios y actividad frente a células tumorales. Para cada molécula calcularon miles de características numéricas que codifican aspectos de su estructura. Usando varios tipos de modelos de aprendizaje automático, entrenaron a las computadoras para vincular esas características estructurales con nueve actividades biológicas diferentes. Para evitar el sobreajuste y mejorar la precisión, filtraron y seleccionaron cuidadosamente las características más informativas antes de construir los modelos.
Equilibrar seguridad, resistencia y poder antibacteriano
Diseñar un gel para la enfermedad de las encías requiere más que matar gérmenes. El material debe ser seguro para las células humanas y capaz de formar un gel estable e inyectable que pueda permanecer en el bolsillo gingival. Para compaginar estas necesidades, los investigadores introdujeron dos nuevas herramientas de puntuación. El Índice de Especificidad de Bioactividad Molecular resalta en qué actividad individual destaca una molécula, por ejemplo, dirigirse a una bacteria clave de la enfermedad de las encías mientras permanece inactiva en otros frentes. La Puntuación Compuesta de Atributos Moleculares pondera varias propiedades a la vez, clasificando las moléculas que mejor combinan formación de gel sólida, baja toxicidad y alto potencial antibacteriano.
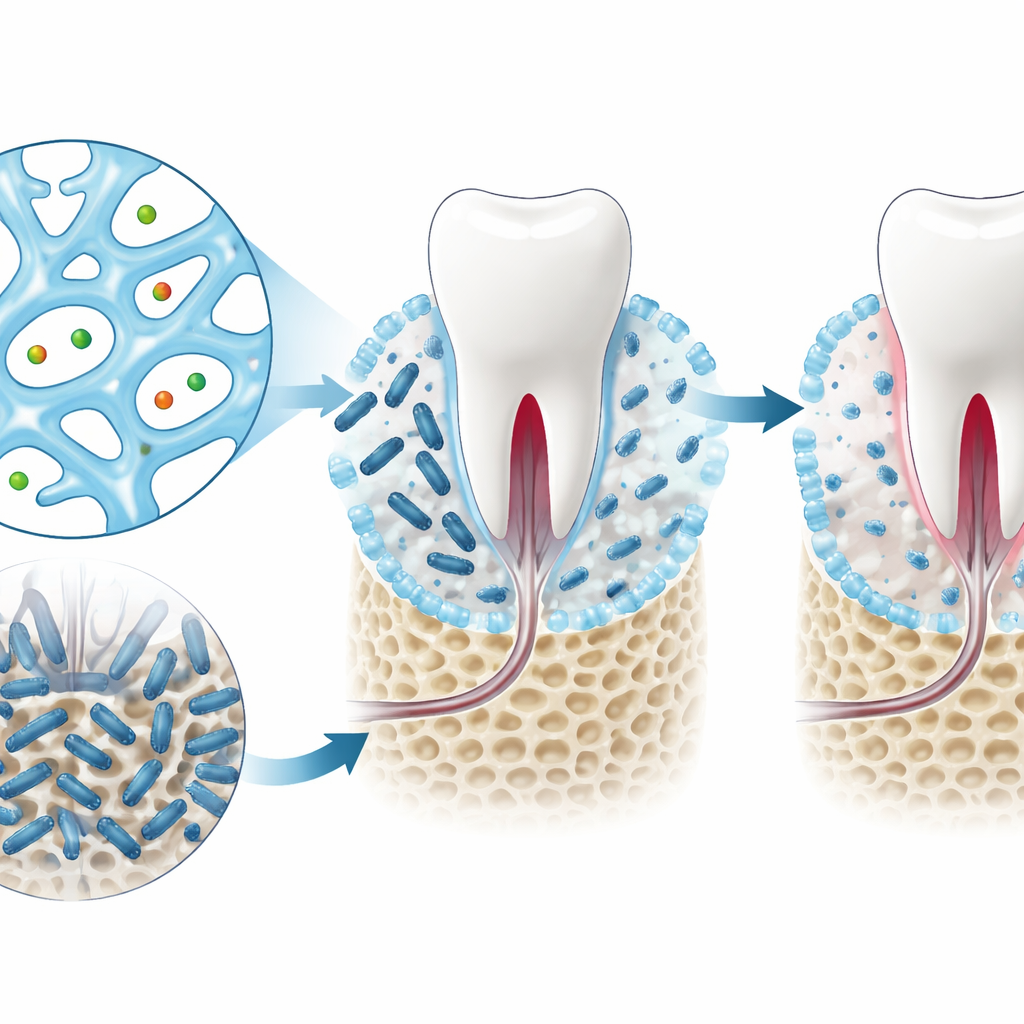
De los aciertos informáticos a hidrogeles funcionales
Usando sus modelos y sistema de puntuación, los autores examinaron más de siete mil candidatos basados en nucleósidos y redujeron la lista a cuatro que podían fabricarse de forma realista en el laboratorio. Entre estos, dos compuestos relacionados, conocidos como GMP y dGMP, destacaron una vez probados. Mezclados con iones de plata, formaron geles blandos y porosos con buena resistencia mecánica y la capacidad de recuperar su estructura tras ser perturbados. En placas de laboratorio, tanto las moléculas libres como sus versiones en gel redujeron drásticamente el crecimiento de Porphyromonas gingivalis, una bacteria importante vinculada a la periodontitis, mientras resultaban suaves para las células de mamíferos.
Probar la protección de las encías en animales vivos
Los investigadores probaron a continuación los geles en modelos de ratón de enfermedad de las encías. En un conjunto de experimentos trataron la periodontitis establecida inyectando los geles en los bolsillos gingivales tras la infección con P. gingivalis. En otro, usaron los geles poco después de la infección para ver si podían prevenir el desarrollo del daño. En ambos casos, las exploraciones del hueso mandibular mostraron que los ratones tratados perdieron menos hueso de soporte alrededor de sus dientes y mantuvieron una estructura ósea más densa y saludable. Los cortes de tejido de las encías revelaron signos reducidos de inflamación y niveles más altos de marcadores asociados a la curación y la reparación tisular. Es importante que las comprobaciones de los principales órganos y de los puntos de inyección no mostraron daños tisulares evidentes ni inflamación persistente.
Qué significa esto para el cuidado bucal futuro
Para un lector general, el mensaje clave es que el equipo construyó una forma más inteligente de diseñar geles blandos portadores de medicamento para la boca permitiendo que las computadoras aprendan de grandes conjuntos de datos químicos y biológicos. Su enfoque identificó dos geles basados en nucleósidos que pueden combatir de forma segura una bacteria importante de la enfermedad de las encías y ayudar a preservar el hueso alrededor de los dientes en ratones. Aunque se necesita más trabajo antes de que estos materiales lleguen a la clínica, el estudio sugiere que el diseño guiado por aprendizaje automático podría acelerar el desarrollo de tratamientos dirigidos para la enfermedad de las encías y, quizás, otras afecciones orales.
Cita: Li, W., Wen, Y., Huang, Z. et al. Machine learning-driven discovery of therapeutic nucleoside hydrogels for periodontitis. Int J Oral Sci 18, 41 (2026). https://doi.org/10.1038/s41368-026-00438-3
Palabras clave: aprendizaje automático, periodontitis, hidrogeles, microbioma oral, biomateriales