Clear Sky Science · de
Maschinelles Lernen gesteuerte Entdeckung therapeutischer Nukleosid-Hydrogele bei Parodontitis
Warum clevere Gele bei entzündetem Zahnfleisch wichtig sind
Zahnfleischerkrankungen gehören zu den häufigsten Gesundheitsproblemen weltweit, doch aktuelle Behandlungen schaffen es oft nicht, Medikamente genau dorthin zu bringen, wo sie gebraucht werden, und lange genug zu halten, um wirksam zu sein. Diese Studie beschreibt, wie Forschende Computerlernwerkzeuge einsetzten, um winzige, medikamentenähnliche Bausteine zu entwerfen, die sich zu weichen Gelen zusammenlagern können. Diese Gele werden um Zähne platziert, um schädliche Mundbakterien zu bekämpfen und den Knochen zu schützen, der die Zähne hält.
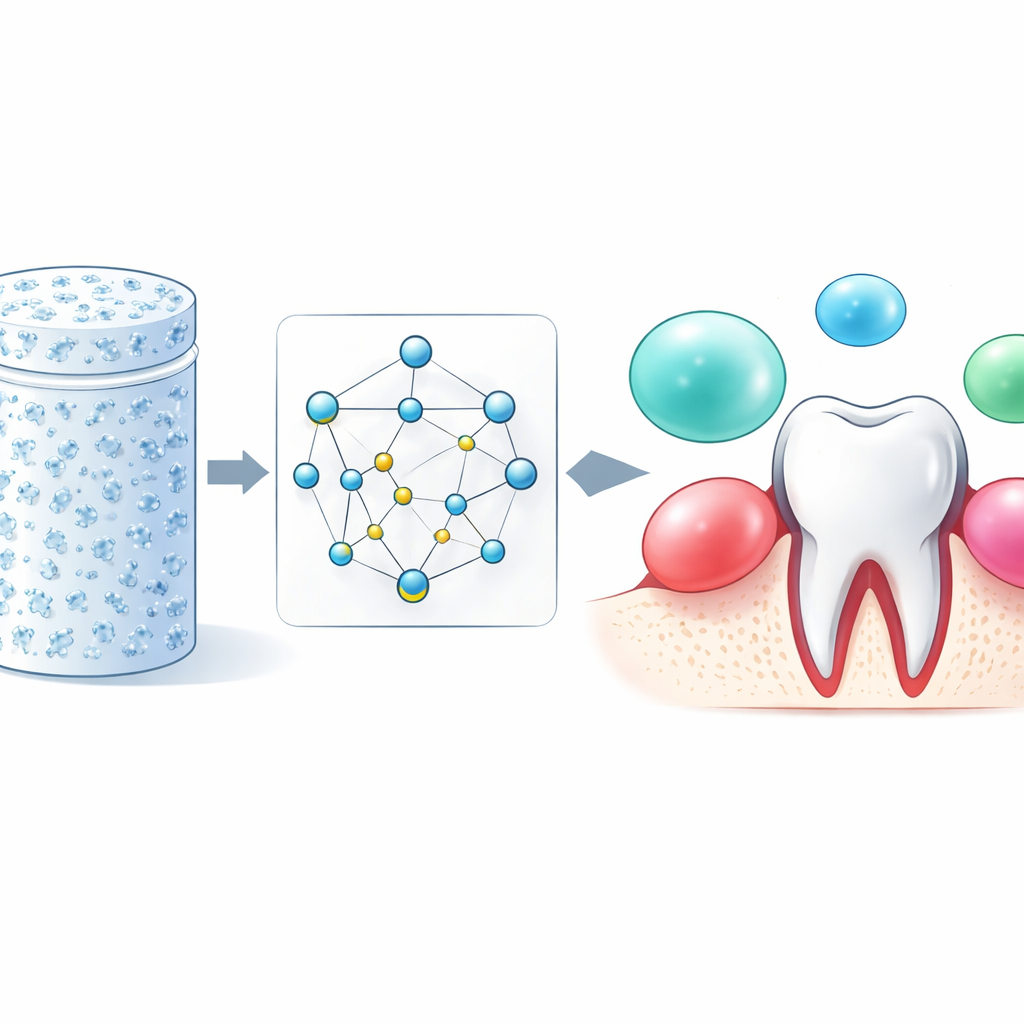
Vom zufälligen Versuch zur geleiteten Entwicklung
Weiche, wasserreiche Gele aus kleinen Molekülen gelten seit langem als vielversprechende Materialien für Wirkstofffreisetzung und Gewebereparatur. Insbesondere Gele aus Nukleosiden, der Molekülfamilie, aus der DNA und RNA bestehen, sind attraktiv, weil sie gut mit lebendem Gewebe kompatibel sind und kleinere Schäden in ihrer Struktur reparieren können. Bislang wurden brauchbare Versionen solcher Gele oft zufällig oder durch langsames Modifizieren chemischer Gruppen entdeckt — ein langsamer und unsicherer Prozess. Die Autorinnen und Autoren wollten einen großen Teil dieser Schätzarbeit durch einen systematischeren Weg ersetzen, der vorhersagt, welche Nukleosid-Moleküle Gele bilden können und wie sie sich im Körper verhalten könnten.
Computern beibringen, nützliche Moleküle zu erkennen
Das Team sammelte große öffentliche Datensätze, die beschreiben, wie Tausende kleiner Moleküle in biologischen Tests reagieren, darunter Toxizität, antibakterielle Wirksamkeit, antivirale Aktivität, entzündungshemmende Effekte und Aktivität gegen Tumorzellen. Für jedes Molekül berechneten sie Tausende numerischer Merkmale, die Aspekte seiner Struktur kodieren. Mit mehreren Typen von Modellen des maschinellen Lernens trainierten sie Computer, diese strukturellen Merkmale mit neun verschiedenen biologischen Aktivitäten zu verknüpfen. Um Überanpassung zu vermeiden und die Genauigkeit zu verbessern, filterten und wählten sie sorgfältig die informativsten Merkmale, bevor sie die Modelle bauten.
Sicherheit, Stabilität und antibakterielle Wirkung in Balance
Ein Gel zur Behandlung von Zahnfleischerkrankungen muss mehr leisten als nur Keime abzutöten. Das Material muss für menschliche Zellen sicher sein und ein stabiles, injizierbares Gel bilden, das in der Zahnfleischtasche verbleiben kann. Um diese Anforderungen auszubalancieren, führten die Forschenden zwei neue Bewertungswerkzeuge ein. Der Molecular Bioactivity Specificity Index hebt hervor, bei welcher einzelnen Aktivität ein Molekül besonders stark ist, etwa wenn es gezielt ein wichtiges Zahnfleischerreger-Bakterium angreift und auf anderen Gebieten unauffällig bleibt. Der Composite Molecular Attribute Score gewichtet mehrere Eigenschaften gleichzeitig und reiht Moleküle höher ein, die Gelbildung, geringe Toxizität und hohe antibakterielle Potenz am besten kombinieren.
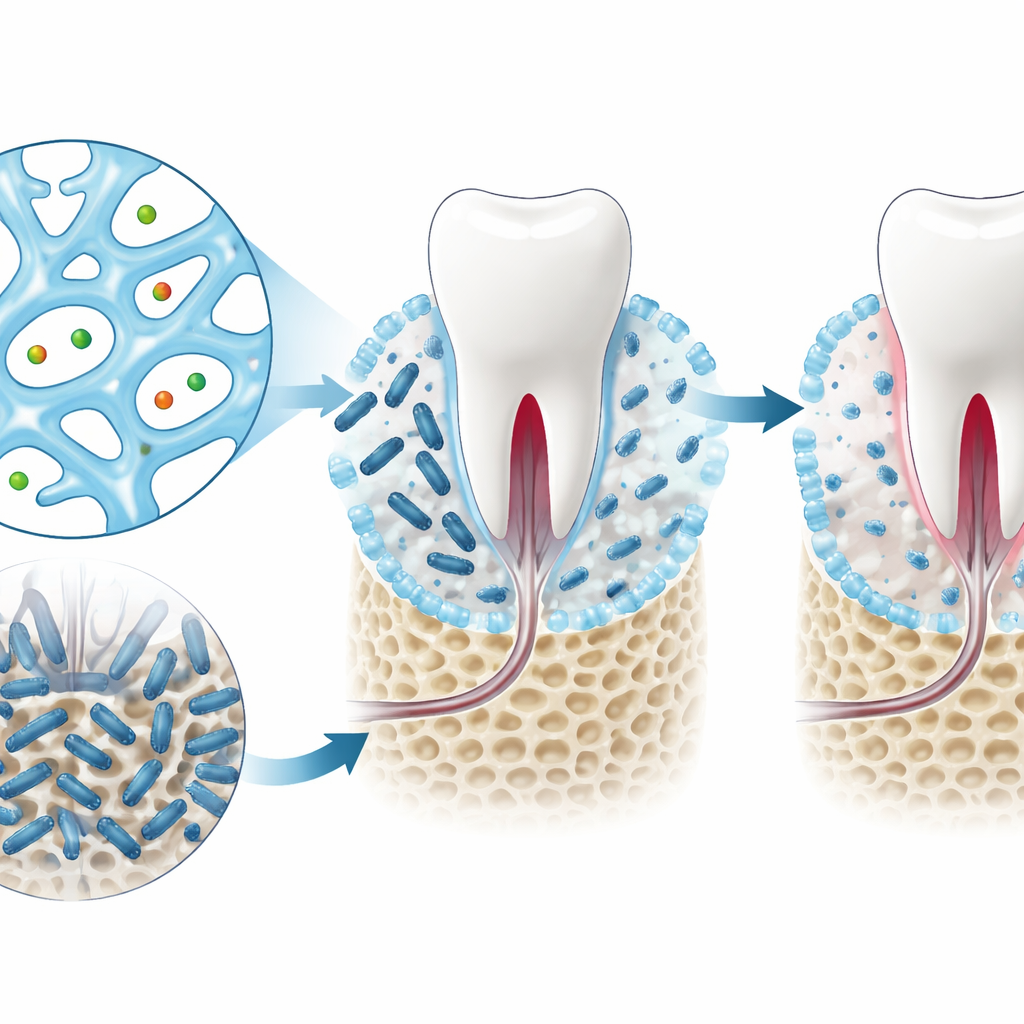
Von Computer-Treffern zu funktionierenden Hydrogelen
Mithilfe ihrer Modelle und des Bewertungssystems screente das Autorenteam mehr als siebentausend nukleosidbasierte Kandidaten und reduzierte die Liste auf vier Verbindungen, die realistisch im Labor herstellbar waren. Unter diesen stachen zwei verwandte Verbindungen, bekannt als GMP und dGMP, in Tests besonders hervor. Gemischt mit Silberionen bildeten sie weiche, poröse Gele mit guter mechanischer Festigkeit und der Fähigkeit, ihre Struktur nach Störung wiederherzustellen. Im Reagenzglas verringerten sowohl die freien Moleküle als auch ihre Gel-Formen das Wachstum von Porphyromonas gingivalis, einem Hauptbakterium, das mit Parodontitis verbunden ist, stark, während sie gegenüber Säugerzellen schonend blieben.
Test des Zahnfleischschutzes in lebenden Tieren
Als Nächstes testeten die Forschenden die Gele in Mäusemodellen der Zahnfleischerkrankung. In einem Experiment behandelten sie eine bereits etablierte Parodontitis, indem sie die Gele nach der Infektion mit P. gingivalis in die Zahnfleischtaschen injizierten. In einem anderen setzten sie die Gele kurz nach der Infektion ein, um zu prüfen, ob sie Schäden verhindern können. In beiden Fällen zeigten Aufnahmen des Kieferknochens, dass behandelte Mäuse weniger stützenden Knochen rund um die Zähne verloren und eine dichtere, gesündere Knochenstruktur behielten. Gewebeschnitte des Zahnfleisches zeigten reduzierte Entzündungszeichen und höhere Werte von Markern, die mit Heilung und Gewebereparatur verbunden sind. Wichtig ist, dass Kontrollen von wichtigen Organen und Injektionsstellen keinen eindeutigen Gewebeschaden oder anhaltende Entzündungen zeigten.
Was das für die zukünftige Mundpflege bedeutet
Für eine allgemeine Leserschaft lautet die Kernbotschaft, dass das Team einen intelligenteren Weg entwickelt hat, weiche, wirkstofftragende Gele für den Mund zu entwerfen, indem Computer aus umfangreichen chemischen und biologischen Datensätzen lernen. Ihr Ansatz identifizierte zwei nukleosidbasierte Gele, die sicher ein bedeutendes Zahnfleischerkrankungs-Bakterium bekämpfen und in Mäusen den Knochen um die Zähne erhalten helfen. Zwar ist noch weitere Arbeit nötig, bevor diese Materialien in die Klinik gelangen, doch die Studie legt nahe, dass maschinelles Lernen die Entwicklung gezielter Behandlungen für Zahnfleischerkrankungen und möglicherweise andere orale Erkrankungen beschleunigen könnte.
Zitation: Li, W., Wen, Y., Huang, Z. et al. Machine learning-driven discovery of therapeutic nucleoside hydrogels for periodontitis. Int J Oral Sci 18, 41 (2026). https://doi.org/10.1038/s41368-026-00438-3
Schlüsselwörter: maschinelles Lernen, Parodontitis, Hydrogele, orale Mikrobiota, Biomaterialien