Clear Sky Science · pt
Desenvolvendo fisiologia virtual de tecido tumoral humano para avaliação de malignidade
Por que apertar tumores importa
Quando pensamos em câncer, normalmente imaginamos células fora de controle crescendo sem limites. Mas tumores também são objetos físicos que empurram, puxam e comprimem os tecidos ao redor. Essas forças invisíveis podem ajudar a decidir se um tumor permanece relativamente contido ou se torna perigoso e difícil de tratar. Este estudo constrói um “gêmeo virtual” detalhado de amostras reais de tumores de mama para medir como as tensões dentro do tecido se relacionam com o quão perigoso um tumor pode ser — sem necessidade de experimentação direta em pacientes.
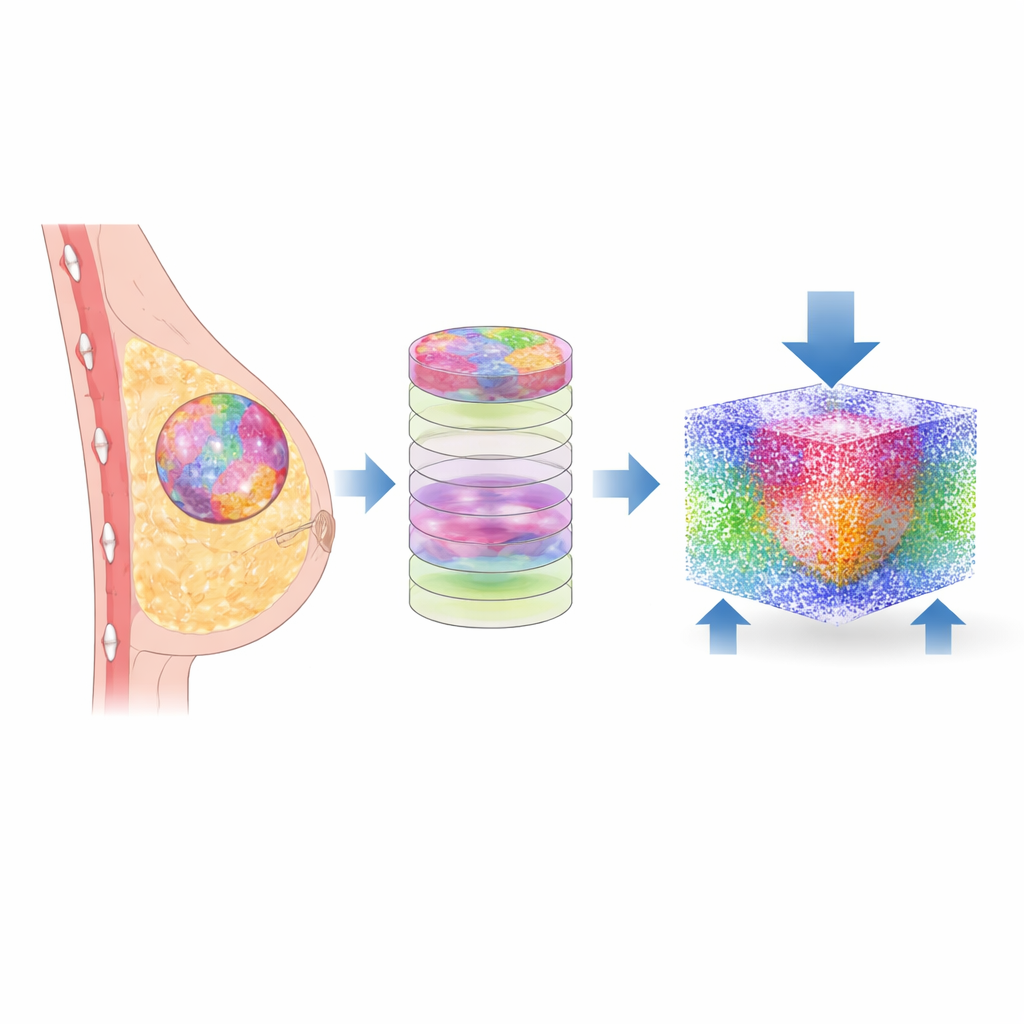
De uma lâmina de biópsia a um gêmeo digital
Os pesquisadores partiram de pequenas biópsias de tecido mamário semelhantes às examinadas por patologistas diariamente. Em vez de usar apenas corantes tradicionais, empregaram microscopia por transformada de Fourier no infravermelho (FTIR), que lê as impressões químicas do tecido. Com aprendizado de máquina, cada pixel da imagem foi classificado em um dos seis componentes: células malignas, células não cancerosas, vários tipos de tecido de suporte (estroma) e outros elementos. Software customizado então converteu essas imagens planas em camadas empilhadas, construindo um mapa tridimensional do tecido de cada paciente, preservando o emaranhado complexo de diferentes regiões exatamente como visto na amostra real.
Transformando tecido em física
Para explorar como essas estruturas se comportam sob carga, a equipe traduziu os mapas 3D em um modelo computacional baseado em partículas. Cada pequeno pedaço de tecido foi representado por partículas interagentes com propriedades mecânicas — como rigidez e densidade — extraídas de medições prévias de tecido mamário. Usando um método chamado hidrodinâmica por partículas suavizadas (smoothed particle hydrodynamics), simularam o que acontece quando uma pressão suave e fisiologicamente realista é aplicada em um lado do tecido, enquanto o lado oposto é mantido fixo. Isso lhes permitiu calcular como tensão e deformação — o quanto o tecido é comprimido e deformado — se propagam por cada componente de doze amostras de pacientes diferentes.
O que os tumores virtuais revelaram
As simulações mostraram que os tumores não sofrem tensões de forma uniforme. Amostras nas quais as áreas malignas estavam fragmentadas em muitas ilhas pequenas e dispersas apresentaram tensões locais muito mais altas do que tumores onde regiões malignas formavam manchas maiores e mais contínuas. O mesmo padrão apareceu para os tipos de tecido circundantes: manchas pequenas e desconectadas de qualquer componente tenderam a suportar cargas maiores do que regiões amplas e contínuas. A vizinhança também importou. Quando uma região rígida ficava ao lado de uma muito mais macia, ambas experimentavam tensões elevadas, enquanto aglomerados cercados por tecidos de rigidez semelhante sofriam menos deformação. Em alguns casos, até amostras classificadas como normais, mas com estrutura altamente mista e em mosaico, mostraram níveis de tensão comparáveis a tecidos claramente malignos.
Forças que podem inclinar o tecido rumo ao câncer
Essas tensões internas não foram apenas ondulações pequenas. Nos tecidos mais heterogêneos, as tensões compressivas previstas atingiram níveis que experimentos anteriores mostraram capazes de empurrar células saudáveis em direção a comportamentos malignos ao alterar como crescem, se movem ou morrem. Regiões malignas mais rígidas tendiam a deformar-se menos que vizinhos mais macios, mas contribuíam para concentrar tensão em componentes próximos. O modelo também rastreou como as áreas de superfície de diferentes regiões do tecido mudavam ao longo do tempo, revelando que componentes pequenos e desconectados não apenas sentiam tensões mais altas, mas também sofriam mudanças de forma maiores, o que poderia perturbar ainda mais o ambiente local.
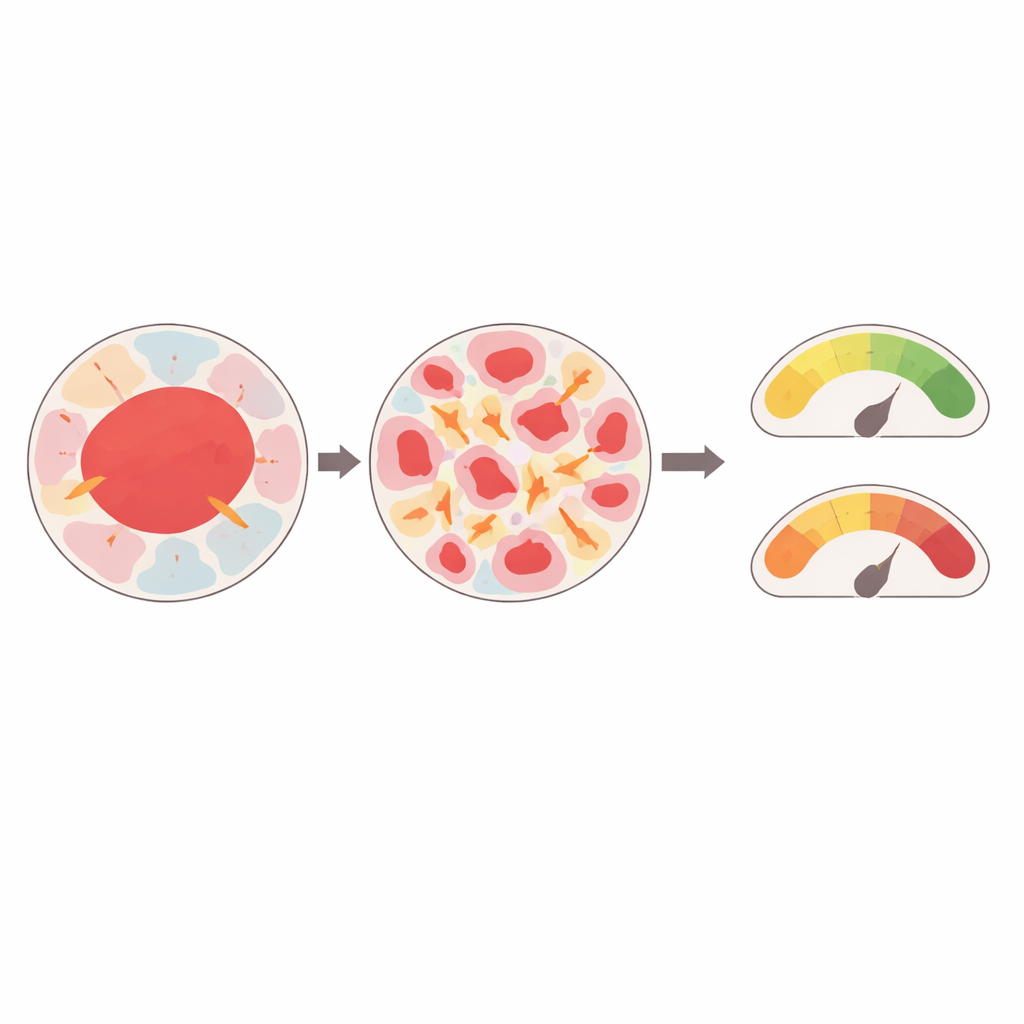
Rumo a impressões digitais mecânicas personalizadas de tumores
Ao vincular imagens reais de biópsias a simulações físicas detalhadas, o estudo entrega um “gêmeo fisiológico” conceitual para tumores de mama. Sugere que a forma como um tumor é montado — quão salteado ele é, o tamanho de cada região e quais tecidos se tocam — molda fortemente as forças mecânicas que atuam nele. Essas forças, por sua vez, estão dentro de faixas conhecidas por promover transformação maligna e resistência a terapias. No futuro, gêmeos digitais semelhantes podem ajudar a sinalizar tecidos aparentemente normais, mas mecanicamente estressados, que correm risco de se tornarem cancerosos, ou orientar médicos em planos de tratamento adaptados tanto à impressão digital mecânica única de um tumor quanto à sua genética.
Citação: Arbabi, S., Vincent, H., Hansen, E. et al. Developing virtual physiology of human tumor tissue for malignancy assessment. npj Precis. Onc. 10, 136 (2026). https://doi.org/10.1038/s41698-026-01316-1
Palavras-chave: câncer de mama, mecânica tumoral, gêmeo digital, microambiente tumoral, oncologia computacional