Clear Sky Science · es
Desarrollo de la fisiología virtual del tejido tumoral humano para la evaluación de la malignidad
Por qué importa apretar los tumores
Cuando pensamos en el cáncer, normalmente imaginamos células fuera de control que crecen sin freno. Pero los tumores también son objetos físicos que empujan, tiran y comprimen los tejidos que los rodean. Esas fuerzas invisibles pueden ayudar a determinar si un tumor se mantiene relativamente contenido o se vuelve potencialmente mortal y difícil de tratar. Este estudio construye un "gemelo virtual" detallado de muestras reales de tumores de mama humanos para medir cómo las tensiones dentro del tejido se relacionan con la peligrosidad de un tumor, sin necesidad de experimentar directamente en pacientes.
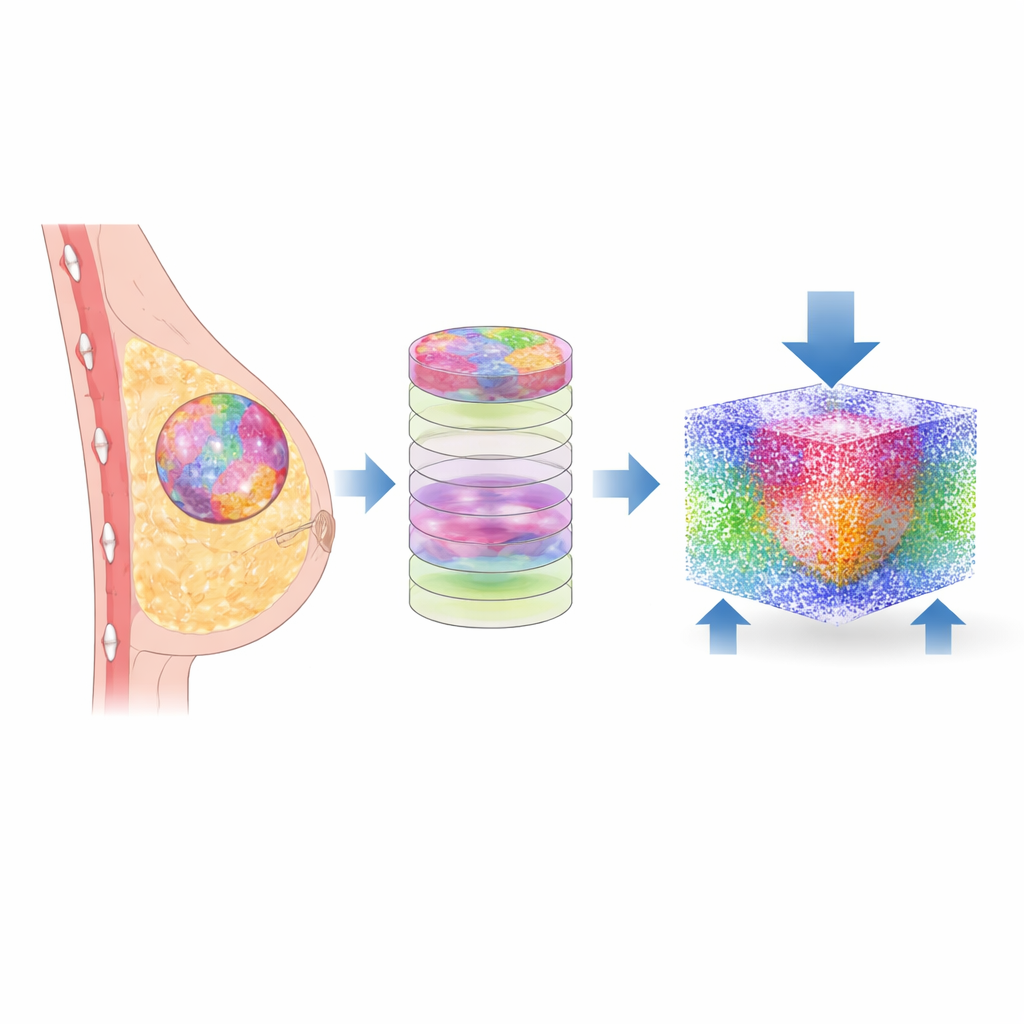
De una lámina de biopsia a un gemelo digital
Los investigadores partieron de pequeñas biopsias de tejido mamario similares a las que examinan los patólogos a diario. En lugar de limitarse a coloraciones tradicionales, usaron microscopía FTIR (transformada de Fourier en el infrarrojo), que lee las huellas químicas del tejido. Con aprendizaje automático, cada píxel de la imagen se clasificó en uno de seis componentes: células malignas, células no cancerosas, varios tipos de tejido de soporte (estroma) y otros elementos. Un software personalizado convirtió luego esas imágenes planas en capas apiladas, construyendo un mapa tridimensional del tejido de cada paciente y preservando el complejo mosaico de diferentes regiones tal como se ve en la muestra real.
Convertir tejido en física
Para explorar cómo se comportan estas estructuras bajo carga, el equipo tradujo los mapas 3D a un modelo computacional basado en partículas. Cada pequeño fragmento de tejido se representó por partículas interactivas con propiedades mecánicas —como rigidez y densidad— extraídas de mediciones previas de tejido mamario. Usando un método llamado hidrodinámica de partículas suavizadas, simularon lo que ocurre cuando se aplica desde un lado una presión suave y fisiológicamente realista, mientras el lado opuesto se mantiene fijado. Esto les permitió calcular cómo se propagan el esfuerzo y la deformación —cuánto se comprime y deforma el tejido— a través de cada componente en doce muestras de pacientes distintas.
Lo que revelaron los tumores virtuales
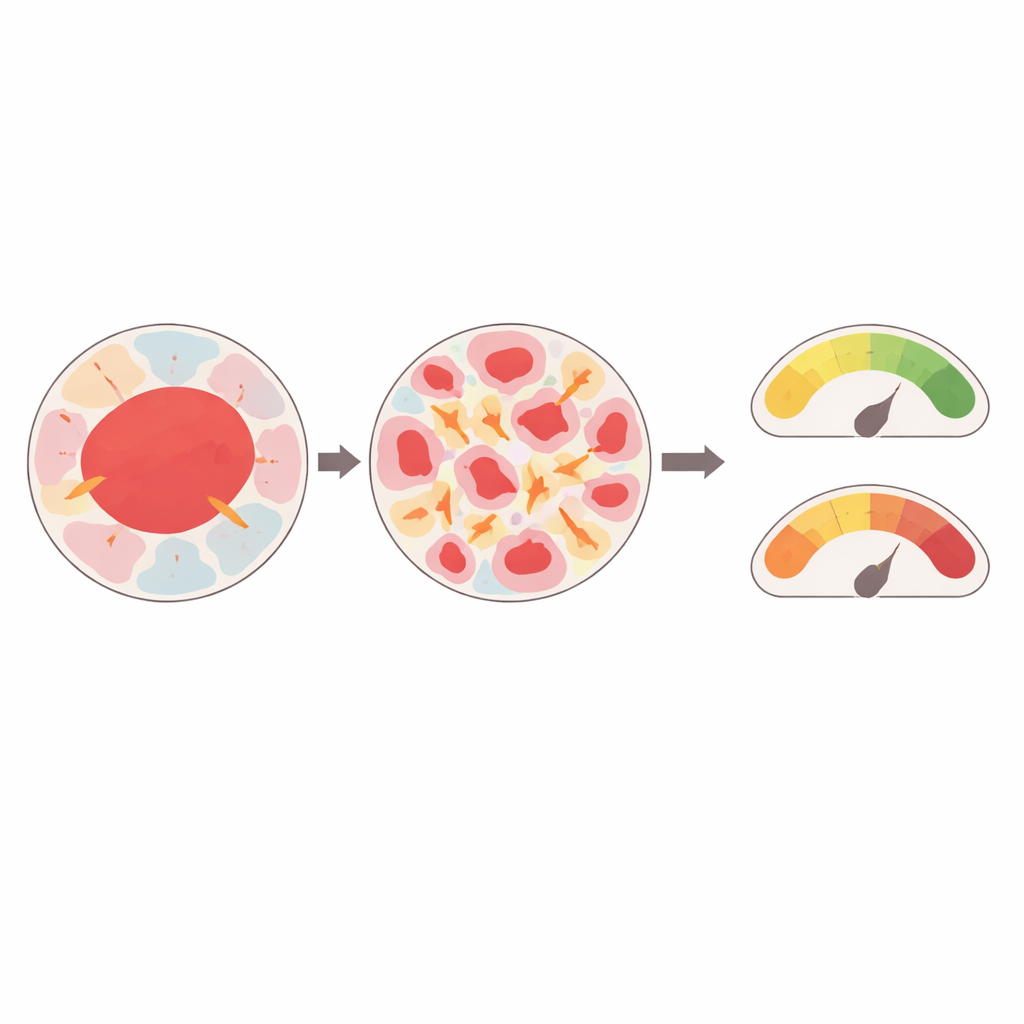
Las simulaciones mostraron que los tumores no están sometidos a estrés de manera uniforme. Las muestras en las que las zonas malignas estaban fragmentadas en muchas islas pequeñas y dispersas experimentaron tensiones locales mucho más altas que los tumores donde las regiones malignas formaban parches más grandes y continuos. El mismo patrón se observó en los tipos de tejido circundantes: los parches pequeños y desconectados de cualquier componente tendían a soportar cargas mayores que las regiones amplias y continuas. También importaba el vecindario. Cuando una región rígida estaba junto a otra mucho más blanda, ambas experimentaban tensiones elevadas, mientras que los agrupamientos rodeados por tejido de rigidez similar estaban menos deformados. En algunos casos, incluso muestras clasificadas como normales pero con una estructura muy mezclada y tipo mosaico mostraron niveles de estrés comparables a tejidos claramente malignos.
Fuerzas que pueden empujar el tejido hacia el cáncer
Estas tensiones internas no fueron meras ondulaciones pequeñas. En los tejidos más heterogéneos, las tensiones compresivas predichas alcanzaron niveles que experimentos previos han mostrado que pueden empujar a células sanas hacia comportamientos malignos al alterar cómo crecen, se mueven o mueren. Las regiones malignas, más rígidas, tendían a deformarse menos que sus vecinas más blandas, pero contribuían a concentrar las tensiones en los componentes cercanos. El modelo también registró cómo cambiaban con el tiempo las áreas superficiales de las distintas regiones tisulares, revelando que los componentes pequeños y desconectados no solo sentían mayores tensiones sino que también sufrían cambios de forma más grandes, lo que podría perturbar aún más el entorno local.
Hacia huellas mecánicas personalizadas de los tumores
Al vincular imágenes reales de biopsias con simulaciones físicas detalladas, el estudio presenta una prueba de concepto de una "fisiología virtual" para los tumores de mama. Sugiere que la forma en que se construye un tumor —qué tan parcheado es, el tamaño de cada región y qué tejidos contactan entre sí— determina en gran medida las fuerzas mecánicas que actúan en su interior. Esas fuerzas, a su vez, se sitúan en rangos conocidos por favorecer la transformación maligna y la resistencia a terapias. En el futuro, gemelos digitales similares podrían ayudar a señalar tejidos aparentemente normales pero mecánicamente estresados que corren riesgo de volverse cancerosos, o guiar a los médicos hacia planes de tratamiento adaptados a la huella mecánica única de un tumor además de su genética.
Cita: Arbabi, S., Vincent, H., Hansen, E. et al. Developing virtual physiology of human tumor tissue for malignancy assessment. npj Precis. Onc. 10, 136 (2026). https://doi.org/10.1038/s41698-026-01316-1
Palabras clave: cáncer de mama, mecánica tumoral, gemelo digital, microambiente tumoral, oncología computacional