Clear Sky Science · it
Sviluppare una fisiologia virtuale del tessuto tumorale umano per la valutazione della malignità
Perché strizzare i tumori è importante
Quando pensiamo al cancro, di solito immaginiamo cellule ribelli che crescono fuori controllo. Ma i tumori sono anche oggetti fisici che spingono, tirano e comprimono i tessuti circostanti. Quelle forze invisibili possono contribuire a stabilire se un tumore rimane relativamente contenuto o diventa pericoloso per la vita e difficile da trattare. Questo studio costruisce un dettagliato "gemello virtuale" di campioni reali di tumore mammario umano per misurare come gli stress all’interno del tessuto si relazionano al grado di pericolosità del tumore—senza dover sperimentare direttamente sui pazienti.
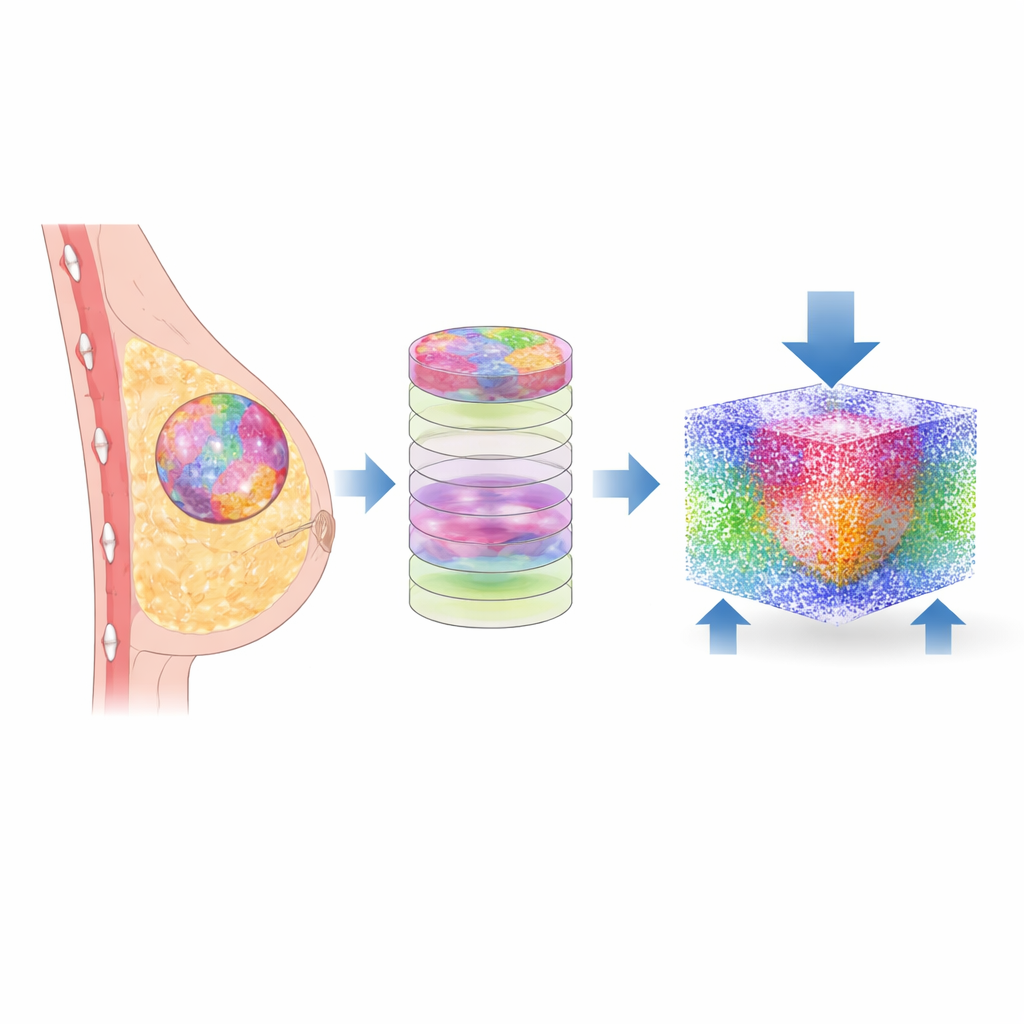
Da un vetrino di biopsia a un doppio digitale
I ricercatori sono partiti da piccole biopsie di tessuto mammario simili a quelle esaminate quotidianamente dai patologi. Invece dei soli coloranti tradizionali, hanno usato la microscopia FTIR (trasformata di Fourier nell’infrarosso), che legge le impronte chimiche del tessuto. Con l’apprendimento automatico, ogni pixel dell’immagine è stato classificato in uno dei sei componenti: cellule maligne, cellule non cancerose, diversi tipi di tessuto di supporto (stroma) e altri elementi. Un software su misura ha quindi convertito queste immagini piatte in strati sovrapposti, costruendo una mappa tridimensionale del tessuto di ciascun paziente, preservando il complesso mosaico delle diverse regioni esattamente come appare nel campione reale.
Trasformare il tessuto in fisica
Per esplorare come queste strutture si comportano sotto carico, il team ha tradotto le mappe 3D in un modello numerico basato su particelle. Ogni piccola porzione di tessuto è stata rappresentata da particelle interagenti con proprietà meccaniche—come rigidità e densità—derivate da misure precedenti sui tessuti mammari. Utilizzando un metodo chiamato idrodinamica a particelle smussate (smoothed particle hydrodynamics), hanno simulato cosa accade quando una pressione lieve e fisiologicamente realistica è applicata da un lato del tessuto, mentre il lato opposto è tenuto fisso. Questo ha permesso di calcolare come stress e deformazione—quanto il tessuto viene compresso e deformato—si propagano attraverso ogni componente di dodici diversi campioni di pazienti.
Cosa hanno rivelato i tumori virtuali
Le simulazioni hanno mostrato che i tumori non sono stressati in modo uniforme. I campioni in cui le aree maligne erano frammentate in molte piccole isole sparse hanno sperimentato stress locali molto più elevati rispetto ai tumori in cui le regioni maligne formavano macchie più grandi e continue. Lo stesso schema è apparso per i tipi di tessuto circostanti: piccole porzioni disconnesse di qualunque componente tendevano a sopportare carichi maggiori rispetto a regioni ampie e continue. Anche il vicinato contava. Quando una regione rigida si trovava accanto a una molto più morbida, entrambe sperimentavano stress elevati, mentre ammassi circondati da tessuto di rigidità simile risultavano meno sollecitati. In alcuni casi, anche campioni classificati come normali ma con struttura fortemente mista e a mosaico mostravano livelli di stress comparabili a tessuti chiaramente maligni.
Forze che possono spingere il tessuto verso il cancro
Questi stress interni non erano solo piccoli increspature. Nei tessuti più eterogenei, gli stress compressivi predetti raggiungevano livelli che esperimenti precedenti hanno mostrato essere in grado di spingere le cellule sane verso comportamenti maligni alterando il loro modo di crescere, muoversi o morire. Le regioni più rigide e maligne tendevano a deformarsi meno rispetto ai vicini più morbidi, ma contribuivano a concentrare lo stress nelle componenti vicine. Il modello ha anche monitorato come le aree superficiali delle diverse regioni tissutali cambiassero nel tempo, rivelando che le componenti piccole e disconnesse non solo avvertivano stress maggiori ma subivano anche variazioni di forma più ampie, che potrebbero ulteriormente perturbare l’ambiente locale.
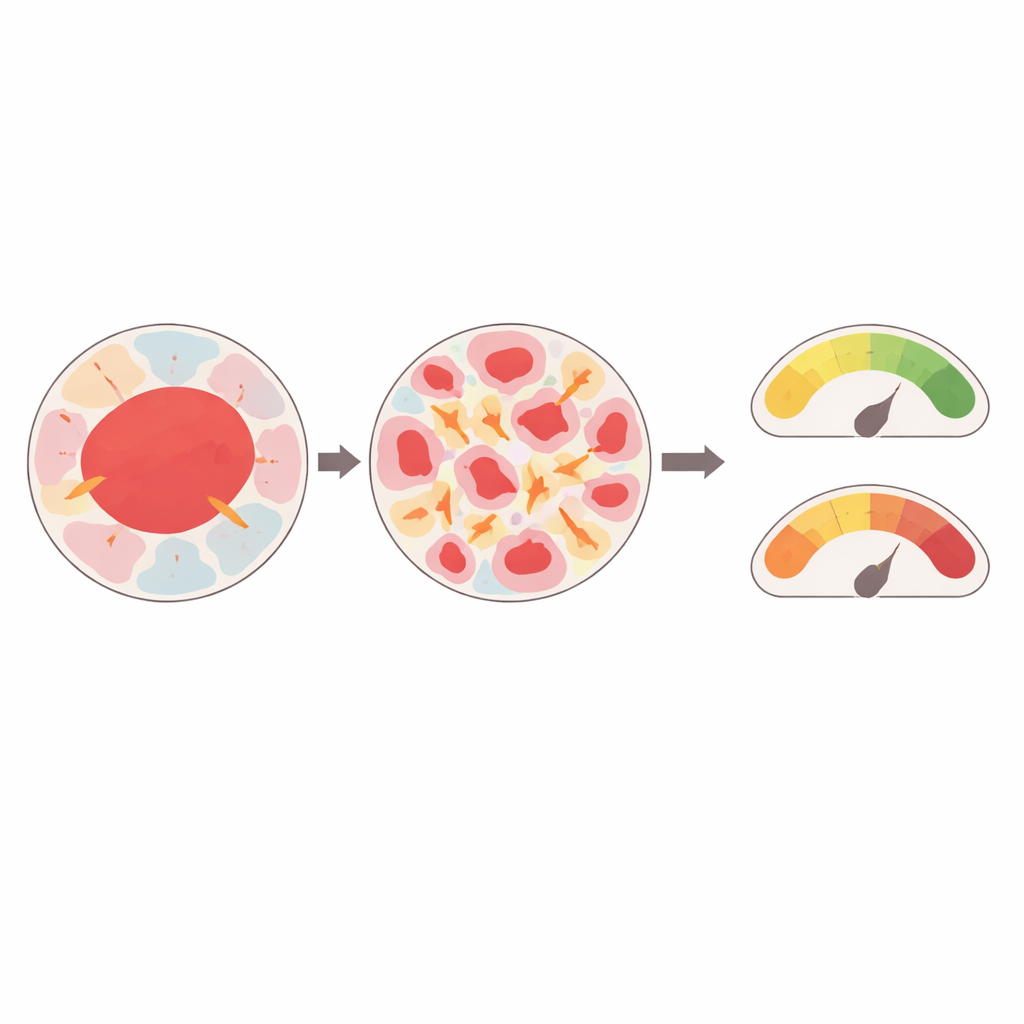
Verso impronte meccaniche personalizzate dei tumori
Collegando immagini reali di biopsie a simulazioni fisiche dettagliate, lo studio fornisce una prova di principio di una "fisiologia virtuale" per i tumori mammari. Suggerisce che il modo in cui un tumore è costruito—quanto è frammentato, quanto è grande ciascuna regione e quali tessuti si toccano—modella fortemente le forze meccaniche che agiscono al suo interno. Queste forze, a loro volta, rientrano in intervalli noti per favorire la trasformazione maligna e la resistenza alle terapie. In futuro, gemelli digitali simili potrebbero aiutare a segnalare tessuti apparentemente normali ma meccanicamente stressati a rischio di diventare cancerosi, oppure guidare i medici verso piani di trattamento personalizzati sulla base dell’impronta meccanica unica di un tumore oltre che del suo profilo genetico.
Citazione: Arbabi, S., Vincent, H., Hansen, E. et al. Developing virtual physiology of human tumor tissue for malignancy assessment. npj Precis. Onc. 10, 136 (2026). https://doi.org/10.1038/s41698-026-01316-1
Parole chiave: cancro al seno, meccanica del tumore, doppio digitale, microambiente tumorale, oncologia computazionale