Clear Sky Science · pl
Opracowywanie wirtualnej fizjologii tkanki nowotworowej człowieka do oceny złośliwości
Dlaczego ściskanie guzów ma znaczenie
Kiedy myślimy o raku, zwykle wyobrażamy sobie zbuntowane komórki rosnące bez kontroli. Jednak guzy są też obiektami fizycznymi, które naciskają, ciągną i ściskają okoliczne tkanki. Te niewidoczne siły mogą decydować, czy guz pozostanie stosunkowo ograniczony, czy stanie się zagrażający życiu i trudny do leczenia. W tym badaniu zbudowano szczegółowy „wirtualny bliźniak” rzeczywistych próbek nowotworów piersi, aby zmierzyć, jak naprężenia wewnątrz tkanki korelują z potencjalnym niebezpieczeństwem guza — bez konieczności bezpośrednich eksperymentów na pacjentach.
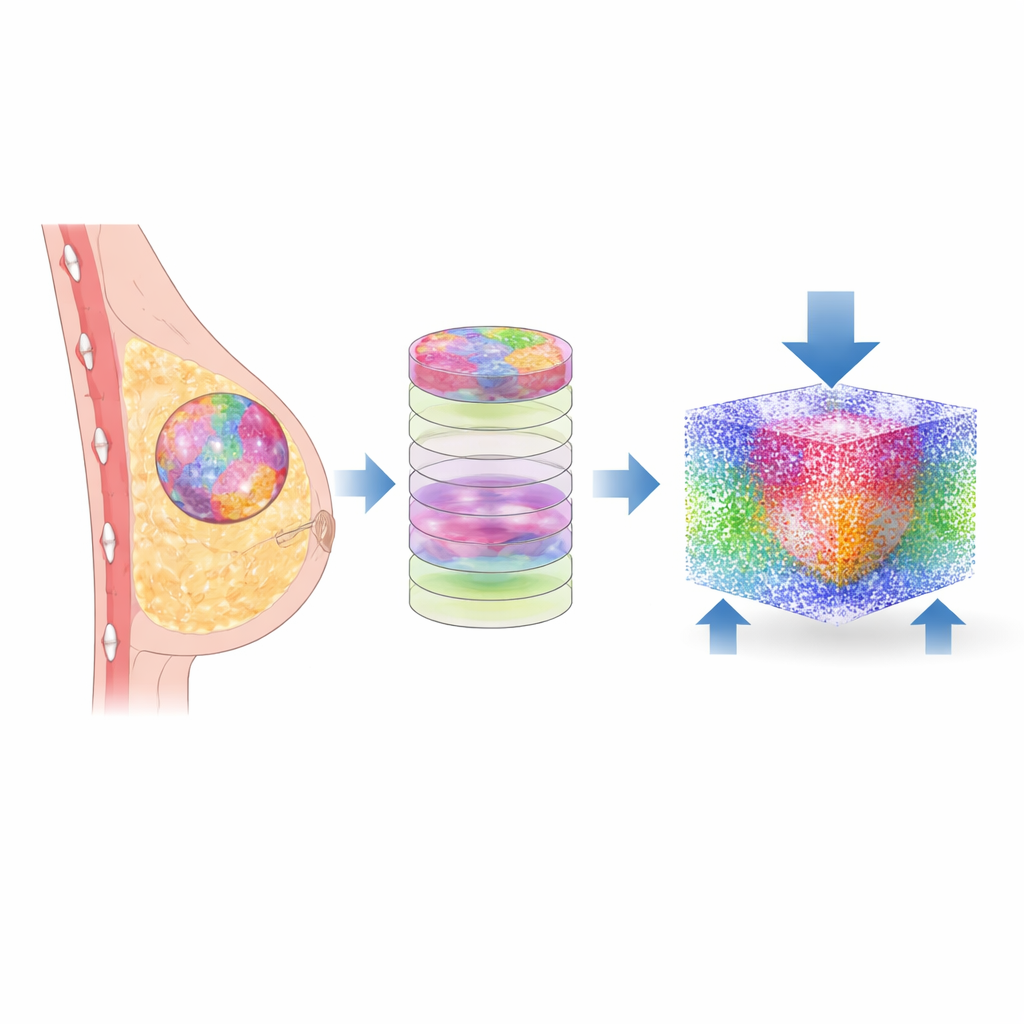
Z preparatu do cyfrowego bliźniaka
Naukowcy zaczęli od drobnych biopsji tkanki piersi podobnych do tych, które codziennie analizują patolodzy. Zamiast polegać wyłącznie na tradycyjnych barwieniach, użyli mikroskopii w podczerwieni z transformatą Fouriera (FTIR), która odczytuje chemiczne odciski palców tkanki. Za pomocą uczenia maszynowego każdy piksel obrazu został sklasyfikowany jako jeden z sześciu składników: komórki złośliwe, komórki niezłośliwe, kilka typów tkanki podporowej (stroma) oraz inne elementy. Autorskie oprogramowanie przekształciło te płaskie obrazy w nałożone warstwy, budując trójwymiarową mapę tkanki każdego pacjenta i zachowując złożony patchwork różnych regionów dokładnie takim, jak w rzeczywistej próbce.
Przekształcanie tkanki w fizykę
Aby zbadać zachowanie tych struktur pod obciążeniem, zespół przekonwertował mapy 3D na model komputerowy oparty na cząstkach. Każdy drobny fragment tkanki reprezentowano jako oddziałujące cząstki o właściwościach mechanicznych — takich jak sztywność i gęstość — zaczerpniętych z wcześniejszych pomiarów tkanki piersi. Przy użyciu metody zwanej wygładzonymi hydrodynamikami cząstek (smoothed particle hydrodynamics) zasymulowano, co się dzieje, gdy z jednej strony przykładane jest delikatne, fizjologicznie realistyczne ciśnienie, podczas gdy przeciwna strona jest unieruchomiona. Pozwoliło to obliczyć, jak naprężenia i odkształcenia — ile tkanka jest ściskana i odkształcana — rozprzestrzeniają się przez każdy składnik w dwunastu różnych próbkach pacjentów.
Co ujawniły wirtualne guzy
Symulacje wykazały, że guzom nie towarzyszą jednakowe naprężenia. Próbki, w których obszary złośliwe były rozbite na wiele małych, rozproszonych wysp, doświadczyły znacznie wyższych naprężeń lokalnych niż guzy, gdzie obszary złośliwe tworzyły większe, bardziej ciągłe płaty. Podobny wzorzec zaobserwowano w otaczających typach tkanki: małe, odizolowane fragmenty dowolnego składnika zwykle przenosiły większe obciążenia niż rozległe, ciągłe obszary. Istotne było też sąsiedztwo. Gdy sztywny region sąsiadował z dużo miększym, oba doświadczały podwyższonych naprężeń, podczas gdy skupiska otoczone tkanką o podobnej sztywności były mniej odkształcone. W niektórych przypadkach nawet próbki klasyfikowane jako „normalne”, ale o wysoce zmieszanej, mozaikowej strukturze, wykazywały poziomy naprężeń porównywalne z wyraźnie złośliwymi tkankami.
Siły, które mogą pchnąć tkankę ku rakowi
Te wewnętrzne naprężenia nie były jedynie drobnymi fluktuacjami. W najbardziej heterogenicznych tkankach przewidywane naprężenia ściskające osiągały poziomy, które wcześniejsze eksperymenty wykazały jako zdolne skłonić zdrowe komórki do zachowań złośliwych przez zmiany w sposobie ich wzrostu, poruszania się lub umierania. Sztywniejsze, złośliwe obszary miały tendencję do mniejszego odkształcania się niż sąsiednie, miększe regiony, ale przyczyniały się do koncentracji naprężeń w pobliskich składnikach. Model śledził również, jak powierzchnie różnych regionów tkanki zmieniały się w czasie, pokazując, że małe, odizolowane fragmenty nie tylko odczuwały większe naprężenia, lecz także przechodziły większe zmiany kształtu, co mogłoby dodatkowo zaburzać lokalne środowisko.
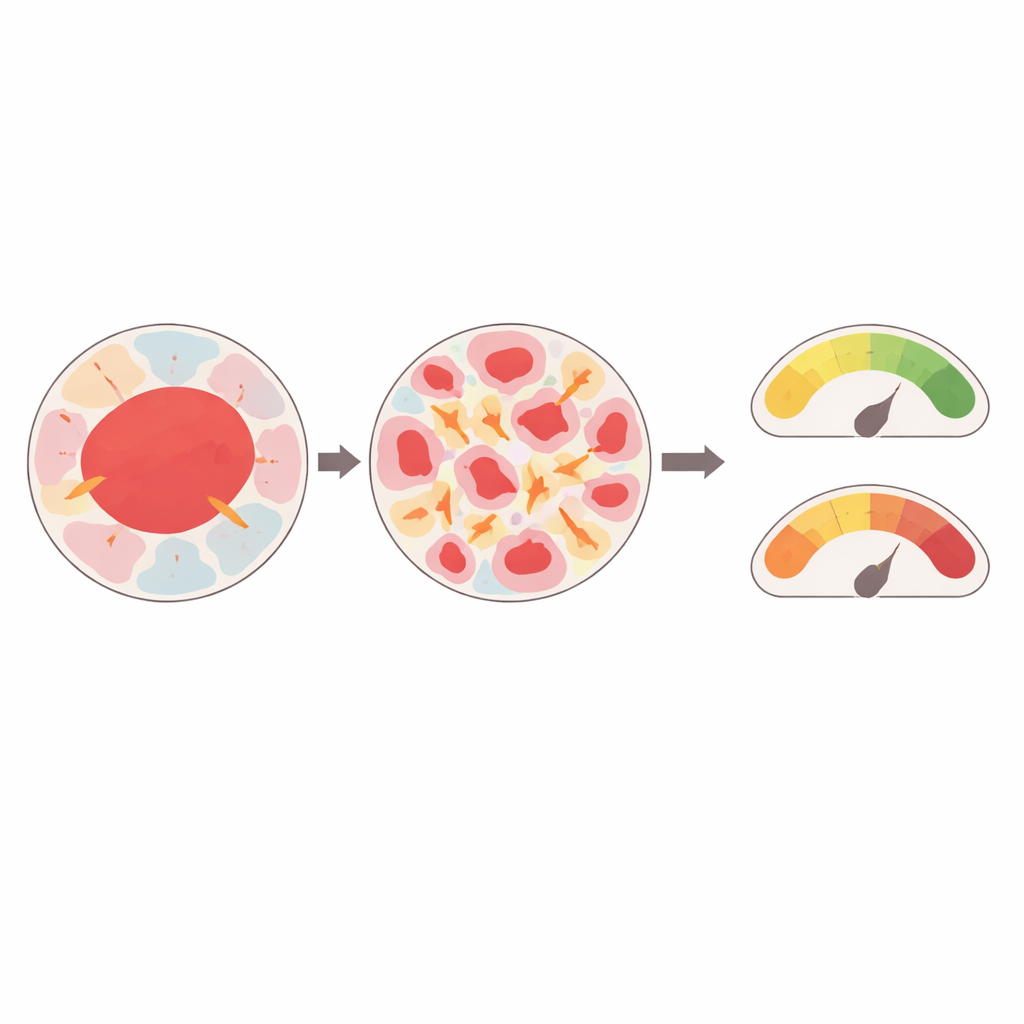
W kierunku spersonalizowanych mechanicznych odcisków palców guzów
Łącząc rzeczywiste obrazy z biopsji z szczegółowymi symulacjami fizycznymi, badanie dostarcza dowodu koncepcji „wirtualnej fizjologii” dla guzów piersi. Sugestia jest taka, że sposób, w jaki zbudowany jest guz — jak bardzo jest łaciaty, jak duże są poszczególne regiony i które tkanki stykają się ze sobą — w istotny sposób kształtuje siły mechaniczne działające wewnątrz niego. Te siły z kolei mieszczą się w zakresach znanych z promowania przemiany złośliwej i oporności na terapię. W przyszłości podobne cyfrowe bliźniaki mogą pomagać wykrywać pozornie normalne, lecz mechanicznie obciążone tkanki zagrożone przekształceniem nowotworowym albo wspierać lekarzy w doborze planów leczenia dostosowanych do unikatowego mechanicznego odcisku palca guza, oprócz jego profilu genetycznego.
Cytowanie: Arbabi, S., Vincent, H., Hansen, E. et al. Developing virtual physiology of human tumor tissue for malignancy assessment. npj Precis. Onc. 10, 136 (2026). https://doi.org/10.1038/s41698-026-01316-1
Słowa kluczowe: rak piersi, mechanika guza, cyfrowy bliźniak, mikrośrodowisko guza, onkologia obliczeniowa