Clear Sky Science · de
Entwicklung einer virtuellen Physiologie menschlichen Tumorgewebes zur Beurteilung von Bösartigkeit
Warum das Zusammendrücken von Tumoren wichtig ist
Wenn wir an Krebs denken, stellen wir uns meist entgleiste Zellen vor, die unkontrolliert wachsen. Tumore sind aber auch physische Objekte, die das umliegende Gewebe drücken, ziehen und zusammendrücken. Diese unsichtbaren Kräfte können mitentscheiden, ob ein Tumor relativ lokal begrenzt bleibt oder lebensgefährlich und schwer zu behandeln wird. Diese Studie erstellt einen detaillierten «virtuellen Zwilling» realer menschlicher Brusttumorproben, um zu messen, wie die inneren Spannungen im Gewebe mit der Gefährlichkeit eines Tumors zusammenhängen — ohne direkte Experimente an Patientinnen und Patienten.
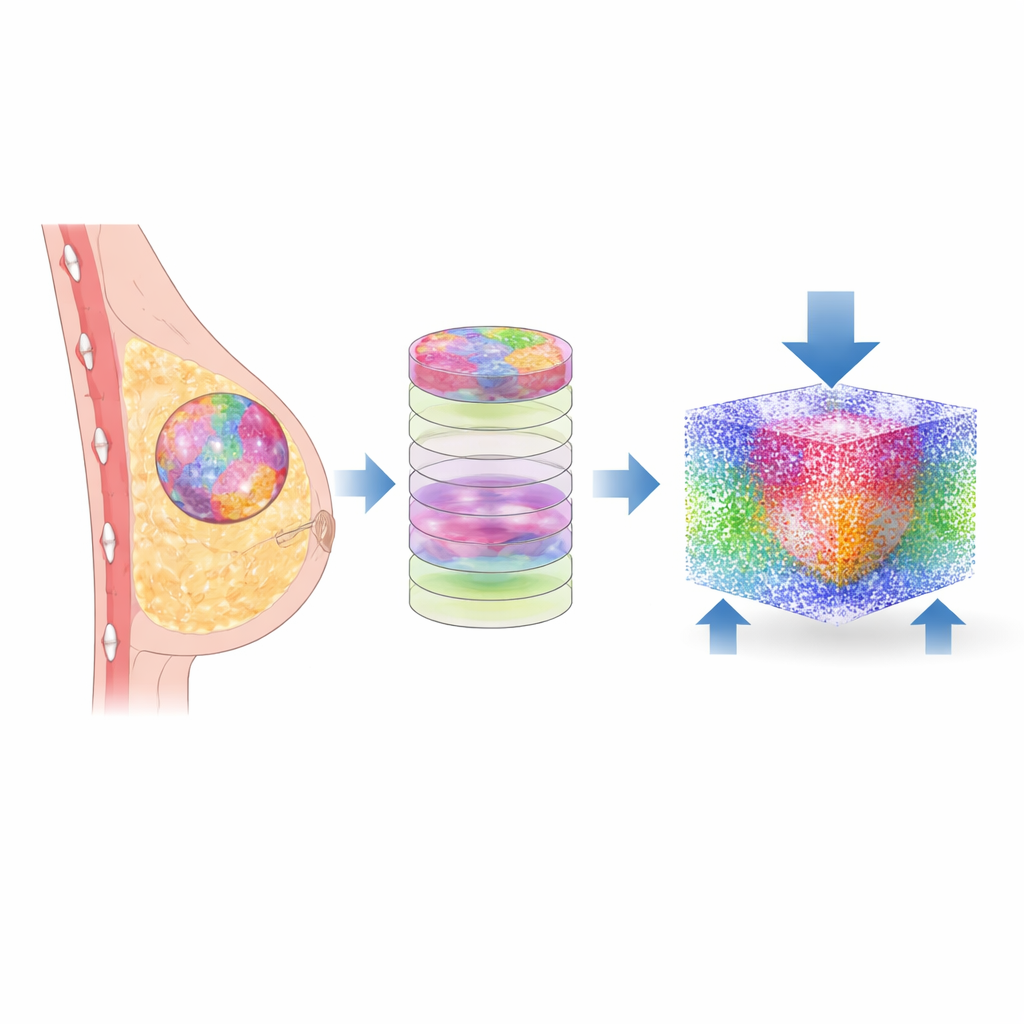
Von einem Biopsieschnitt zum digitalen Zwilling
Die Forschenden begannen mit winzigen Brustgewebebiopsien, wie sie Pathologinnen und Pathologen täglich untersuchen. Anstelle rein traditioneller Färbungen nutzten sie Fourier-Transformations-Infrarot(FTIR)-Mikroskopie, die chemische Fingerabdrücke des Gewebes erfasst. Mit maschinellem Lernen wurde jedes Pixel im Bild einer von sechs Komponenten zugeordnet: bösartige Zellen, nicht‑krebserregende Zellen, mehrere Typen von Stroma (unterstützendes Gewebe) und andere Elemente. Maßgeschneiderte Software wandelte diese flachen Bilder in geschichtete Ebenen um und baute so eine dreidimensionale Karte des Gewebes jeder Patientin bzw. jedes Patienten, wobei das komplexe Mosaik unterschiedlicher Regionen genau so erhalten blieb, wie es in der echten Probe zu sehen war.
Gewebe in Physik übersetzen
Um zu untersuchen, wie diese Strukturen unter Belastung reagieren, übersetzte das Team die 3D‑Karten in ein teilchenbasiertes Computermodell. Jedes winzige Gewebestück wurde durch interagierende Partikel mit mechanischen Eigenschaften — etwa Steifigkeit und Dichte — dargestellt, die aus früheren Messungen von Brustgewebe stammen. Mit einer Methode namens smoothed particle hydrodynamics simulierten sie, was passiert, wenn von einer Seite ein sanfter, physiologisch realistischer Druck angelegt wird, während die gegenüberliegende Seite fixiert bleibt. So konnten sie berechnen, wie sich Spannung und Dehnung — also wie sehr das Gewebe zusammengedrückt und verformt wird — durch jede Komponente in zwölf verschiedenen Patientenproben ausbreiten.
Was die virtuellen Tumore zeigten
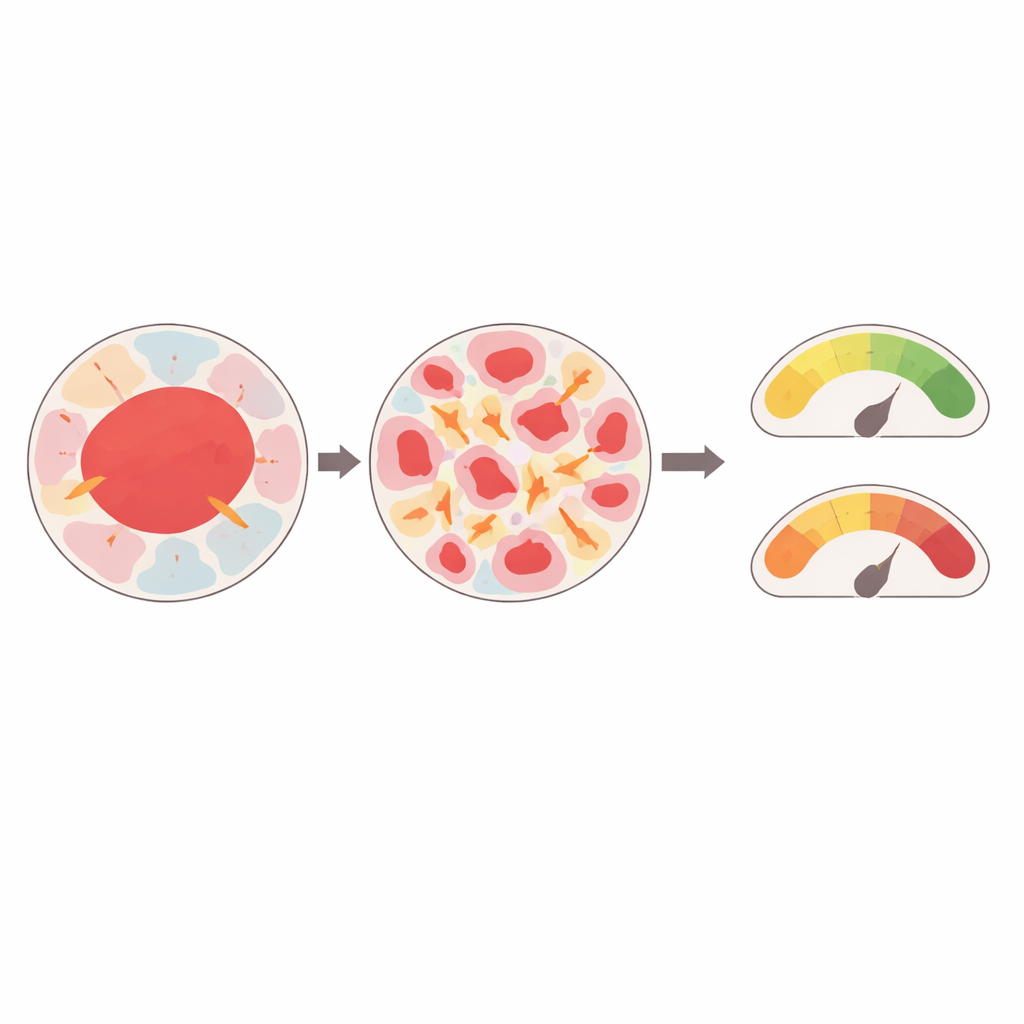
Die Simulationen ergaben, dass Tumore nicht gleichmäßig belastet sind. Proben, in denen bösartige Bereiche in viele kleine, verstreute Inseln zerteilt waren, erfuhren deutlich höhere lokale Spannungen als Tumore, in denen bösartige Regionen größere, zusammenhängende Flächen bildeten. Dasselbe Muster zeigte sich für die umgebenden Gewebetypen: Kleine, getrennte Flecken einer Komponente trugen tendenziell höhere Lasten als breite, zusammenhängende Regionen. Auch die Nachbarschaft spielte eine Rolle. Wenn eine steife Region neben einer deutlich weicheren lag, erfuhren beide erhöhte Spannungen, während Cluster, die von Gewebe ähnlicher Steifigkeit umgeben waren, weniger stark beansprucht wurden. In einigen Fällen wiesen sogar Proben, die als normal klassifiziert waren, aber eine stark durchmischte, mosaikartige Struktur hatten, Stresswerte auf, die mit klar bösartigen Geweben vergleichbar waren.
Kräfte, die Gewebe in Richtung Krebs kippen können
Diese inneren Spannungen waren nicht nur kleine Wellen. In den heterogensten Geweben erreichten die vorhergesagten Kompressionsspannungen Werte, die frühere Experimente gezeigt haben, dass sie gesunde Zellen durch Veränderungen in Wachstum, Bewegung oder Überleben in eine maligne Richtung drängen können. Steifere, bösartige Regionen neigten dazu, sich weniger zu verformen als ihre weicheren Nachbarn, trugen jedoch dazu bei, Stress in benachbarten Komponenten zu konzentrieren. Das Modell verfolgte außerdem, wie sich die Oberflächenflächen verschiedener Geweberegionen im Laufe der Zeit veränderten, und zeigte, dass kleine, getrennte Komponenten nicht nur höhere Spannungen erfahren, sondern auch größere Formänderungen durchlaufen, was die lokale Umgebung weiter stören könnte.
Auf dem Weg zu personalisierten mechanischen Fingerabdrücken von Tumoren
Indem reale Biopsiebilder mit detaillierten physikalischen Simulationen verknüpft werden, liefert die Studie einen Proof‑of‑Concept für eine «virtuelle Physiologie» von Brusttumoren. Sie legt nahe, dass die Bauweise eines Tumors — wie fleckig er ist, wie groß einzelne Regionen sind und welche Gewebe aneinandergrenzen — die mechanischen Kräfte innerhalb stark bestimmt. Diese Kräfte liegen wiederum in Bereichen, die dafür bekannt sind, maligne Transformation und Therapie‑Resistenz zu fördern. In Zukunft könnten ähnliche digitale Zwillinge helfen, scheinbar normales, aber mechanisch belastetes Gewebe zu erkennen, das Gefahr läuft, krebshaft zu werden, oder Ärztinnen und Ärzten dabei helfen, Behandlungspläne zu entwickeln, die auf dem einzigartigen mechanischen Fingerabdruck eines Tumors ebenso beruhen wie auf dessen Genetik.
Zitation: Arbabi, S., Vincent, H., Hansen, E. et al. Developing virtual physiology of human tumor tissue for malignancy assessment. npj Precis. Onc. 10, 136 (2026). https://doi.org/10.1038/s41698-026-01316-1
Schlüsselwörter: Brustkrebs, Tumormechanik, digitaler Zwilling, Tumormikroumgebung, computationale Onkologie