Clear Sky Science · fr
Développement d’une physiologie virtuelle des tissus tumoraux humains pour l’évaluation de la malignité
Pourquoi presser les tumeurs compte
Quand on pense au cancer, on imagine généralement des cellules malignes qui prolifèrent de façon incontrôlée. Mais les tumeurs sont aussi des objets physiques qui poussent, tirent et compriment les tissus qui les entourent. Ces forces invisibles peuvent contribuer à déterminer si une tumeur reste relativement contenue ou devient menaçante et difficile à traiter. Cette étude construit un « jumeau virtuel » détaillé d’échantillons tumoraux mammaires humains réels pour mesurer comment les contraintes à l’intérieur du tissu se rapportent au potentiel de dangerosité d’une tumeur — sans avoir besoin d’expérimenter directement sur les patients.
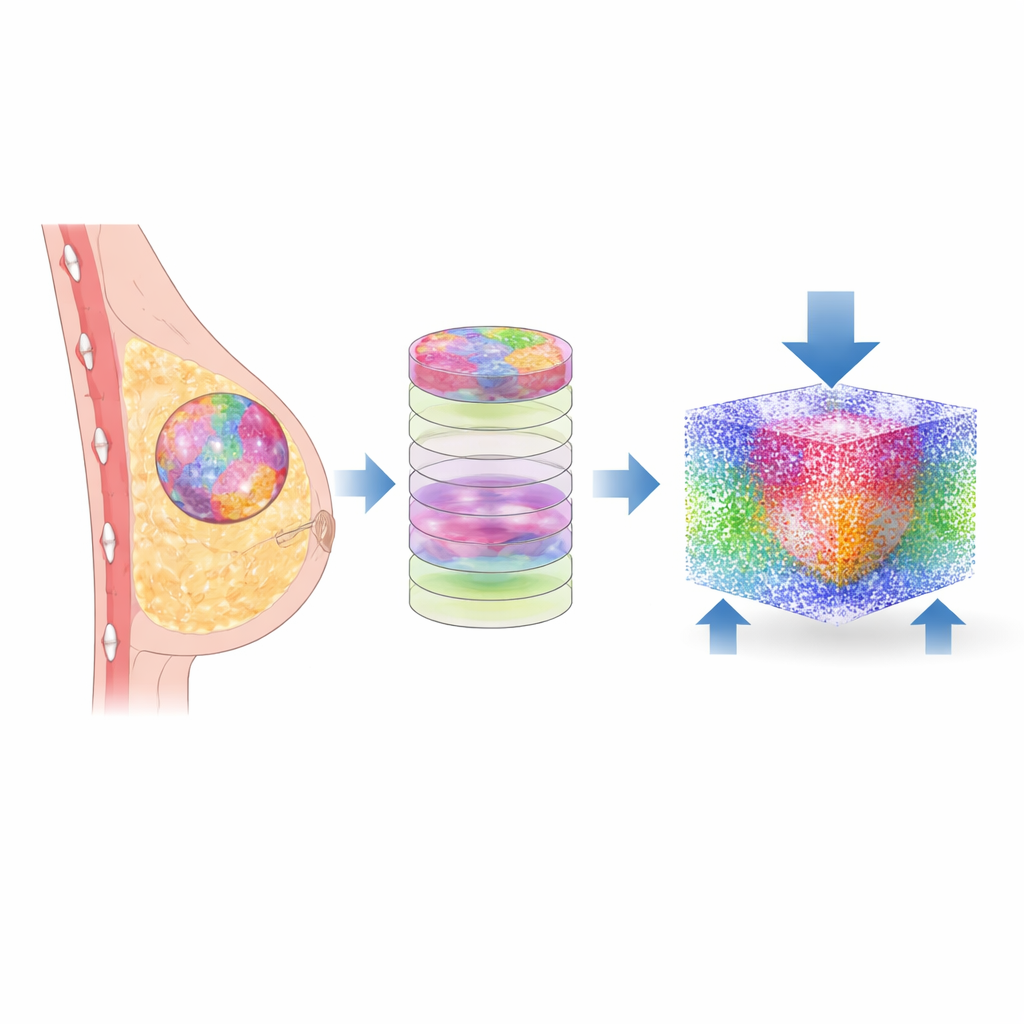
D’une lame de biopsie à un jumeau numérique
Les chercheurs ont commencé par de petites biopsies de tissu mammaire semblables à celles examinées quotidiennement par les pathologistes. Plutôt que de se limiter aux colorations traditionnelles, ils ont utilisé la microscopie par transformée de Fourier infrarouge (FTIR), qui lit les empreintes chimiques des tissus. Grâce à l’apprentissage automatique, chaque pixel de l’image a été classé dans l’un des six composants : cellules malignes, cellules non cancéreuses, plusieurs types de tissu de soutien (stroma) et d’autres éléments. Un logiciel personnalisé a ensuite converti ces images plates en couches empilées, construisant une carte tridimensionnelle du tissu de chaque patient, en préservant exactement la mosaïque complexe des différentes régions telle qu’observée dans l’échantillon réel.
Transformer le tissu en physique
Pour explorer le comportement de ces structures sous charge, l’équipe a traduit les cartes 3D en un modèle informatique à base de particules. Chaque petit fragment de tissu était représenté par des particules interagissantes dotées de propriétés mécaniques — comme la rigidité et la densité — tirées de mesures antérieures sur le tissu mammaire. En utilisant une méthode appelée hydrodynamique des particules lissées, ils ont simulé ce qui se passe quand une pression douce, physiologiquement réaliste, est appliquée d’un côté du tissu tandis que le côté opposé est maintenu fixe. Cela leur a permis de calculer comment les contraintes et les déformations — combien le tissu est comprimé et déformé — se propagent à travers chaque composant de douze échantillons différents de patients.
Ce que les tumeurs virtuelles ont révélé
Les simulations ont montré que les tumeurs ne sont pas soumises aux mêmes contraintes partout. Les échantillons dans lesquels les zones malignes étaient fragmentées en nombreuses petites îles dispersées subissaient des contraintes locales beaucoup plus élevées que les tumeurs où les zones malignes formaient des plaques plus grandes et continues. Le même schéma apparaissait pour les types de tissus environnants : de petits îlots déconnectés de n’importe quel composant supportaient en général des charges plus importantes que de larges régions continues. Le voisinage importait aussi. Lorsqu’une région rigide jouxtait une région beaucoup plus souple, les deux subissaient des contraintes accrues, alors que des amas entourés de tissus de rigidité similaire étaient moins sollicités. Dans certains cas, même des échantillons classés comme normaux mais présentant une structure très mélangée, en mosaïque, montraient des niveaux de contrainte comparables à des tissus nettement malins.
Des forces qui peuvent pousser le tissu vers le cancer
Ces contraintes internes n’étaient pas de simples ondulations. Dans les tissus les plus hétérogènes, les contraintes de compression prédites atteignaient des niveaux que des expériences antérieures ont montré capables d’inciter des cellules saines à adopter un comportement malin en modifiant leur croissance, leur mobilité ou leur mort. Les zones plus rigides et malignes avaient tendance à se déformer moins que leurs voisines plus souples, mais elles contribuaient à concentrer la contrainte dans les composants adjacents. Le modèle a également suivi comment les surfaces des différentes régions tissulaires évoluaient dans le temps, révélant que les petits composants déconnectés ressentaient non seulement des contraintes plus élevées, mais subissaient aussi des changements de forme plus importants, ce qui pourrait perturber encore davantage l’environnement local.
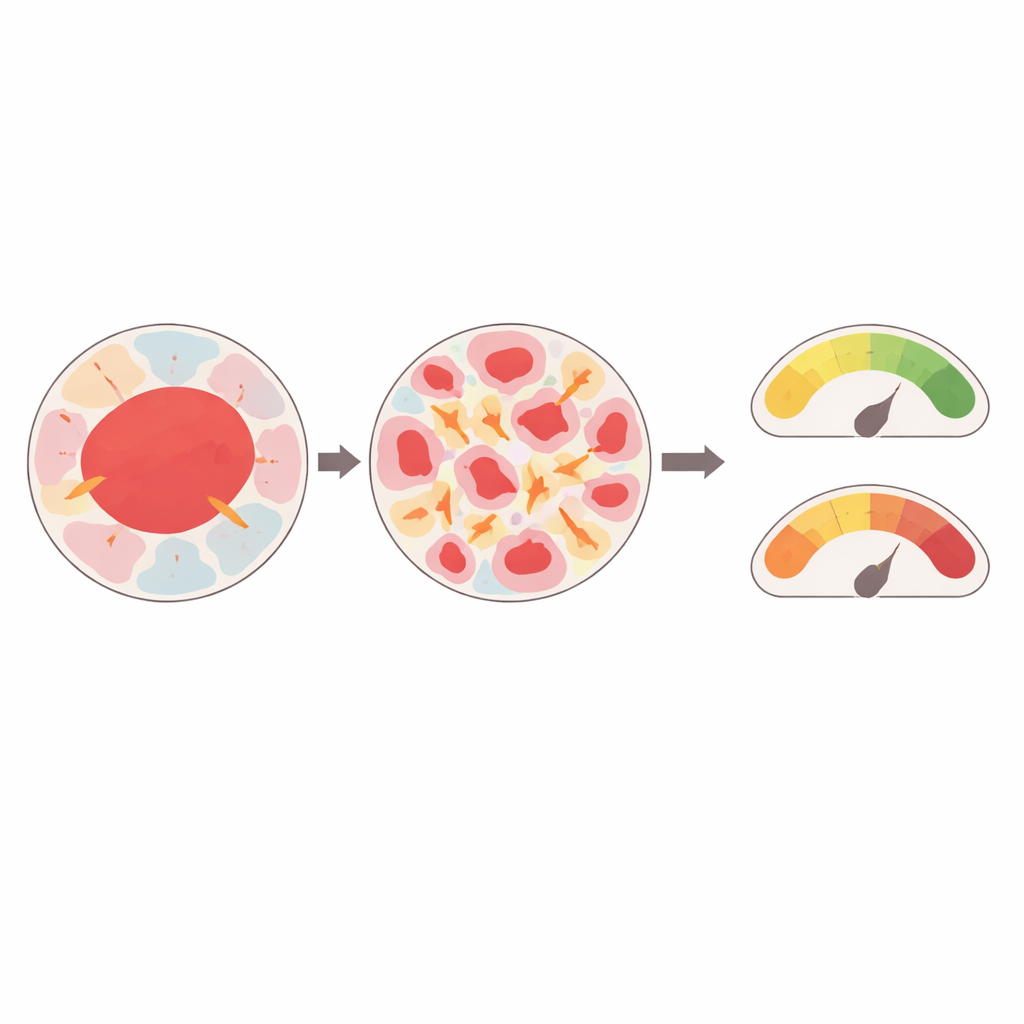
Vers des empreintes mécaniques personnalisées des tumeurs
En reliant des images de biopsies réelles à des simulations physiques détaillées, l’étude fournit un proof‑of‑concept de « physiologie virtuelle » pour les tumeurs mammaires. Elle suggère que la façon dont une tumeur est constituée — sa fragmentation, la taille de chaque région et les tissus en contact — façonne fortement les forces mécaniques qui s’exercent en son sein. Ces forces, à leur tour, se situent dans des plages connues pour favoriser la transformation maligne et la résistance aux thérapies. À l’avenir, des jumeaux numériques similaires pourraient aider à signaler des tissus apparemment normaux mais mécaniquement stressés et à risque de devenir cancéreux, ou guider les médecins vers des plans de traitement adaptés à l’empreinte mécanique unique d’une tumeur ainsi qu’à sa génétique.
Citation: Arbabi, S., Vincent, H., Hansen, E. et al. Developing virtual physiology of human tumor tissue for malignancy assessment. npj Precis. Onc. 10, 136 (2026). https://doi.org/10.1038/s41698-026-01316-1
Mots-clés: cancer du sein, mécanique des tumeurs, jumeau numérique, microenvironnement tumoral, oncologie computationnelle