Clear Sky Science · pt
Análise de célula única e multi-ômica identifica biomarcadores e alvos terapêuticos relacionados à mitofagia no acidente vascular isquêmico
Por que as baterias celulares danificadas importam no AVC
O AVC costuma ser descrito como um problema de vasos sanguíneos entupidos, mas o que ocorre dentro das células cerebrais após a interrupção do fluxo sanguíneo pode ser igualmente importante. Este estudo examina as "usinas de energia" da célula — as mitocôndrias — e um processo de limpeza embutido chamado mitofagia, que remove as mitocôndrias danificadas. Ao acompanhar como esse sistema de limpeza se comporta no AVC e quais genes o controlam, os pesquisadores buscam novas formas de prever quem corre risco de desfechos piores e de conceber tratamentos que protejam as células cerebrais quando cada minuto conta.
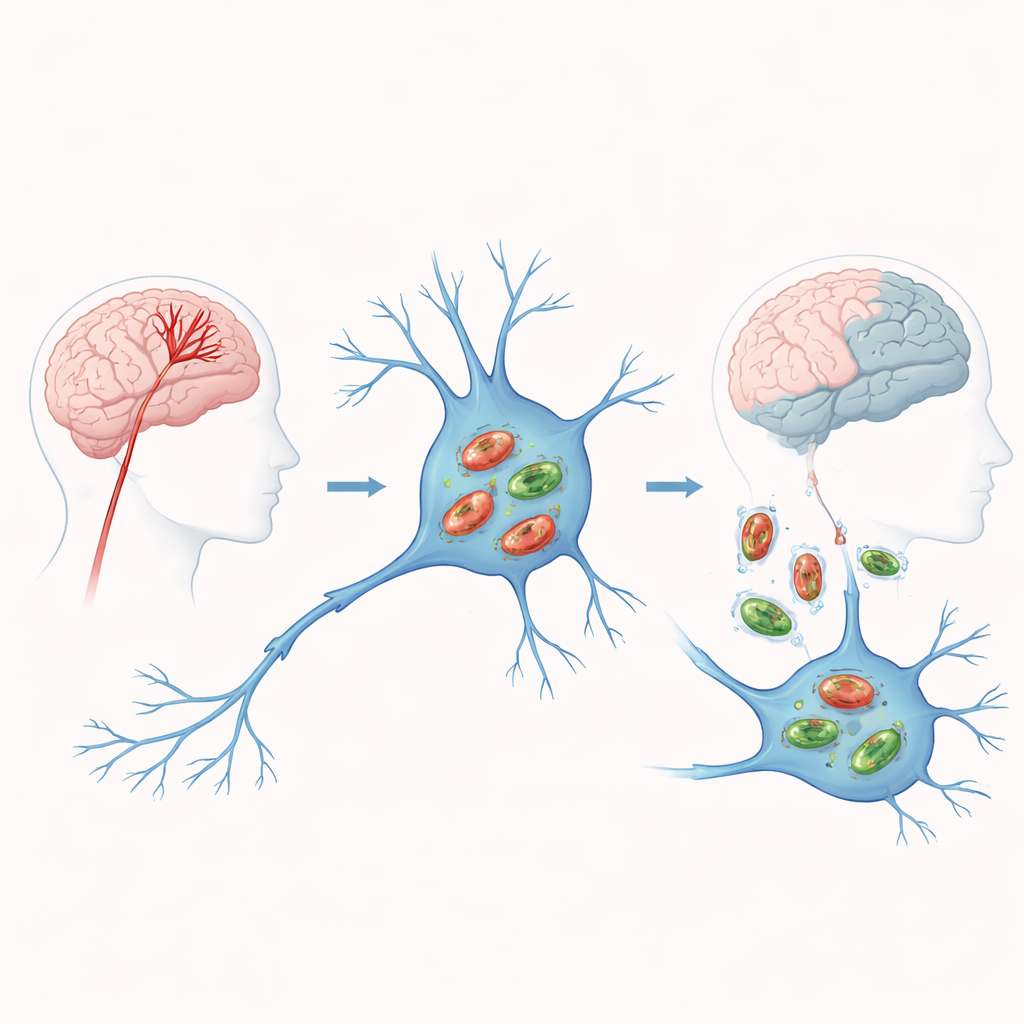
Quando o sangue para, a energia falha nas células cerebrais
Num AVC isquêmico, uma artéria bloqueada corta o fornecimento de oxigênio e nutrientes a parte do cérebro. Sem combustível, as mitocôndrias falham: produzem menos energia e liberam subprodutos tóxicos que lesionam as células e as empurram rumo à morte. A mitofagia é a resposta de emergência da célula, marcando mitocôndrias defeituosas e enviando‑as para degradação e reciclagem. Em teoria, uma limpeza oportuna evita o acúmulo de toxinas e limita os danos. Mas se esse processo for fraco demais ou excessivo, pode permitir que mitocôndrias disfuncionais persistam ou remover demais os geradores de energia de que as células precisam para sobreviver. Compreender onde os pacientes com AVC estão nesse ponto crítico é central para o estudo.
Minerando grandes bases de dados para encontrar sinais de alerta no sangue
A equipe combinou vários grandes conjuntos de dados de expressão gênica de pacientes com AVC e de indivíduos saudáveis, e então concentrou‑se em um painel de genes já associados à mitofagia. Usando estatística avançada e múltiplos modelos de aprendizado de máquina, buscaram padrões que melhor distinguissem amostras de AVC das não‑AVC. Encontraram dezenove genes relacionados à mitofagia que mudaram no AVC e que formaram dois grandes grupos de pacientes com características moleculares e imunes distintas. Uma análise de rede mais profunda destacou um aglomerado denso de genes ligados à função mitocondrial e à produção de proteínas, sugerindo que o suprimento de energia e a atividade da "fábrica" celular estão intimamente entrelaçados no AVC.
Cinco pistas genéticas-chave e a conexão com o sistema imune
A partir dessa rede, os pesquisadores treinaram e compararam oito modelos preditivos, refinando até identificar cinco genes de destaque — SRPRB, ATP5J, LSM7, DEGS1 e TGDS — como marcadores centrais. Um teste combinado de cinco genes separou com precisão as amostras de AVC das de controle nos dados deles. Experimentos de laboratório usando um modelo celular de privação de oxigênio e glicose e sangue de pacientes com AVC confirmaram que esses genes realmente se alteram em sistemas biológicos reais, não apenas em análises computacionais. Vários deles estão ligados a como as mitocôndrias produzem energia, a como as células processam lipídios e a como as mensagens genéticas são tratadas. O estudo também mostrou que esses marcadores estão fortemente associados a certos tipos celulares e vias imunes, sugerindo que a resposta imune após o AVC está intimamente acoplada à saúde mitocondrial e a processos de coagulação.
Focando nos defensores cerebrais chamados microglia
Como amostras sanguíneas não capturam totalmente o que ocorre dentro do cérebro, a equipe recorreu a dados de célula única de um modelo murino de AVC. Eles examinaram milhares de células cerebrais individuais e identificaram grupos distintos, com foco nas microglias, as células imunes residentes do cérebro. Após o AVC, as microglias mudaram de um estado calmo e vigilante para estados inflamatórios e associados à doença. Essas microglias "ativadas" exibiram atividade de mitofagia muito maior, consistente com um forte esforço para limpar mitocôndrias danificadas. Um dos cinco genes-chave, ATP5J, mostrou um aumento dinâmico ao longo da progressão do estado de repouso para microglias associadas à doença, ressaltando seu papel potencial tanto como marcador quanto como regulador da resposta dessas células ao dano.
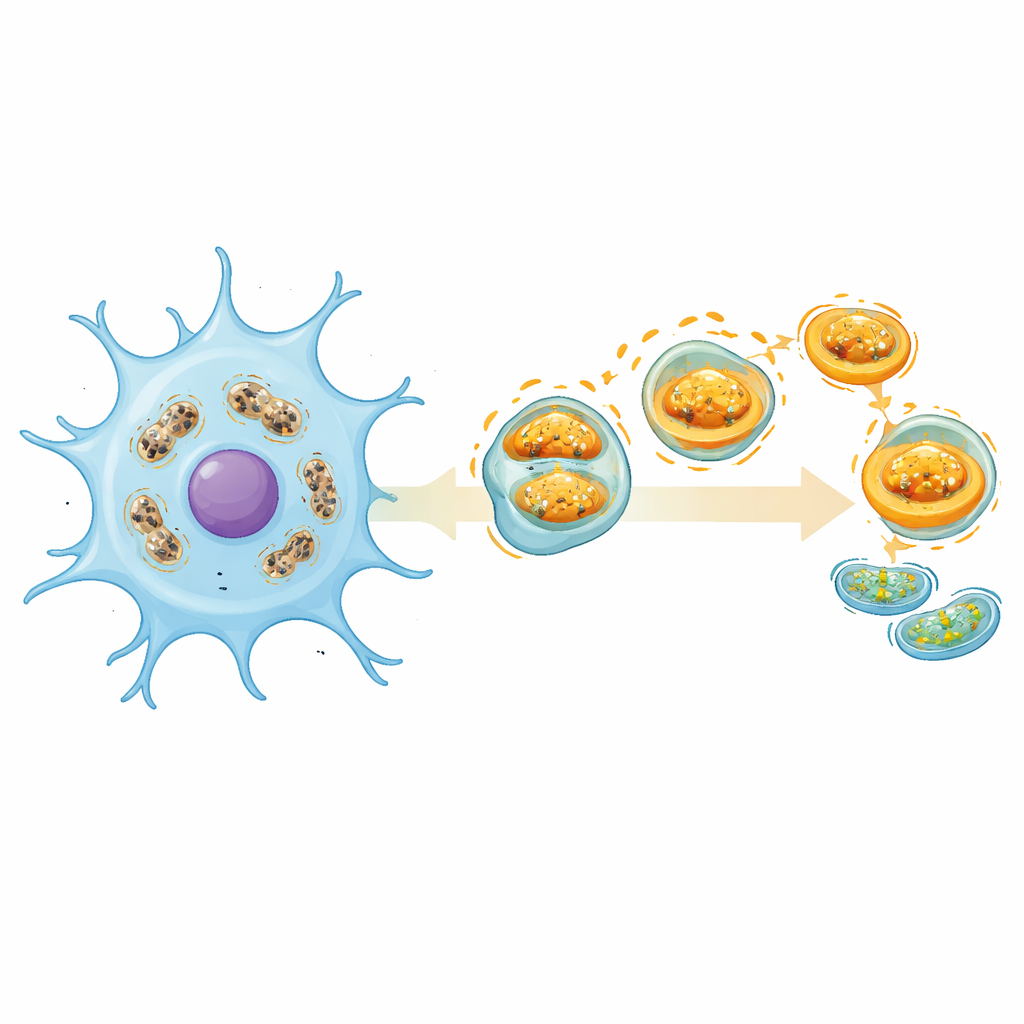
O que isso pode significar para o cuidado futuro do AVC
Em conjunto, o trabalho retrata a mitofagia não como simplesmente boa ou ruim, mas como uma resposta finamente ajustada que difere entre tipos celulares, estágios da doença e compartimentos do corpo, como sangue versus tecido cerebral. Os cinco genes destacados — especialmente ATP5J — oferecem pontos de partida promissores para testes baseados em sangue que possam classificar melhor pacientes com AVC e, eventualmente, orientar terapias que direcionem a limpeza mitocondrial para uma "zona ideal" protetora. Embora sejam necessários mais experimentos em modelos celulares cerebrais apropriados e em grupos maiores de pacientes, o estudo sugere que resgatar o cérebro no AVC pode depender tanto de reparar seus sistemas microscópicos de energia quanto de reabrir artérias bloqueadas.
Citação: Cao, Z., Wang, Y., Sun, M. et al. Single-cell and multi-omics analysis identifies mitophagy-related biomarkers and therapeutic targets in ischemic stroke. Sci Rep 16, 12433 (2026). https://doi.org/10.1038/s41598-026-43377-z
Palavras-chave: acidente vascular isquêmico, mitofagia, mitocôndrias, microglia, biomarcadores