Clear Sky Science · pl
Analiza jednowątkowa i multi‑omics identyfikuje markery związane z mitofagią oraz cele terapeutyczne w udarze niedokrwiennym
Dlaczego uszkodzone „baterie” komórek mają znaczenie w udarze
Udar zwykle opisuje się jako problem zatkanych naczyń krwionośnych, ale równie ważne może być to, co dzieje się wewnątrz komórek mózgu po ustaniu przepływu krwi. Badanie to koncentruje się na „elektrowniach” komórki – mitochondriach – oraz na wbudowanym mechanizmie oczyszczania zwanym mitofagią, który usuwa uszkodzone organelle. Śledząc zachowanie tego systemu oczyszczania w udarze oraz geny go kontrolujące, autorzy chcą znaleźć nowe sposoby przewidywania, u kogo wystąpią gorsze rokowania, oraz zaprojektować terapie chroniące komórki mózgu, gdy każda minuta ma znaczenie.
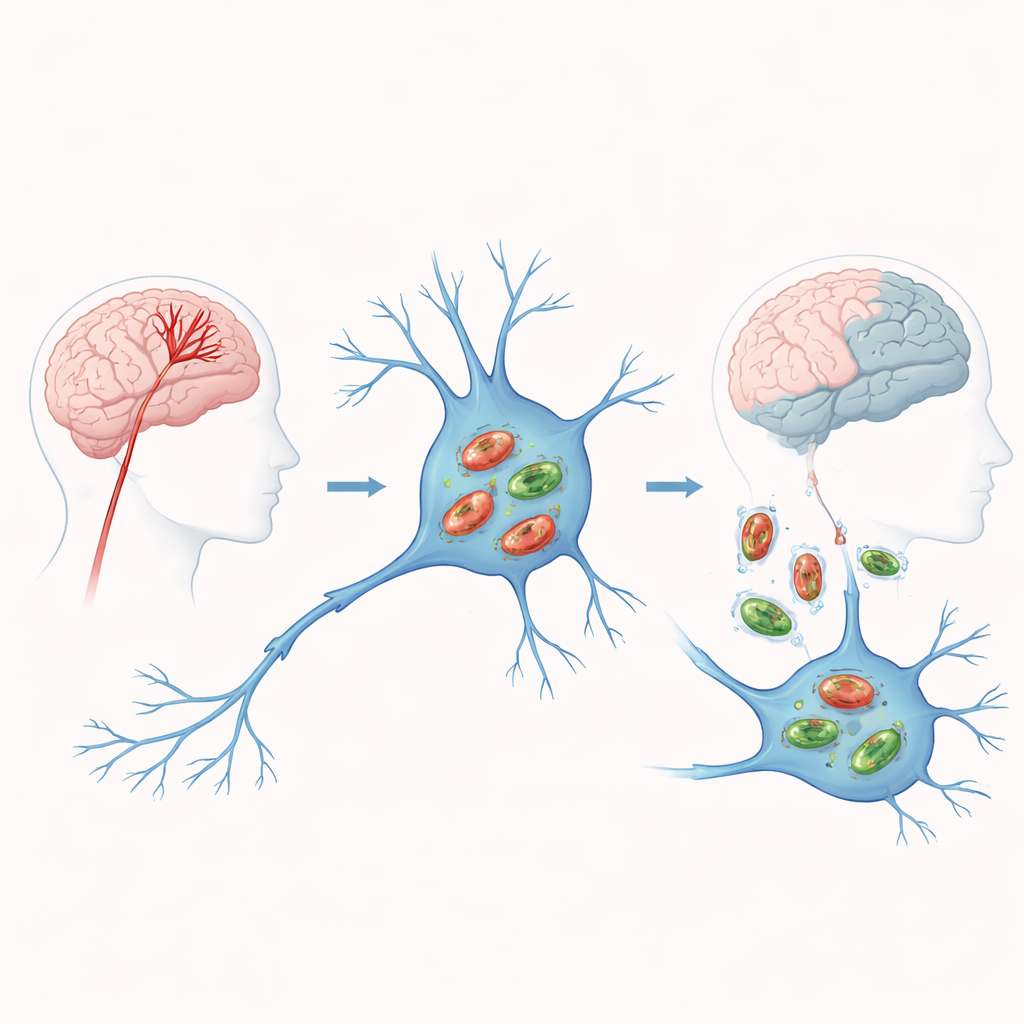
Gdy krew przestaje płynąć, w komórkach mózgu gaśnie zasilanie
W udarze niedokrwiennym zatkana tętnica odcina dopływ tlenu i składników odżywczych do części mózgu. Bez paliwa mitochondria zawodzą: wytwarzają mniej energii i uwalniają szkodliwe produkty uboczne, które uszkadzają komórki i popychają je w stronę śmierci. Mitofagia to awaryjna reakcja komórki, oznaczająca wadliwe mitochondria i kierująca je do rozkładu i recyklingu. W teorii terminowe oczyszczanie zapobiega gromadzeniu się toksyn i ogranicza uszkodzenia. Jednak gdy proces ten jest zbyt słaby lub zbyt silny, może albo pozwolić na zaleganie niesprawnych mitochondriów, albo pozbawić komórkę potrzebnych producentów energii. Zrozumienie, gdzie pacjenci z udarem znajdują się na tym ostrzu noża, jest kluczowe dla badania.
Kopalnia dużych danych w poszukiwaniu sygnałów ostrzegawczych we krwi
Zespół połączył kilka dużych zestawów danych ekspresji genów od pacjentów z udarem i osób zdrowych, a następnie skupił się na panelu genów powiązanych już z mitofagią. Przy użyciu zaawansowanej statystyki i wielu modeli uczenia maszynowego poszukiwano wzorców najlepiej rozróżniających próbki z udarem od kontrolnych. Wykryto dziewiętnaście genów związanych z mitofagią, które ulegały zmianie w udarze i tworzyły dwie główne grupy pacjentów o odmiennych cechach molekularnych i immunologicznych. Głębsza analiza sieciowa uwypukliła jedną gęstą grupę genów związaną z funkcją mitochondrialną i produkcją białek, sugerując, że zaopatrzenie w energię i aktywność „fabryki” komórkowej są ściśle powiązane w udarze.
Pięć kluczowych genetycznych wskazówek i związek z odpornością
Z tej sieci badacze wytrenowali i porównali osiem modeli predykcyjnych, ostatecznie wyłaniając pięć wyróżniających się genów — SRPRB, ATP5J, LSM7, DEGS1 i TGDS — jako rdzenne markery. Test oparty na tych pięciu genach skutecznie oddzielał próbki z udarem od kontrolnych w dostępnych danych. Eksperymenty laboratoryjne z użyciem modelu komórkowego niedoboru tlenu i glukozy oraz próbek krwi od pacjentów z udarem potwierdziły, że te geny rzeczywiście zmieniają ekspresję w systemach biologicznych, a nie tylko w analizie komputerowej. Kilka z nich wiąże się z produkcją energii w mitochondriach, metabolizmem lipidów oraz przetwarzaniem informacji genetycznej. Badanie wykazało także silne powiązania tych markerów z określonymi komórkami i szlakami układu odpornościowego, co sugeruje, że reakcja immunologiczna po udarze jest ściśle sprzężona ze zdrowiem mitochondriów i procesami krzepnięcia krwi.
Zbliżenie na obrońców mózgu — mikroglej
Ponieważ próbki krwi nie oddają w pełni tego, co dzieje się wewnątrz mózgu, zespół sięgnął po dane jednowątkowe z mysiego modelu udaru. Przeanalizowano tysiące pojedynczych komórek mózgu i zidentyfikowano odrębne populacje, koncentrując się na mikrogleju — rezydujących w mózgu komórkach odpornościowych. Po udarze mikroglej przeszedł z uspokojonego, czuwającego stanu w kierunku stanów zapalnych i związanych z chorobą. Te „aktywowane” komórki mikrogleju wykazywały znacznie wyższą aktywność mitofagii, co jest zgodne z intensywnym wysiłkiem usuwania uszkodzonych mitochondriów. Jeden z pięciu kluczowych genów, ATP5J, wykazywał dynamiczny wzrost w trakcie przejścia od stanu spoczynkowego do stanów powiązanych z chorobą, podkreślając jego potencjalną rolę zarówno jako markera, jak i regulatora reakcji tych komórek na uraz.
Co to może znaczyć dla przyszłej opieki nad pacjentami z udarem
W sumie praca przedstawia mitofagię nie jako coś jednoznacznie dobrego lub złego, lecz jako precyzyjnie wyregulowaną reakcję różniącą się między typami komórek, etapami choroby i przedziałami organizmu, takimi jak krew kontra tkanka mózgowa. Pięć wyróżnionych genów — szczególnie ATP5J — stanowi obiecujący punkt wyjścia do testów opartych na krwi, które mogłyby lepiej klasyfikować pacjentów z udarem i w przyszłości kierować terapiami przesuwającymi mitochondrialne oczyszczanie w stronę ochronnego „złotego środka”. Chociaż potrzebne są dalsze eksperymenty w odpowiednich modelach komórek mózgowych i większych grupach pacjentów, badanie sugeruje, że ratowanie mózgu w udarze może zależeć nie tylko od przywrócenia przepływu krwi, ale równie mocno od naprawy jego mikroskopijnych systemów zasilania.
Cytowanie: Cao, Z., Wang, Y., Sun, M. et al. Single-cell and multi-omics analysis identifies mitophagy-related biomarkers and therapeutic targets in ischemic stroke. Sci Rep 16, 12433 (2026). https://doi.org/10.1038/s41598-026-43377-z
Słowa kluczowe: udar niedokrwienny, mitofagia, mitochondria, mikroglej, markery