Clear Sky Science · de
Einzelzell- und Multi‑Omics-Analyse identifiziert mitophagie‑bezogene Biomarker und therapeutische Ziele beim ischämischen Schlaganfall
Warum beschädigte Zellbatterien beim Schlaganfall zählen
Schlaganfall wird oft als Problem verstopfter Blutgefäße beschrieben, doch ebenso wichtig ist, was in den Gehirnzellen passiert, nachdem die Durchblutung aussetzt. Diese Studie untersucht die „Kraftwerke“ der Zelle – die Mitochondrien – und einen eingebauten Reinigungsprozess, die Mitophagie, die beschädigte Mitochondrien entfernt. Indem sie verfolgen, wie dieses Reinigungssystem beim Schlaganfall reagiert und welche Gene es steuern, wollen die Forschenden Wege finden, besser vorherzusagen, wer ein erhöhtes Risiko für ungünstige Verläufe hat, und Behandlungen zu entwickeln, die Gehirnzellen schützen, wenn jede Minute zählt.
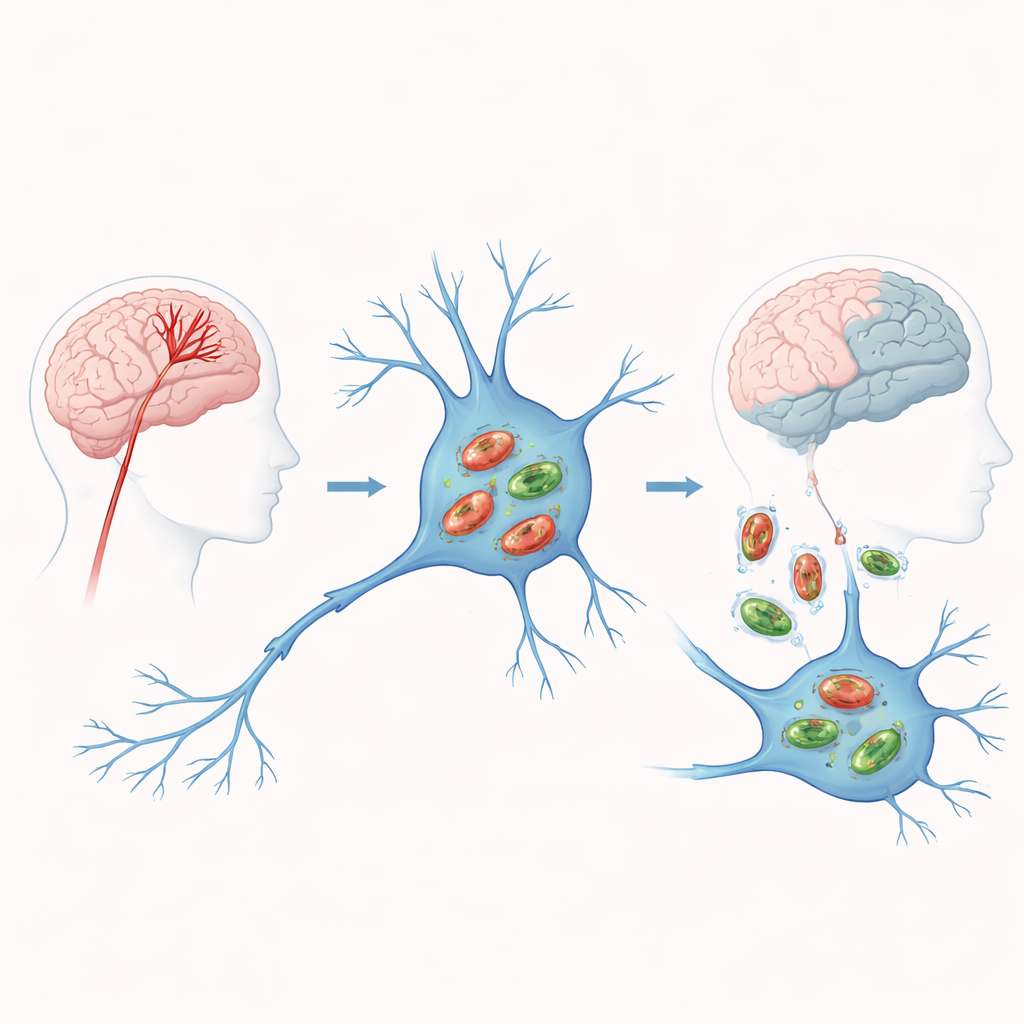
Wenn das Blut aufhört zu fließen, versagt die Energie in Gehirnzellen
Bei einem ischämischen Schlaganfall unterbricht ein verschlossenes Gefäß die Versorgung eines Gehirnbereichs mit Sauerstoff und Nährstoffen. Ohne Treibstoff geraten Mitochondrien in Bedrängnis: sie produzieren weniger Energie und setzen schädliche Nebenprodukte frei, die Zellen verletzen und in Richtung Zelltod treiben. Mitophagie ist die Notfallantwort der Zelle, bei der defekte Mitochondrien markiert und zum Abbau sowie Recycling weitergeleitet werden. Theoretisch verhindert rechtzeitige Reinigung schädliche Anhäufungen und begrenzt den Schaden. Ist dieser Prozess jedoch zu schwach oder zu stark, können entweder funktionsgestörte Mitochondrien bestehen bleiben oder Zellen ihrer benötigten Energiequellen beraubt werden. Zu verstehen, wo sich Schlaganfallpatienten auf diesem schmalen Grat befinden, ist zentral für die Studie.
Große Daten nach Warnsignalen durchsuchen — im Blut
Das Team kombinierte mehrere große Genexpressionsdatensätze von Schlaganfallpatienten und gesunden Kontrollen und konzentrierte sich dann auf ein Set von Genen, die bereits mit Mitophagie in Verbindung stehen. Mithilfe fortgeschrittener Statistik und mehrerer maschineller Lernmodelle suchten sie nach Mustern, die Schlaganfall‑ und Nicht‑Schlaganfallproben am besten unterscheiden. Sie fanden neunzehn mitophagie‑bezogene Gene, die sich beim Schlaganfall veränderten, und identifizierten zwei Hauptpatientengruppen mit unterschiedlichen molekularen und immunologischen Merkmalen. Eine vertiefte Netzwerk‑Analyse hob einen dichten Gencluster hervor, der mit mitochondrialer Funktion und Proteinproduktion verknüpft ist, was darauf hindeutet, dass Energieversorgung und zelluläre „Fabrikaktivität“ beim Schlaganfall eng miteinander verflochten sind.
Fünf zentrale genetische Hinweise und die Verbindung zum Immunsystem
Aus diesem Netzwerk trainierten und verglichen die Forschenden acht Vorhersagemodelle und konzentrierten sich schließlich auf fünf herausragende Gene — SRPRB, ATP5J, LSM7, DEGS1 und TGDS — als Kernmarker. Ein kombinierter Fünf‑Gen‑Test trennte Schlaganfall‑ von Kontrollproben in ihren Datensätzen zuverlässig. Laborversuche mit einem Zellmodell der Sauerstoff‑Glukose‑Entbehrung sowie Blutproben von Schlaganfallpatienten bestätigten, dass sich diese Gene in realen biologischen Systemen tatsächlich verändern und nicht nur in der Datenanalyse. Mehrere dieser Gene sind mit der Energieproduktion der Mitochondrien, dem Fettstoffwechsel und der Verarbeitung genetischer Botschaften verbunden. Die Studie zeigte außerdem, dass diese Marker stark mit bestimmten Immunzellen und Signalwegen korrelieren, was nahelegt, dass die Immunantwort nach Schlaganfall eng mit mitochondrialer Gesundheit und Gerinnungsprozessen verknüpft ist.
Fokus auf die Hirnverteidiger: Microglia
Da Blutproben nicht vollständig abbilden, was im Gehirn geschieht, nutzte das Team Einzelzell‑Daten aus einem Mausmodell des Schlaganfalls. Sie untersuchten Tausende einzelner Gehirnzellen und identifizierten verschiedene Zellgruppen, wobei der Fokus auf Microglia lag, den residenten Immunzellen des Gehirns. Nach dem Schlaganfall wandelten sich Microglia von einem ruhigen, beobachtenden Zustand in entzündliche und krankheitsassoziierte Zustände. Diese „aktivierten“ Microglia zeigten deutlich erhöhte Mitophagie‑Aktivität, was auf einen starken Drang zur Beseitigung beschädigter Mitochondrien hindeutet. Eines der fünf Schlüsselgene, ATP5J, stieg dynamisch entlang der Progression vom ruhenden hin zum krankheitsassoziierten Microglia‑Zustand an und unterstreicht damit seine potenzielle Rolle als Marker und Regulator der Reaktion dieser Zellen auf Verletzung.
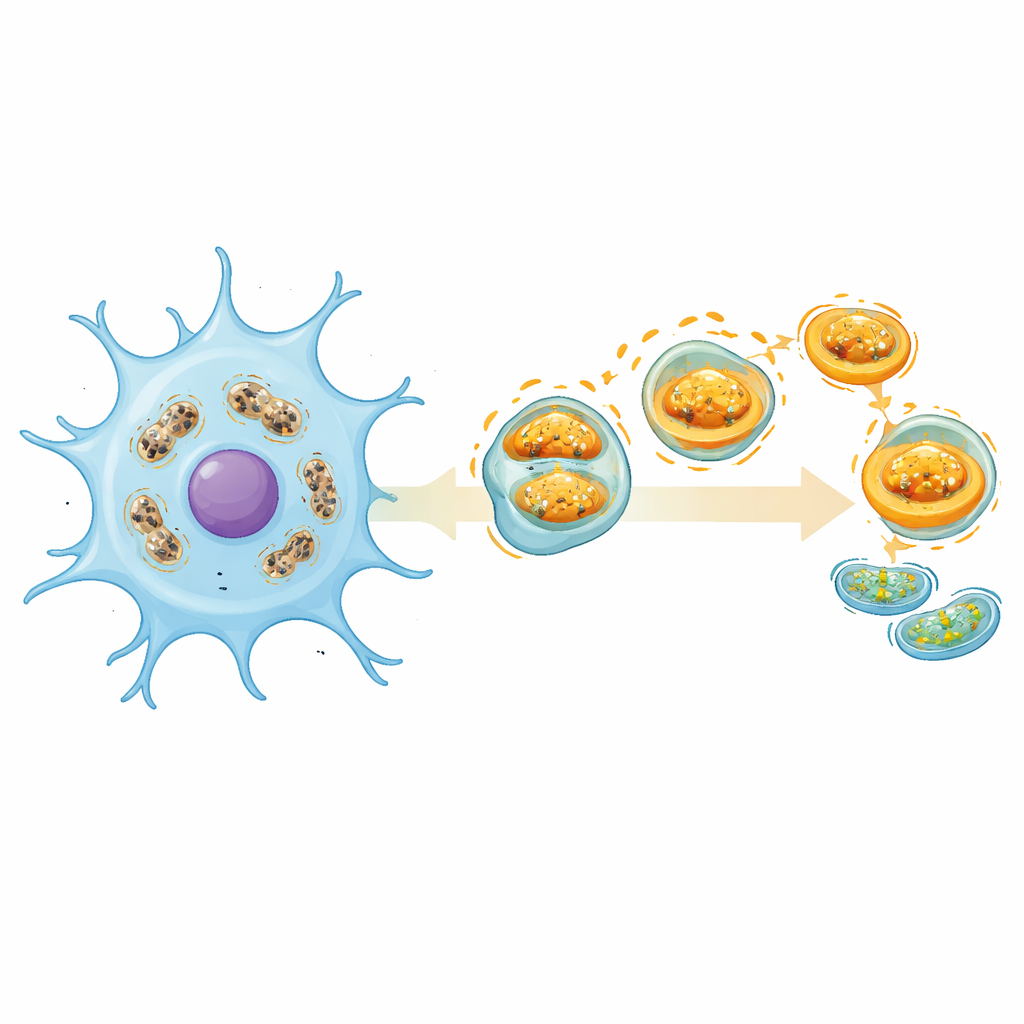
Was das für die zukünftige Schlaganfallversorgung bedeuten könnte
In der Summe zeichnet die Arbeit das Bild von Mitophagie nicht als einfach gut oder schlecht, sondern als fein abgestimmte Reaktion, die je nach Zelltyp, Krankheitsstadium und Körperkompartiment—etwa Blut versus Hirngewebe—variiert. Die fünf hervorgehobenen Gene—insbesondere ATP5J—bieten vielversprechende Ansatzpunkte für blutbasierte Tests, die Schlaganfallpatienten besser klassifizieren und langfristig Therapien lenken könnten, die die mitochondriale Reinigung in eine schützende „Sweetspot“-Zone verschieben. Obwohl weitere Experimente in geeigneten Hirnzellmodellen und größeren Patientengruppen erforderlich sind, legt die Studie nahe, dass die Rettung des Gehirns beim Schlaganfall ebenso sehr davon abhängen könnte, seine mikroskopischen Energiesysteme zu reparieren wie blockierte Arterien wieder zu öffnen.
Zitation: Cao, Z., Wang, Y., Sun, M. et al. Single-cell and multi-omics analysis identifies mitophagy-related biomarkers and therapeutic targets in ischemic stroke. Sci Rep 16, 12433 (2026). https://doi.org/10.1038/s41598-026-43377-z
Schlüsselwörter: ischämischer Schlaganfall, Mitophagie, Mitochondrien, Microglia, Biomarker