Clear Sky Science · es
Análisis unicelular y multi-ómica identifica biomarcadores y dianas terapéuticas relacionados con la mitofagia en el ictus isquémico
Por qué importan las baterías celulares dañadas en el ictus
El ictus suele describirse como un problema de vasos sanguíneos obstruidos, pero lo que ocurre dentro de las células cerebrales después de que se interrumpe el flujo sanguíneo puede ser igual de decisivo. Este estudio examina las “centrales eléctricas” de la célula —las mitocondrias— y un proceso interno de limpieza llamado mitofagia que elimina las mitocondrias dañadas. Al seguir cómo funciona este sistema de limpieza durante el ictus y qué genes lo regulan, los investigadores pretenden encontrar nuevas formas de predecir quién tiene mayor riesgo de peores desenlaces y diseñar tratamientos que protejan las células cerebrales cuando cada minuto cuenta.
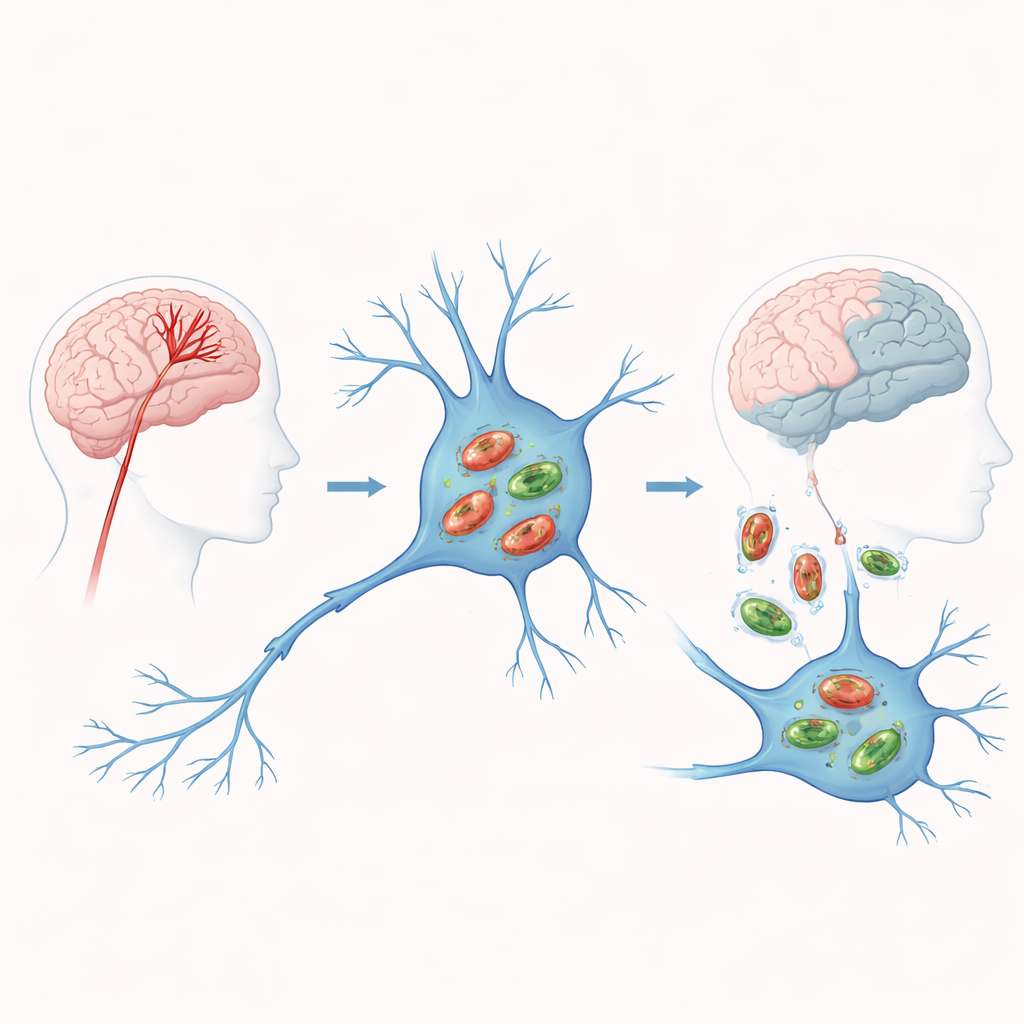
Cuando se detiene la sangre, falla la energía en las células cerebrales
En un ictus isquémico, una arteria bloqueada priva de oxígeno y nutrientes a una región del cerebro. Sin combustible, las mitocondrias flaquean: producen menos energía y liberan subproductos nocivos que lesionan las células y las empujan hacia la muerte. La mitofagia es la respuesta de emergencia de la célula, etiquetando mitocondrias defectuosas y enviándolas para su degradación y reciclaje. En teoría, una limpieza oportuna evita la acumulación de tóxicos y limita el daño. Pero si este proceso es demasiado débil o demasiado intenso, puede permitir que mitocondrias disfuncionales persistan o, por el contrario, despojar a las células de los generadores de energía que necesitan para sobrevivir. Entender en qué punto de este equilibrio se sitúan los pacientes de ictus es clave en el estudio.
Minería de grandes datos para encontrar señales de aviso en sangre
El equipo combinó varios conjuntos de datos de expresión génica de gran tamaño procedentes de pacientes con ictus y personas sanas, y se centró en un panel de genes ya vinculados con la mitofagia. Usando estadísticas avanzadas y múltiples modelos de aprendizaje automático, buscaron patrones que distinguieran mejor las muestras de ictus de las de no-ictus. Identificaron diecinueve genes relacionados con la mitofagia que cambiaron en el ictus y formaron dos grupos principales de pacientes con características moleculares e inmunitarias diferentes. Un análisis de red más profundo destacó un cúmulo denso de genes asociados a la función mitocondrial y a la producción de proteínas, lo que sugiere que el suministro de energía y la actividad de la “fábrica” celular están estrechamente entrelazados en el ictus.
Cinco pistas genéticas clave y la conexión inmune
A partir de esta red, los investigadores entrenaron y compararon ocho modelos predictivos, centrando finalmente la atención en cinco genes destacados —SRPRB, ATP5J, LSM7, DEGS1 y TGDS— como marcadores principales. Una prueba combinada de cinco genes separó con precisión las muestras de ictus de las de control en sus datos. Experimentos de laboratorio con un modelo celular de privación de oxígeno y glucosa y con sangre de pacientes con ictus confirmaron que estos genes realmente cambian en sistemas biológicos reales, no solo en análisis informáticos. Varios de ellos están vinculados a la producción de energía mitocondrial, al manejo de lípidos y al procesamiento de mensajes genéticos. El estudio también mostró que estos marcadores están fuertemente asociados a ciertos tipos de células inmunitarias y rutas inmunes, lo que insinúa que la reacción del sistema inmune tras el ictus está estrechamente ligada a la salud mitocondrial y a los procesos de coagulación sanguínea.
Acercándose a los defensores del cerebro llamados microglía
Dado que las muestras de sangre no capturan completamente lo que ocurre dentro del cerebro, el equipo recurrió a datos unicelulares procedentes de un modelo murino de ictus. Examinaron miles de células cerebrales individuales e identificaron grupos distintos, centrando su atención en la microglía, las células inmunitarias residentes del cerebro. Tras el ictus, la microglía pasó de un estado tranquilo y vigilante a estados inflamatorios y asociados a la enfermedad. Estas microglías “activadas” mostraron una actividad de mitofagia mucho mayor, coherente con un fuerte impulso para eliminar mitocondrias dañadas. Uno de los cinco genes clave, ATP5J, mostró un incremento dinámico a lo largo de la progresión desde microglía en reposo hasta microglía asociada a la enfermedad, subrayando su potencial papel tanto como marcador como regulador de la respuesta de estas células al daño.
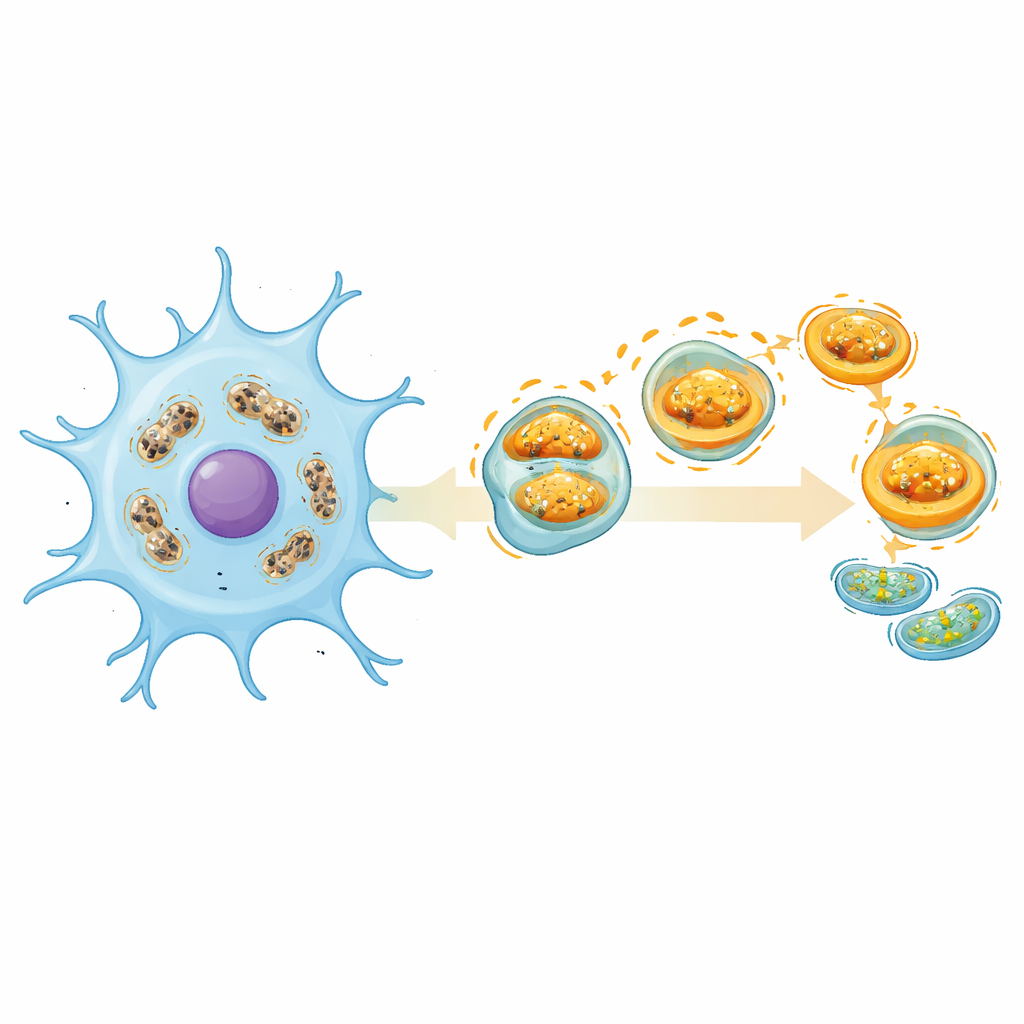
Qué podría significar esto para la atención futura del ictus
En conjunto, el trabajo presenta la mitofagia no como algo simplemente bueno o malo, sino como una respuesta finamente ajustada que difiere entre tipos celulares, etapas de la enfermedad y compartimentos del cuerpo como sangre frente a tejido cerebral. Los cinco genes destacados —especialmente ATP5J— ofrecen puntos de partida prometedores para pruebas basadas en sangre que puedan clasificar mejor a los pacientes con ictus y, eventualmente, guiar terapias que orienten la limpieza mitocondrial hacia un “punto óptimo” protector. Aunque se necesitan más experimentos en modelos celulares cerebrales apropiados y en grupos de pacientes más amplios, el estudio sugiere que rescatar el cerebro en el ictus puede depender tanto de reparar sus sistemas microscópicos de energía como de restablecer la circulación en arterias obstruidas.
Cita: Cao, Z., Wang, Y., Sun, M. et al. Single-cell and multi-omics analysis identifies mitophagy-related biomarkers and therapeutic targets in ischemic stroke. Sci Rep 16, 12433 (2026). https://doi.org/10.1038/s41598-026-43377-z
Palabras clave: ictus isquémico, mitofagia, mitocondrias, microglía, biomarcadores