Clear Sky Science · it
Analisi single‑cell e multi‑omica identifica biomarcatori e bersagli terapeutici legati alla mitofagia nell’ictus ischemico
Perché le batterie cellulari danneggiate contano nell’ictus
L’ictus è spesso descritto come un problema di vasi sanguigni ostruiti, ma ciò che avviene all’interno delle cellule cerebrali dopo l’interruzione del flusso sanguigno può essere altrettanto cruciale. Questo studio esamina le “centrali elettriche” della cellula — i mitocondri — e un meccanismo di pulizia integrato chiamato mitofagia che rimuove quelli danneggiati. Tracciando il comportamento di questo sistema di smaltimento nell’ictus e i geni che lo regolano, i ricercatori mirano a trovare nuovi modi per prevedere chi è a rischio di esiti peggiori e progettare trattamenti che proteggano le cellule cerebrali quando ogni minuto conta.
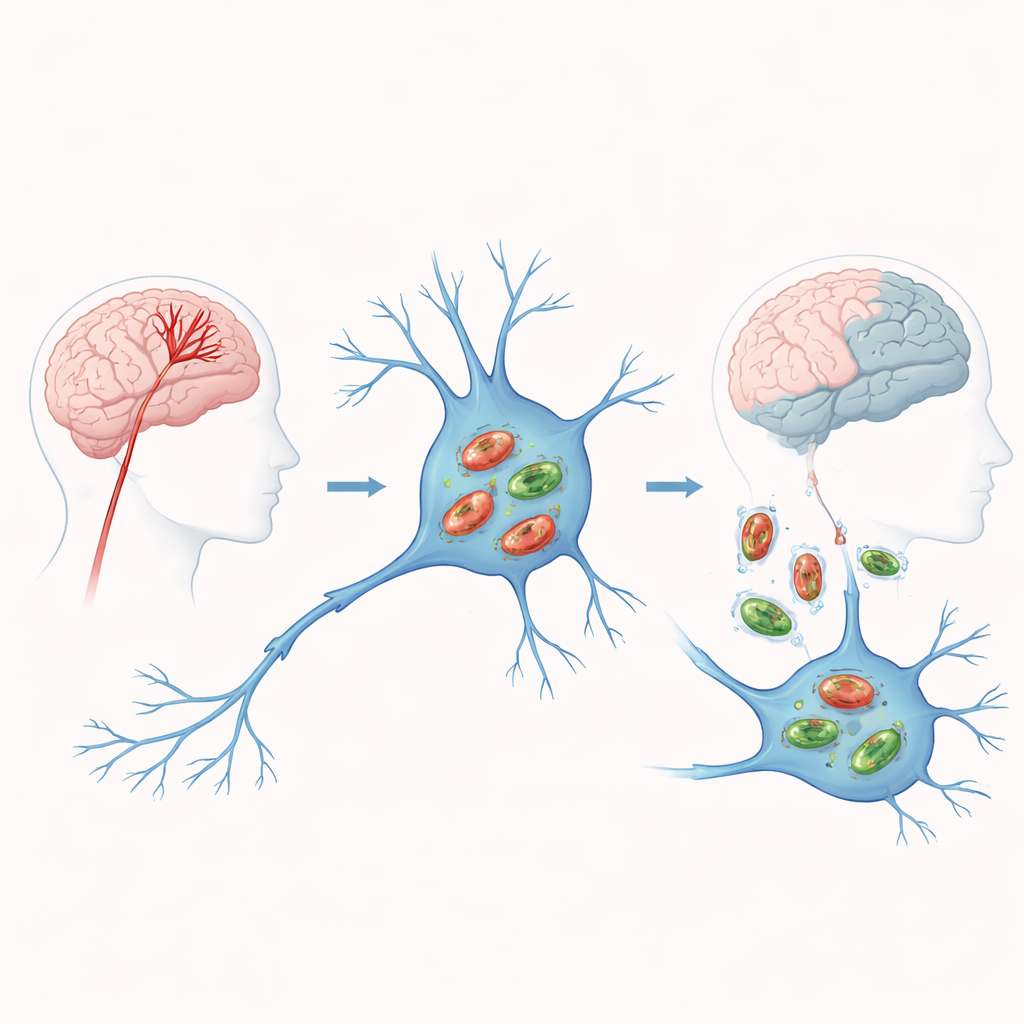
Quando il sangue si ferma, l’energia nelle cellule cerebrali viene meno
In un ictus ischemico, un’arteria ostruita interrompe l’apporto di ossigeno e nutrienti a una parte del cervello. Senza carburante, i mitocondri vacillano: producono meno energia e rilasciano sottoprodotti nocivi che danneggiano le cellule e le spingono verso la morte. La mitofagia è la risposta d’emergenza della cellula, che marca i mitocondri difettosi e li invia alla degradazione e al riciclo. In teoria, una pulizia tempestiva previene l’accumulo di tossine e limita il danno. Ma se questo processo è troppo debole o troppo intenso, può permettere ai mitocondri malfunzionanti di persistere o privare la cellula dei produttori di energia di cui ha bisogno per sopravvivere. Comprendere dove si collocano i pazienti colpiti da ictus su questo filo sottile è centrale nello studio.
Scavando nei big data per trovare segnali di allarme nel sangue
Il team ha combinato diversi grandi dataset di espressione genica provenienti da pazienti con ictus e da soggetti sani, poi si è concentrato su un pannello di geni già associati alla mitofagia. Utilizzando statistiche avanzate e più modelli di machine learning, hanno cercato i pattern che distinguevano meglio i campioni di ictus da quelli di controllo. Hanno identificato diciannove geni correlati alla mitofagia che risultavano alterati nell’ictus e che definivano due grandi gruppi di pazienti con caratteristiche molecolari e immunitarie differenti. Un’analisi di rete più approfondita ha messo in evidenza un cluster denso di geni legati alla funzione mitocondriale e alla produzione proteica, suggerendo che l’approvvigionamento energetico e l’attività della “fabbrica” cellulare sono strettamente interconnessi nell’ictus.
Cinque indizi genetici chiave e il legame con il sistema immunitario
Da questa rete, i ricercatori hanno addestrato e confrontato otto modelli predittivi, concentrandosi infine su cinque geni di spicco — SRPRB, ATP5J, LSM7, DEGS1 e TGDS — come marcatori principali. Un test combinato a cinque geni ha separato con precisione i campioni di ictus dai controlli nei loro dati. Esperimenti di laboratorio usando un modello cellulare di deprivazione di ossigeno e glucosio e sangue di pazienti colpiti da ictus hanno confermato che questi geni effettivamente variano in sistemi biologici reali, non solo nelle analisi al computer. Diversi di essi sono associati a come i mitocondri producono energia, a come le cellule gestiscono i lipidi e a come vengono processati i messaggi genetici. Lo studio ha inoltre mostrato che questi marcatori sono fortemente correlati con specifici tipi di cellule immunitarie e percorsi di segnalazione, suggerendo che la reazione immunitaria dopo l’ictus è strettamente collegata alla salute mitocondriale e ai processi di coagulazione del sangue.
Zoom sulle sentinelle cerebrali chiamate microglia
Poiché i campioni di sangue non possono catturare pienamente ciò che avviene all’interno del cervello, il team si è rivolto a dati single‑cell provenienti da un modello murino di ictus. Hanno esaminato migliaia di singole cellule cerebrali e identificato gruppi distinti, concentrandosi sulle microglia, le cellule immunitarie residenti del cervello. Dopo l’ictus, le microglia sono passate da uno stato calmo e sorvegliante a stati infiammatori e associati alla malattia. Queste microglia “attivate” hanno mostrato un’attività di mitofagia molto più elevata, coerente con un forte impulso a eliminare i mitocondri danneggiati. Uno dei cinque geni chiave, ATP5J, ha mostrato un aumento dinamico lungo la progressione dallo stato di riposo a quello associato alla malattia, sottolineando il suo potenziale ruolo sia come marcatore sia come regolatore della risposta di queste cellule al danno.
Cosa potrebbe significare per la cura dell’ictus in futuro
Nel complesso, il lavoro dipinge la mitofagia non come qualcosa di semplicemente buono o cattivo, ma come una risposta finemente regolata che varia tra tipi cellulari, stadi della malattia e compartimenti corporei come sangue e tessuto cerebrale. I cinque geni evidenziati — in particolare ATP5J — offrono punti di partenza promettenti per test basati sul sangue che potrebbero classificare meglio i pazienti con ictus e, in prospettiva, guidare terapie che orientino la pulizia mitocondriale verso una “zona protettiva” ottimale. Sebbene siano necessari ulteriori esperimenti in modelli cellulari cerebrali appropriati e studi su gruppi di pazienti più ampi, lo studio suggerisce che salvare il cervello nell’ictus potrebbe dipendere tanto dal riparare i suoi microscopici sistemi energetici quanto dal riaprire le arterie bloccate.
Citazione: Cao, Z., Wang, Y., Sun, M. et al. Single-cell and multi-omics analysis identifies mitophagy-related biomarkers and therapeutic targets in ischemic stroke. Sci Rep 16, 12433 (2026). https://doi.org/10.1038/s41598-026-43377-z
Parole chiave: ictus ischemico, mitofagia, mitocondri, microglia, biomarcatori