Clear Sky Science · nl
Single-cell en multi-omics analyse identificeert mitofagie-gerelateerde biomarkers en therapeutische doelen bij ischemische beroerte
Waarom beschadigde celbatterijen belangrijk zijn bij beroerte
Beroerte wordt vaak beschreven als een probleem van verstopte bloedvaten, maar wat er binnenin hersencellen gebeurt nadat de bloedtoevoer stopt, kan net zo bepalend zijn. Deze studie bekijkt de cel"s “energiecentrales” – de mitochondriën – en een ingebouwd opruimproces genaamd mitofagie dat beschadigde mitochondriën verwijdert. Door te volgen hoe dit opruimsysteem zich gedraagt bij een beroerte en welke genen het reguleren, willen de onderzoekers nieuwe manieren vinden om te voorspellen wie een slechtere uitkomst loopt en behandelingen te ontwikkelen die hersencellen beschermen wanneer iedere minuut telt.
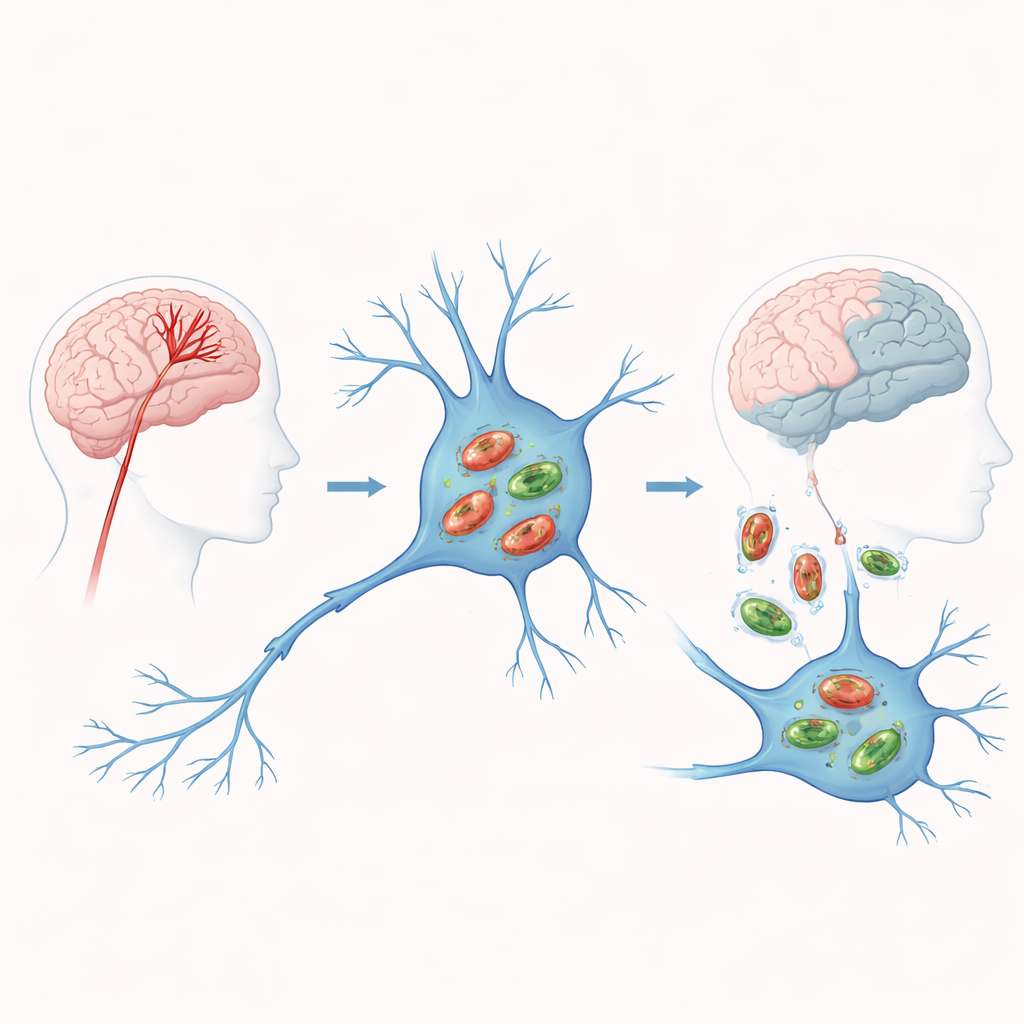
Wanneer de bloedstroom stopt, faalt de energie in hersencellen
Bij een ischemische beroerte sluit een geblokkeerde slagader de toevoer van zuurstof en voedingsstoffen naar een deel van de hersenen af. Zonder brandstof functioneren mitochondriën minder goed: ze produceren minder energie en lozen schadelijke bijproducten die cellen beschadigen en richting celdood duwen. Mitofagie is de noodreactie van de cel, die defecte mitochondriën markeert en verzendt voor afbraak en recyclage. In theorie voorkomt tijdige opruiming giftige ophoping en beperkt het schade. Maar als dit proces te zwak of juist te sterk is, kan het óf gecorrumpeerde mitochondriën laten aanhouden óf cellen beroven van de energieleveranciers die ze nodig hebben om te overleven. Begrijpen waar patiënten op dit scheermesje zitten, staat centraal in de studie.
Grote datasets doorzoeken om waarschuwingssignalen in bloed te vinden
Het team combineerde meerdere grote genexpressiedatasets van beroertepatiënten en gezonde personen en richtte zich vervolgens op een paneel genen dat al aan mitofagie gekoppeld is. Met geavanceerde statistiek en meerdere machine-learningmodellen zochten ze naar patronen die het beste beroerte- van niet-beroerte-monsters onderscheiden. Ze vonden negentien mitofagie-gerelateerde genen die veranderden bij beroerte en die twee hoofdgroepen patiënten vormden met verschillende moleculaire en immuunkenmerken. Een diepere netwerk analyse benadrukte één dicht cluster van genen verbonden aan mitochondriale functie en eiwitproductie, wat suggereert dat energievoorziening en de activiteit van de cellulaire “fabriek” nauw met elkaar verweven zijn bij beroerte.
Vijf belangrijke genetische aanwijzingen en de immuunverbinding
Uit dit netwerk trainden en vergeleken de onderzoekers acht voorspellingsmodellen en kwamen uiteindelijk uit op vijf opvallende genen—SRPRB, ATP5J, LSM7, DEGS1 en TGDS—als kernmarkers. Een gecombineerd vijf-genentest onderscheidde beroerte- van controlemateriaal nauwkeurig in hun gegevens. Laboratoriumexperimenten met een celmodel van zuurstof- en glucosegebrek en bloed van beroertepatiënten bevestigden dat deze genen daadwerkelijk veranderen in echte biologische systemen, niet alleen in computersimulaties. Verschillende van deze genen zijn gekoppeld aan hoe mitochondriën energie produceren, hoe cellen vetten verwerken en hoe genetische boodschappen worden verwerkt. De studie toonde ook aan dat deze markers sterk samenhangen met bepaalde immuuncellen en -routes, wat aangeeft dat de immuunreactie na beroerte nauw verbonden is met mitochondriale gezondheid en stollingsprocessen.
Inzoomen op hersenverdedigers genaamd microglia
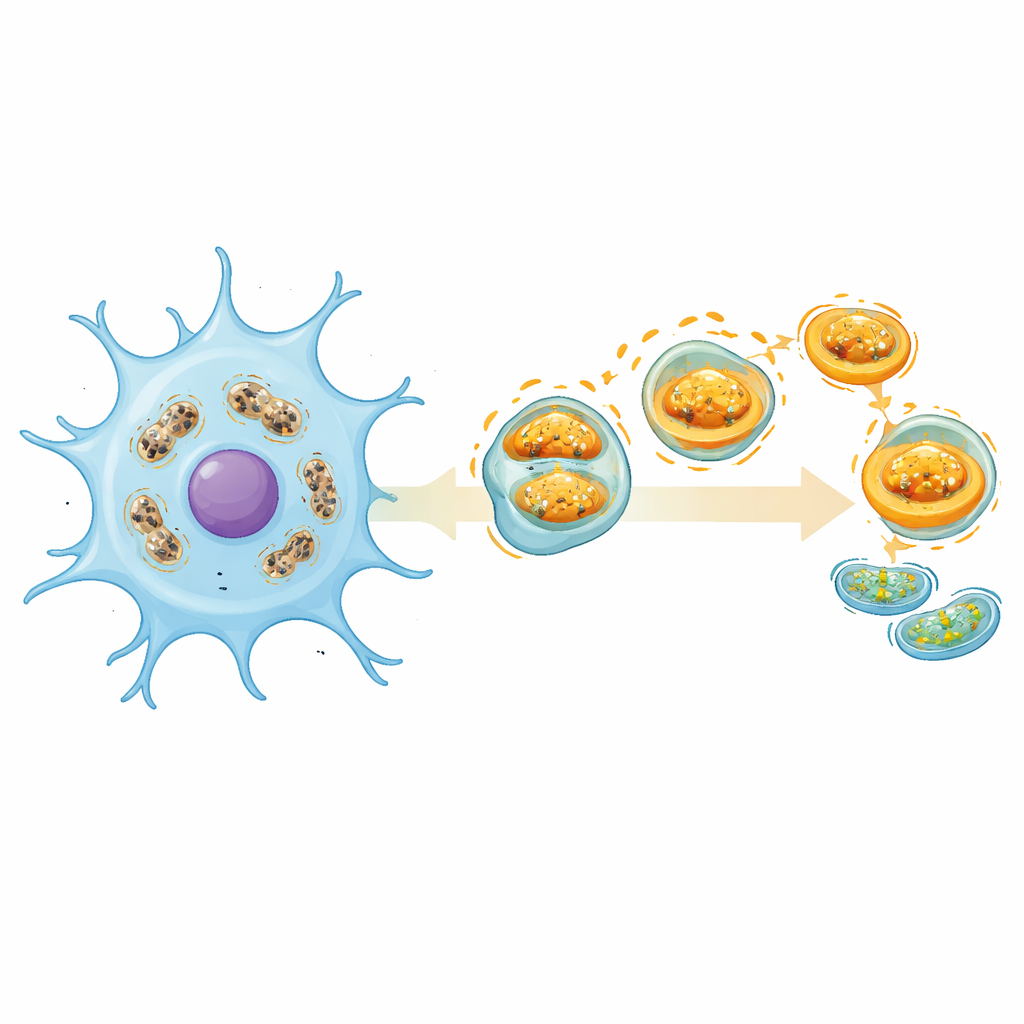
Aangezien bloedmonsters niet volledig vastleggen wat er in de hersenen gebeurt, wendde het team zich tot single-cell data uit een muismodel van beroerte. Ze onderzochten duizenden individuele hersencellen en identificeerden onderscheiden groepen, met de nadruk op microglia, de residentiële immuuncellen van de hersenen. Na beroerte verschoven microglia van een kalme, waakzame toestand naar inflammatoire en ziekte-geassocieerde toestanden. Deze “geactiveerde” microglia vertoonden veel hogere mitofagie-activiteit, overeenkomend met een sterke inzet om beschadigde mitochondriën te verwijderen. Eén van de vijf sleutelgenen, ATP5J, toonde een dynamische toename langs de progressie van rustende naar ziekte-gerelateerde microglia, wat zijn potentiële rol onderstreept als zowel merker als regulator van hoe deze cellen op letsel reageren.
Wat dit kan betekenen voor toekomstige beroertezorg
Alles bij elkaar schetst het werk mitofagie niet als simpelweg goed of slecht, maar als een fijn afgestelde respons die verschilt tussen celtypen, ziektefasen en lichaamscompartimenten zoals bloed versus hersenweefsel. De vijf uitgelichte genen—met name ATP5J—bieden veelbelovende aanknopingspunten voor bloedtests die beroortepatiënten beter kunnen classificeren en uiteindelijk therapieën kunnen sturen die de mitochondriale opruiming naar een beschermend “sweet spot” duwen. Hoewel meer experimenten in geschikte hersencelmodellen en grotere patiëntengroepen nodig zijn, suggereert de studie dat het redden van de hersenen bij beroerte net zozeer kan afhangen van het herstellen van zijn microscopische energiesystemen als van het weer openen van afgesloten bloedvaten.
Bronvermelding: Cao, Z., Wang, Y., Sun, M. et al. Single-cell and multi-omics analysis identifies mitophagy-related biomarkers and therapeutic targets in ischemic stroke. Sci Rep 16, 12433 (2026). https://doi.org/10.1038/s41598-026-43377-z
Trefwoorden: ischeemische beroerte, mitofagie, mitochondriën, microglia, biomarkers