Clear Sky Science · pt
Avaliação do potencial anti-inflamatório da atorvastatina visando TNF-α, IL-6 e IL-1β usando abordagens integradas in vitro e in silico
Por que um remédio para colesterol importa na inflamação
Milhões de pessoas tomam atorvastatina para reduzir o colesterol e proteger o coração. Este estudo faz uma pergunta surpreendente: a mesma pílula também poderia acalmar a inflamação nociva em todo o corpo? Ao combinar modelagem computacional com experimentos em células, os pesquisadores investigam se a atorvastatina pode reduzir diretamente mensageiros inflamatórios potentes que impulsionam doenças como artrite, diabetes e doenças cardíacas.
Como o sistema de alarme do corpo pode se voltar contra nós
A inflamação é o sistema de alarme embutido do corpo, acionado quando enfrentamos infecção ou lesão. No curto prazo, ela é protetora, recrutando células imunes e ajudando a reparar tecidos. O problema surge quando o alarme nunca realmente se desliga. Então, mensageiros químicos-chave chamados citocinas — particularmente TNF-alfa, IL-6 e IL-1 beta — permanecem elevados e mantêm o corpo em um estado constante de batalha de baixo grau. Essa inflamação crônica está associada a uma ampla gama de doenças, desde problemas articulares e artérias obstruídas até distúrbios neurológicos e alguns cânceres. Como desenvolver medicamentos completamente novos é lento e caro, os cientistas têm interesse em saber se medicamentos já confiáveis, como as estatinas, podem ser reposicionados para atuar nesses sinais inflamatórios.
Investigando encontros droga–proteína no computador
A equipe primeiro usou simulações computacionais avançadas para ver como a atorvastatina poderia interagir fisicamente com as três citocinas. Eles realizaram docking molecular, um método que prevê quão bem uma pequena molécula pode encaixar na superfície de uma proteína, e seguiram com longas simulações de dinâmica molecular para observar o complexo ao longo do tempo. A atorvastatina mostrou o acoplamento mais firme e estável com o TNF-alfa, acomodando-se numa região superficial usada para se ligar ao seu receptor nas células. O complexo virtual permaneceu compacto e estável durante uma simulação de 200 nanosegundos, e cálculos de energia sugeriram que forças atrativas entre regiões lipofílicas (hidrofóbicas) e porções cíclicas do fármaco e da proteína favoreceram fortemente a ligação.
Testando o efeito anti-inflamatório em células imunes
Para verificar se essas previsões computacionais se traduzem em biologia real, os pesquisadores recorreram a um modelo laboratorial padrão de inflamação. Eles expuseram macrófagos de camundongo — células imunes que ajudam a coordenar respostas inflamatórias — a um componente bacteriano que as ativa fortemente. Antes desse estímulo, as células foram tratadas com diferentes doses de atorvastatina. O fármaco não comprometeu a sobrevivência celular até 20 micromolar, indicando que seus efeitos não se deviam à toxicidade. À medida que a dose aumentou, as células liberaram progressivamente menos TNF-alfa, IL-6 e IL-1 beta ao seu redor. Na dose mais alta, os níveis desses mensageiros inflamatórios caíram acentuadamente. A atorvastatina também reduziu a produção de óxido nítrico, outra molécula que aumenta durante a inflamação e pode danificar tecidos quando produzida em excesso.
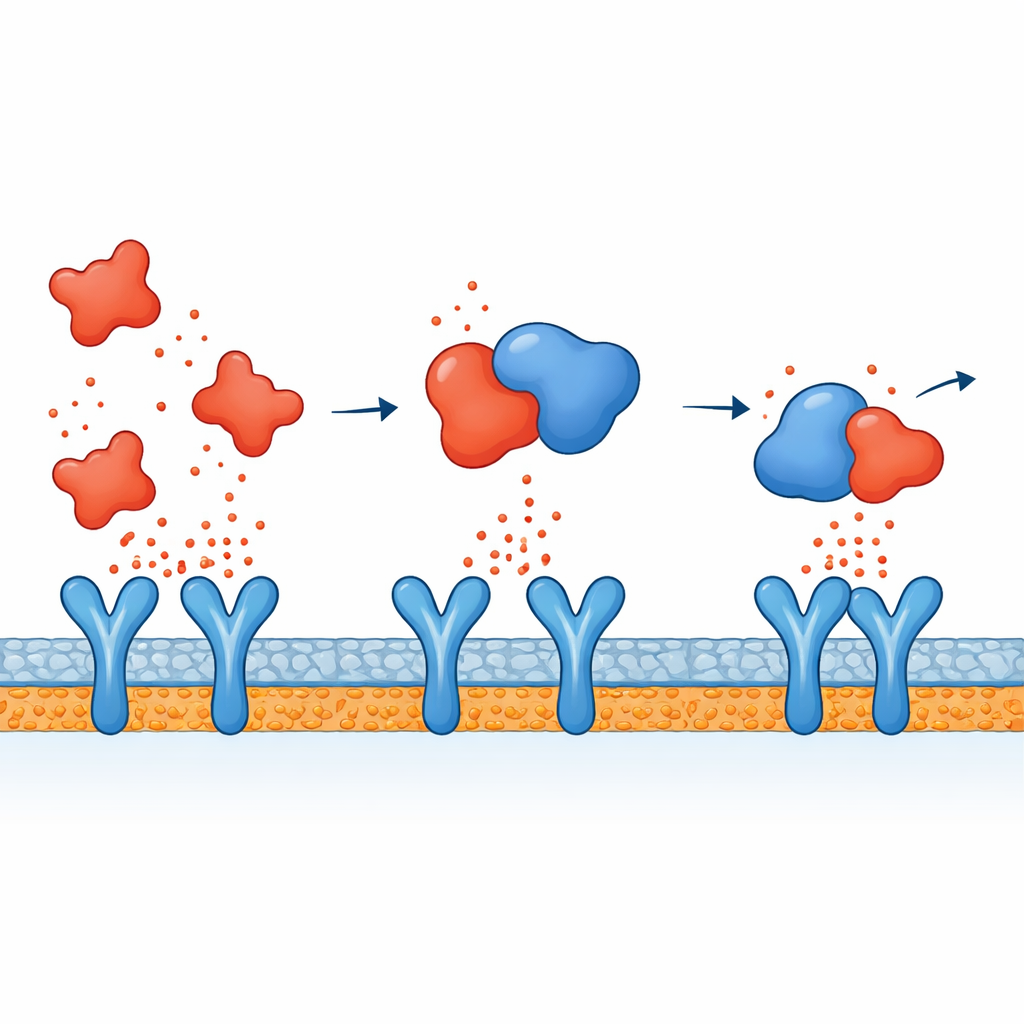
Ligando a ligação molecular a um sinal mais calmo
Juntando as peças, os autores propõem uma ação dupla para a atorvastatina. Dentro das células imunes, ela parece atenuar as vias de sinalização que normalmente ativam genes inflamatórios após uma ameaça microbiana, de modo que menos citocinas são produzidas desde o início. Ao mesmo tempo, as simulações sugerem que as citocinas que escapam para a corrente sanguínea podem ser parcialmente neutralizadas porque a atorvastatina se liga diretamente a elas, especialmente ao TNF-alfa, dificultando que esses mensageiros se acoplem a seus receptores e propaguem o alarme. Esse efeito combinado poderia ajudar a explicar por que observou-se que as estatinas reduzem marcadores inflamatórios em pacientes, além de seu conhecido impacto sobre o colesterol.
O que isso pode significar para os pacientes
Para um leitor geral, a conclusão principal é que um conhecido medicamento para reduzir o colesterol também pode atuar como um modulador multifuncional da inflamação. Embora este trabalho tenha sido realizado em modelos computacionais e culturas celulares — ainda não em pacientes —, ele oferece um quadro detalhado, em nível molecular, de como a atorvastatina poderia desarmar diretamente alguns dos mensageiros inflamatórios mais potentes do corpo sem prejudicar as células. As descobertas reforçam o argumento a favor de testar a atorvastatina, e possivelmente seus parentes químicos próximos, como tratamentos acessíveis e amplamente disponíveis para condições inflamatórias crônicas, além de seu papel estabelecido na proteção cardíaca.
Citação: Swaroop, K., M., R., Shaik, S. et al. Evaluation of the anti-inflammatory potential of atorvastatin targeting TNF-α, IL-6, and IL-1β using integrated in vitro and in silico approaches. Sci Rep 16, 9914 (2026). https://doi.org/10.1038/s41598-026-39082-6
Palavras-chave: atorvastatina, inflamação crônica, citocinas, reposicionamento de medicamentos, TNF-alfa