Clear Sky Science · de
Bewertung des antientzündlichen Potenzials von Atorvastatin mit Blick auf TNF-α, IL-6 und IL-1β durch integrierte in vitro- und in silico-Ansätze
Warum ein Cholesterinmedikament für Entzündungen relevant ist
Millionen Menschen nehmen Atorvastatin, um ihren Cholesterinspiegel zu senken und das Herz zu schützen. Die Studie stellt eine überraschende Frage: Könnte dieselbe Tablette auch schädliche Entzündungen im ganzen Körper dämpfen? Durch die Kombination von Computermodellen und Zellversuchen untersuchen die Forschenden, ob Atorvastatin die starken entzündlichen Botenstoffe, die Krankheiten wie Arthritis, Diabetes und Herzkrankheiten antreiben, direkt herunterregeln kann.
Wie das körpereigene Alarmsystem gegen uns arbeiten kann
Entzündung ist das eingebaute Alarmsystem des Körpers, das bei Infektion oder Verletzung aktiviert wird. Kurzfristig schützt es, ruft Immunzellen herbei und unterstützt die Gewebereparatur. Problematisch wird es, wenn der Alarm nicht wirklich abschaltet. Dann bleiben Schlüsselbotenstoffe, sogenannte Zytokine – insbesondere TNF-alpha, IL-6 und IL-1 beta – erhöht und halten den Körper in einem dauerhaften Zustand niedriggradiger Abwehr. Diese chronische Entzündung steht im Zusammenhang mit einer Vielzahl von Erkrankungen, von Gelenkkrankheiten und verstopften Arterien bis zu neurologischen Störungen und einigen Krebsarten. Da völlig neue Medikamente langsam und teuer zu entwickeln sind, prüfen Wissenschaftler gern, ob bewährte Arzneien wie Statine für die gezielte Bekämpfung dieser Entzündungssignale umgenutzt werden können.
Untersuchung von Wirkstoff–Protein-Begegnungen im Computer
Das Team nutzte zunächst fortgeschrittene Computersimulationen, um zu sehen, wie Atorvastatin physikalisch mit den drei Zytokinen interagieren könnte. Sie führten molekulares Docking durch, ein Verfahren, das vorhersagt, wie gut ein kleines Molekül auf der Proteinoberfläche passen könnte, und ergänzten dies durch lange Molekulardynamik-Simulationen, um das Komplexverhalten über die Zeit zu beobachten. Atorvastatin zeigte die engste und stabilste Bindung an TNF-alpha und nahm eine Oberflächenregion ein, die normalerweise zur Bindung an dessen Rezeptor auf Zellen genutzt wird. Der virtuelle Komplex blieb über einen 200-Nanosekunden-Lauf kompakt und stabil, und Energieanalysen deuteten darauf hin, dass anziehende Kräfte zwischen hydrophoben Bereichen und ringförmigen Regionen des Wirkstoffs und des Proteins die Bindung stark begünstigen.
Test des antientzündlichen Effekts in Immunzellen
Um zu prüfen, ob diese Computerprognosen in lebender Biologie greifen, wandten sich die Forschenden einem standardisierten Labormodell der Entzündung zu. Sie setzten Mausmakrophagen — Immunzellen, die Entzündungsreaktionen koordinieren — einem bakteriellen Bestandteil aus, der sie stark aktiviert. Vor diesem Auslöser wurden die Zellen mit unterschiedlichen Dosen Atorvastatin behandelt. Das Medikament beeinträchtigte das Überleben der Zellen bis zu 20 Mikromolar nicht, was bedeutet, dass die Effekte nicht auf Toxizität zurückzuführen waren. Mit steigender Dosis schütteten die Zellen zunehmend weniger TNF-alpha, IL-6 und IL-1 beta in ihr Umfeld aus. Bei der höchsten Dosis sanken die Spiegel dieser entzündlichen Botenstoffe deutlich. Atorvastatin reduzierte außerdem die Produktion von Stickstoffmonoxid, einem weiteren Molekül, das während Entzündungen ansteigt und bei Überproduktion Gewebe schädigen kann.
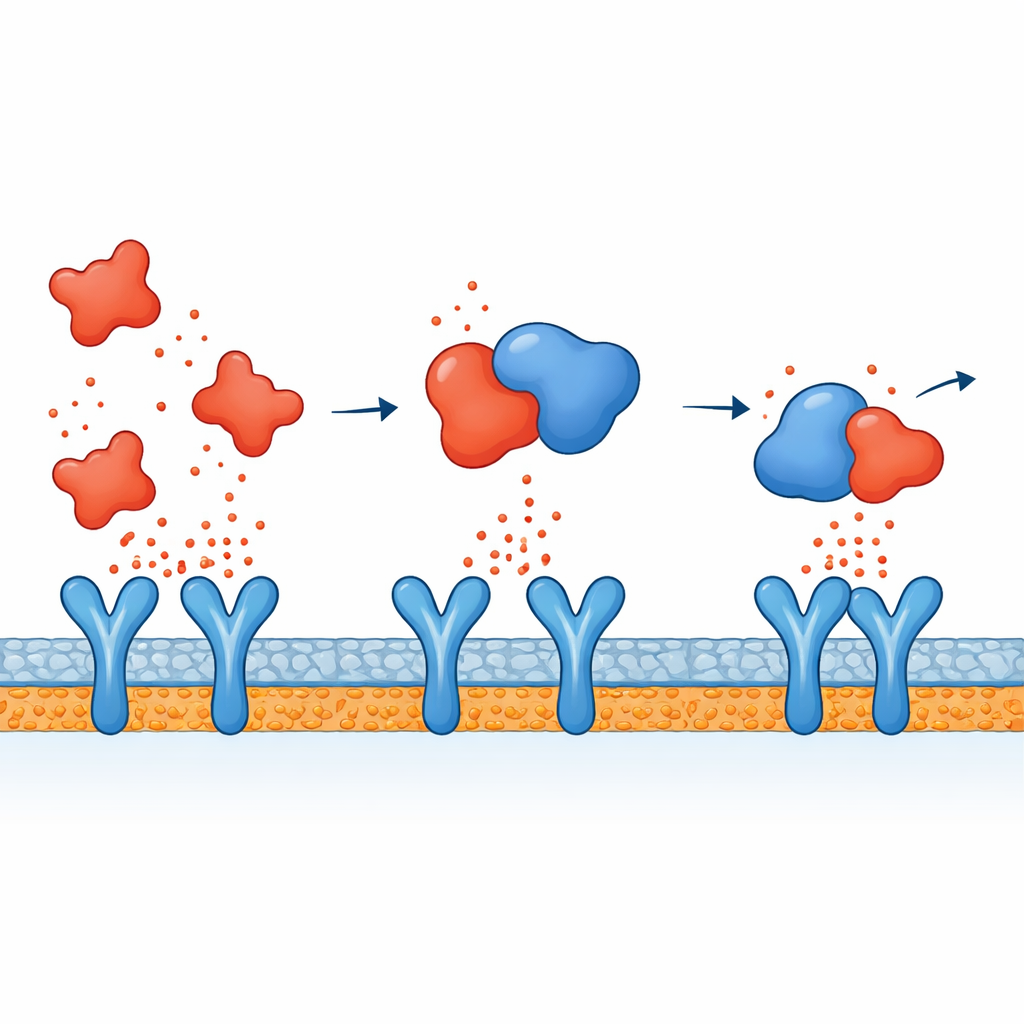
Verknüpfung von Molekülbindung mit gedämpfter Signalübertragung
Zusammengeführt schlagen die Autorinnen und Autoren eine zweigleisige Wirkweise für Atorvastatin vor. Innerhalb der Immunzellen scheint es die Signalwege zu dämpfen, die normalerweise nach einer mikrobiellen Bedrohung entzündungsfördernde Gene einschalten, sodass von vornherein weniger Zytokine produziert werden. Gleichzeitig deuten die Simulationen darauf hin, dass Zytokine, die dennoch in den Blutkreislauf gelangen, teilweise neutralisiert werden könnten, weil Atorvastatin direkt an sie bindet — besonders an TNF-alpha — und es ihnen so schwerer macht, an ihre Rezeptoren anzudocken und den Alarm weiterzugeben. Dieser kombinierte Effekt könnte erklären, warum Statine in Patienten beobachtet wurden, dass sie Entzündungsmarker senken, zusätzlich zu ihrem bekannten Einfluss auf Cholesterin.
Was das für Patientinnen und Patienten bedeuten könnte
Für eine allgemeine Leserschaft ist die zentrale Erkenntnis, dass ein vertrautes cholesterinsenkendes Medikament zugleich als vielseitiger Entzündungsmodulator wirken könnte. Während diese Arbeit in Computermodellen und Zellkulturen durchgeführt wurde — noch nicht in Patientinnen und Patienten — liefert sie ein detailliertes, molekular motiviertes Bild davon, wie Atorvastatin einige der stärksten entzündlichen Signale des Körpers direkt entschärfen kann, ohne Zellen zu schädigen. Die Befunde untermauern die Argumente für weitergehende Tests von Atorvastatin und möglicherweise seiner nahen chemischen Verwandten als kostengünstige und breit verfügbare Behandlungsoptionen für chronische Entzündungserkrankungen, zusätzlich zu ihrer etablierten Rolle beim Schutz des Herzens.
Zitation: Swaroop, K., M., R., Shaik, S. et al. Evaluation of the anti-inflammatory potential of atorvastatin targeting TNF-α, IL-6, and IL-1β using integrated in vitro and in silico approaches. Sci Rep 16, 9914 (2026). https://doi.org/10.1038/s41598-026-39082-6
Schlüsselwörter: atorvastatin, chronische Entzündung, Zytokine, Wirkstoff-Repositionierung, TNF-alpha