Clear Sky Science · fr
Évaluation du potentiel anti-inflammatoire de l’atorvastatine ciblant TNF-α, IL-6 et IL-1β à l’aide d’approches intégrées in vitro et in silico
Pourquoi un médicament contre le cholestérol importe pour l’inflammation
Des millions de personnes prennent de l’atorvastatine pour réduire leur cholestérol et protéger leur cœur. Cette étude pose une question surprenante : la même pilule pourrait-elle aussi calmer l’inflammation nocive dans tout l’organisme ? En combinant modélisation informatique et expériences cellulaires, les chercheurs examinent si l’atorvastatine peut directement réduire des messagers inflammatoires puissants qui alimentent des maladies comme l’arthrite, le diabète et les maladies cardiovasculaires.
Comment le système d’alarme du corps peut se retourner contre nous
L’inflammation est le système d’alarme intégré du corps, activé quand nous sommes confrontés à une infection ou à une blessure. À court terme, elle protège en attirant les cellules immunitaires et en aidant à réparer les tissus. Le problème survient quand l’alarme ne s’éteint jamais vraiment. Alors, des messagers chimiques clés appelés cytokines — en particulier le TNF-alpha, l’IL-6 et l’IL-1 bêta — restent élevés et maintiennent le corps dans un état persistant de lutte de faible intensité. Cette inflammation chronique est liée à un large éventail de pathologies, des maladies articulaires et des artères obstruées aux troubles neurologiques et à certains cancers. Parce que le développement de nouveaux médicaments est long et coûteux, les scientifiques cherchent à savoir si des médicaments éprouvés comme les statines peuvent être réutilisés pour cibler ces signaux inflammatoires.
Explorer les rencontres médicament–protéine sur ordinateur
L’équipe a d’abord utilisé des simulations informatiques avancées pour voir comment l’atorvastatine pourrait interagir physiquement avec les trois cytokines. Ils ont réalisé du docking moléculaire, une méthode qui prédit à quel point une petite molécule peut s’ajuster sur la surface d’une protéine, puis ont enchaîné avec de longues simulations de dynamique moléculaire pour observer le complexe au fil du temps. L’atorvastatine a montré l’ajustement le plus serré et le plus stable avec le TNF-alpha, se calant dans une région de surface utilisée pour se lier à son récepteur sur les cellules. Le complexe virtuel est resté compact et stable pendant une simulation de 200 nanosecondes, et des calculs énergétiques ont suggéré que des forces attractives entre des patchs hydrophobes et des régions annulaires du médicament et de la protéine favorisaient fortement la liaison.
Tester l’effet anti-inflammatoire dans des cellules immunitaires
Pour vérifier si ces prédictions informatiques se traduisent en biologie réelle, les chercheurs se sont tournés vers un modèle de laboratoire standard d’inflammation. Ils ont exposé des macrophages de souris — des cellules immunitaires qui aident à coordonner les réponses inflammatoires — à un composant bactérien qui les active fortement. Avant ce stimulus, les cellules ont été traitées avec différentes doses d’atorvastatine. Le médicament n’a pas nui à la survie cellulaire jusqu’à 20 micromoles, ce qui signifie que ses effets n’étaient pas dus à une toxicité. À mesure que la dose augmentait, les cellules relâchaient de moins en moins de TNF-alpha, d’IL-6 et d’IL-1 bêta dans leur environnement. À la dose la plus élevée, les niveaux de ces messagers inflammatoires ont chuté fortement. L’atorvastatine a aussi réduit la production d’oxyde nitrique, une autre molécule qui augmente pendant l’inflammation et peut endommager les tissus lorsqu’elle est surproduite.
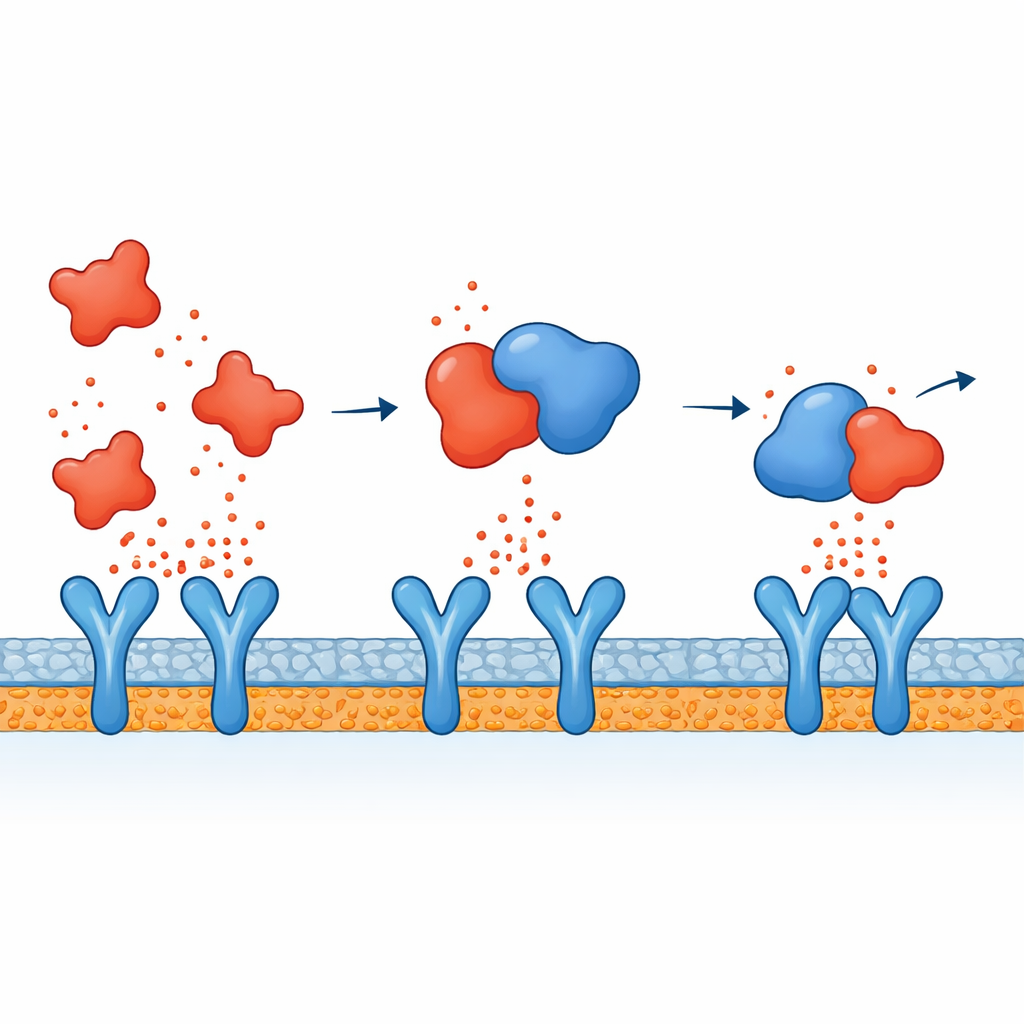
Relier la liaison moléculaire à un signalement plus calme
En réunissant les éléments, les auteurs proposent une action à deux volets pour l’atorvastatine. À l’intérieur des cellules immunitaires, elle semble atténuer les voies de signalisation qui activent normalement les gènes inflammatoires après une menace microbienne, de sorte que moins de cytokines sont produites initialement. Parallèlement, les simulations suggèrent que les cytokines qui parviennent dans le sang peuvent être partiellement neutralisées parce que l’atorvastatine se lie directement à elles, en particulier au TNF-alpha, rendant plus difficile l’attachement de ces messagers à leurs récepteurs et la propagation de l’alerte. Cet effet combiné pourrait aider à expliquer pourquoi on a observé que les statines abaissent des marqueurs inflammatoires chez les patients, au-delà de leur effet bien établi sur le cholestérol.
Ce que cela pourrait signifier pour les patients
Pour le lecteur général, la conclusion clé est qu’un médicament bien connu pour abaisser le cholestérol pourrait aussi agir comme un modulateur polyvalent de l’inflammation. Bien que ce travail ait été réalisé en modèles informatiques et en cultures cellulaires — pas encore chez l’humain — il offre une image détaillée au niveau moléculaire de la manière dont l’atorvastatine pourrait désarmer directement certains des signaux inflammatoires les plus puissants du corps sans nuire aux cellules. Les résultats renforcent l’intérêt d’évaluer l’atorvastatine, et peut-être ses proches cousins chimiques, comme traitements abordables et largement disponibles pour des affections inflammatoires chroniques, en complément de leur rôle établi dans la protection cardiaque.
Citation: Swaroop, K., M., R., Shaik, S. et al. Evaluation of the anti-inflammatory potential of atorvastatin targeting TNF-α, IL-6, and IL-1β using integrated in vitro and in silico approaches. Sci Rep 16, 9914 (2026). https://doi.org/10.1038/s41598-026-39082-6
Mots-clés: atorvastatine, inflammation chronique, cytokines, réaffectation de médicaments, TNF-alpha