Clear Sky Science · ar
تقييم الإمكانات المضادة للالتهاب للأتورفاستاتين مستهدفةً TNF-α وIL-6 وIL-1β باستخدام نهج متكامل in vitro وin silico
لماذا يهم دواء للكوليسترول في الالتهاب
يتناول الملايين الأتورفاستاتين لتخفيض الكوليسترول وحماية القلب. تطرح هذه الدراسة سؤالاً مفاجئاً: هل يمكن أن يهدئ نفس القرص الالتهاب الضار في أنحاء الجسم؟ من خلال الجمع بين النمذجة الحاسوبية وتجارب الخلايا، يستكشف الباحثون ما إذا كان الأتورفاستاتين قادرًا على تقليل مباشرة الرسائل الالتهابية القوية التي تدفع أمراضًا مثل التهاب المفاصل والسكري وأمراض القلب.
كيف يتحول نظام الإنذار في الجسم ضدنا
الالتهاب هو نظام الإنذار المدمج بالجسم، يُفعل عند مواجهة عدوى أو إصابة. على المدى القصير يكون حمايةً، يستدعي خلايا المناعة ويساعد على إصلاح الأنسجة. تكمن المشكلة عندما لا ينطفئ هذا الإنذار فعلاً. عندها تبقى رسائل كيميائية رئيسية تُسمى السيتوكينات—لاسيما TNF-alpha وIL-6 وIL-1 beta—مرتفعة وتبقي الجسم في حالة صراع مزمن منخفض المستوى. يرتبط هذا الالتهاب المزمن بنطاق واسع من الأمراض، من أمراض المفاصل وتصلب الشرايين إلى اضطرابات عصبية وبعض السرطانات. وبما أن تطوير أدوية جديدة بالكامل بطيء ومكلف، يحرص العلماء على معرفة ما إذا كان يمكن إعادة توظيف أدوية موثوقة مثل الستاتينات لاستهداف هذه الإشارات الالتهابية.
استكشاف لقاءات الدواء–البروتين في الحاسوب
بدأ الفريق باستخدام محاكيات حاسوبية متقدمة ليرى كيف قد يتفاعل الأتورفاستاتين فعليًا مع السيتوكينات الثلاثة. أجروا إرساء جزيئي، وهي طريقة تتنبأ بمدى ملاءمة جزيء صغير لالتصاق على سطح بروتين، وتبعوها بمحاكاة ديناميكيات جزيئية طويلة لمراقبة المجمع مع مرور الزمن. أظهر الأتورفاستاتين أفضل توافق واستقرار مع TNF-alpha، مستقرًا في منطقة سطحية تُستخدم للالتصاق بالمستقبل على الخلايا. ظل المجمع الافتراضي مدمجًا ومستقرًا على مدار تشغيل دام 200 نانوثانية، وأشارت حسابات الطاقة إلى أن القوى الجاذبة بين بقع دهنية (محبة للماء الضعيفة) والمناطق الحلقية في الدواء والبروتين فضلت الارتباط بقوة.
اختبار التأثير المضاد للالتهاب في خلايا المناعة
ليروا ما إذا كانت تنبؤات الحاسوب هذه تترجم إلى بيولوجيا حقيقية، لجأ الباحثون إلى نموذج مخبري معيار للالتهاب. عرضوا خلايا البلعميات من الفئران—خلايا مناعية تساعد على تنسيق الاستجابات الالتهابية—لمكون بكتيري ينشطها بقوة. قبل هذا المنشط، عُولجت الخلايا بجرعات مختلفة من الأتورفاستاتين. لم يسبب الدواء ضررًا لبقاء الخلايا حتى 20 ميكرومولار، ما يعني أن تأثيراته لم تكن ناتجة عن سمية. مع زيادة الجرعة، أطلقت الخلايا كميات أقل تدريجيًا من TNF-alpha وIL-6 وIL-1 beta إلى محيطها. عند أعلى جرعة، انخفضت مستويات هذه الرسائل الالتهابية بشكل حاد. خفّض الأتورفاستاتين أيضًا إنتاج أكسيد النيتريك، وهو جزيء آخر يرتفع أثناء الالتهاب ويمكن أن يضر الأنسجة عند فرطه.
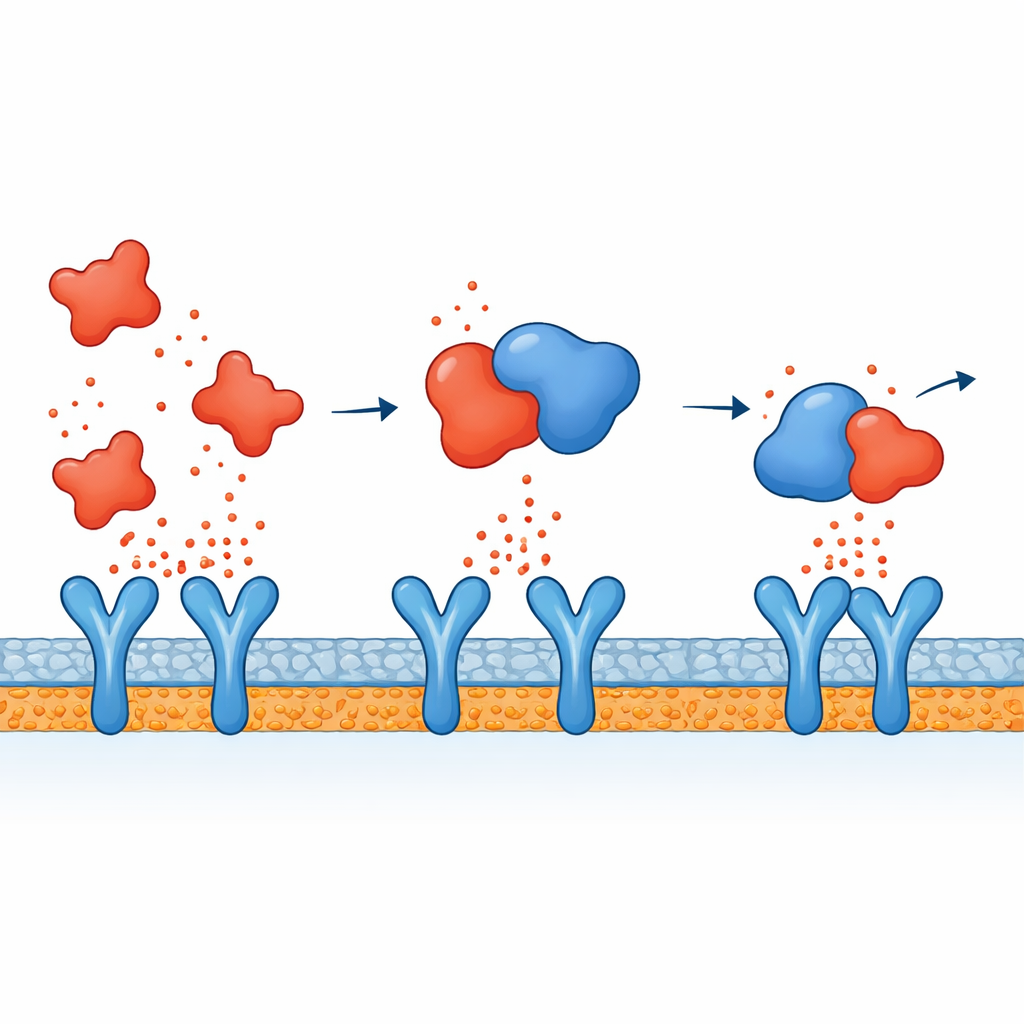
ربط ارتباط الجزيء بتهدئة الإشارات
بجمع الأدلة، يقترح المؤلفون آلية ذات شقين للأتورفاستاتين. داخل خلايا المناعة، يبدو أنه يخفف مسارات الإشارة التي عادةً تشغل الجينات الالتهابية بعد التهديد الميكروبي، فيُنتَج عدد أقل من السيتوكينات في المقام الأول. في الوقت نفسه، تقترح المحاكاة أن أي سيتوكينات تصل إلى مجرى الدم قد تُعطل جزئيًا لأن الأتورفاستاتين يرتبط بها مباشرة، خاصة TNF-alpha، مما يصعّب على هذه الرسائل الالتحام بمستقبلاتها ونشر الإنذار. قد يساهم هذا التأثير المركب في تفسير ملاحظات خفض علامات الالتهاب لدى المرضى الذين يتناولون الستاتينات، إلى جانب تأثيرها المعروف على الكوليسترول.
ماذا قد يعني هذا للمرضى
للقارئ العام، الخلاصة الرئيسة هي أن دواءً معروفًا لخفض الكوليسترول قد يعمل أيضًا كمنظّم متعدد الوظائف للالتهاب. بينما أُجريت هذه الدراسة في نماذج حاسوبية وزرعات خلوية—وليس بعد في المرضى—فإنها تقدم صورة جزيئية مفصلة عن كيفية تمكن الأتورفاستاتين من تعطيل بعض أقوى إشارات الالتهاب في الجسم مباشرةً دون إلحاق ضرر بالخلايا. تعزز النتائج الحجّة لاختبار الأتورفاستاتين، وربما نظائره الكيميائية القريبة، كعلاجات متاحة وبأسعار معقولة للحالات الالتهابية المزمنة، إلى جانب دوره الراسخ في حماية القلب.
الاستشهاد: Swaroop, K., M., R., Shaik, S. et al. Evaluation of the anti-inflammatory potential of atorvastatin targeting TNF-α, IL-6, and IL-1β using integrated in vitro and in silico approaches. Sci Rep 16, 9914 (2026). https://doi.org/10.1038/s41598-026-39082-6
الكلمات المفتاحية: أتورفاستاتين, الالتهاب المزمن, السيتوكينات, إعادة توظيف الأدوية, TNF-alpha