Clear Sky Science · pl
Ocena przeciwzapalnego potencjału atorwastatyny ukierunkowanego na TNF-α, IL-6 i IL-1β przy użyciu zintegrowanych podejść in vitro i in silico
Dlaczego lek na cholesterol ma znaczenie w zapaleniu
Miliony osób przyjmują atorwastatynę, by obniżyć cholesterol i chronić serce. W tym badaniu postawiono zaskakujące pytanie: czy ta sama tabletka może także uspokoić szkodliwe zapalenie w całym organizmie? Łącząc modelowanie komputerowe z eksperymentami na komórkach, badacze sprawdzają, czy atorwastatyna może bezpośrednio przyciszyć silne przekaźniki zapalne, które napędzają choroby takie jak zapalenie stawów, cukrzyca i choroba serca.
Jak system alarmowy organizmu może się obrócić przeciw nam
Zapalenie to wrodzony system alarmowy organizmu, uruchamiany w obliczu zakażenia lub urazu. Krótkoterminowo jest ochronne — przyciąga komórki odpornościowe i pomaga naprawić tkanki. Problem pojawia się, gdy alarm nigdy się nie wyłącza. Wtedy kluczowe przekaźniki chemiczne zwane cytokinami — w szczególności TNF-alfa, IL-6 i IL-1 beta — pozostają podwyższone i utrzymują organizm w stanie przewlekłego, niskiego poziomu walki. To przewlekłe zapalenie wiąże się z szerokim spektrum chorób, od schorzeń stawów i zwężenia tętnic po zaburzenia neurologiczne i niektóre nowotwory. Ponieważ opracowywanie zupełnie nowych leków jest wolne i kosztowne, naukowcy chętnie sprawdzają, czy sprawdzone leki, takie jak statyny, można przeznaczyć ponownie do celowania w te sygnały zapalne.
Badanie spotkań leku z białkami w komputerze
Zespół najpierw zastosował zaawansowane symulacje komputerowe, żeby zobaczyć, jak atorwastatyna mogłaby fizycznie wchodzić w interakcję z trzema cytokininami. Wykonali dokowanie molekularne, metodę przewidującą, jak ciasno mała cząsteczka może dopasować się do powierzchni białka, a następnie przeprowadzili długie symulacje dynamiki molekularnej, aby obserwować kompleks w czasie. Atorwastatyna wykazała najsilniejsze i najstabilniejsze dopasowanie z TNF-alfa, osiadając w obszarze powierzchni wykorzystywanym do wiązania z jego receptorem na komórkach. Wirtualny kompleks pozostał zwarty i stabilny podczas 200-nanosekundowego przebiegu, a obliczenia energetyczne sugerowały, że siły atrakcji między hydrofobowymi obszarami i pierścieniowymi fragmentami leku i białka silnie sprzyjały wiązaniu.
Testowanie przeciwzapalnego działania w komórkach odpornościowych
Aby sprawdzić, czy przewidywania komputerowe przekładają się na rzeczywistą biologię, badacze wykorzystali standardowy model laboratoryjny zapalenia. Narażali mysie makrofagi — komórki odpornościowe, które koordynują odpowiedzi zapalne — na składnik bakteryjny, który silnie je aktywuje. Przed podaniem tego bodźca komórki traktowano różnymi dawkami atorwastatyny. Lek nie wpływał negatywnie na przeżywalność komórek przy stężeniach do 20 mikromolowych, co oznacza, że obserwowane efekty nie były wynikiem toksyczności. Wraz ze wzrostem dawki komórki wydzielały stopniowo mniej TNF-alfa, IL-6 i IL-1 beta do otoczenia. Przy najwyższej dawce poziomy tych przekaźników zapalnych spadły gwałtownie. Atorwastatyna obniżała także produkcję tlenku azotu, innej cząsteczki wzrastającej podczas zapalenia, która przy nadprodukcji może uszkadzać tkanki.
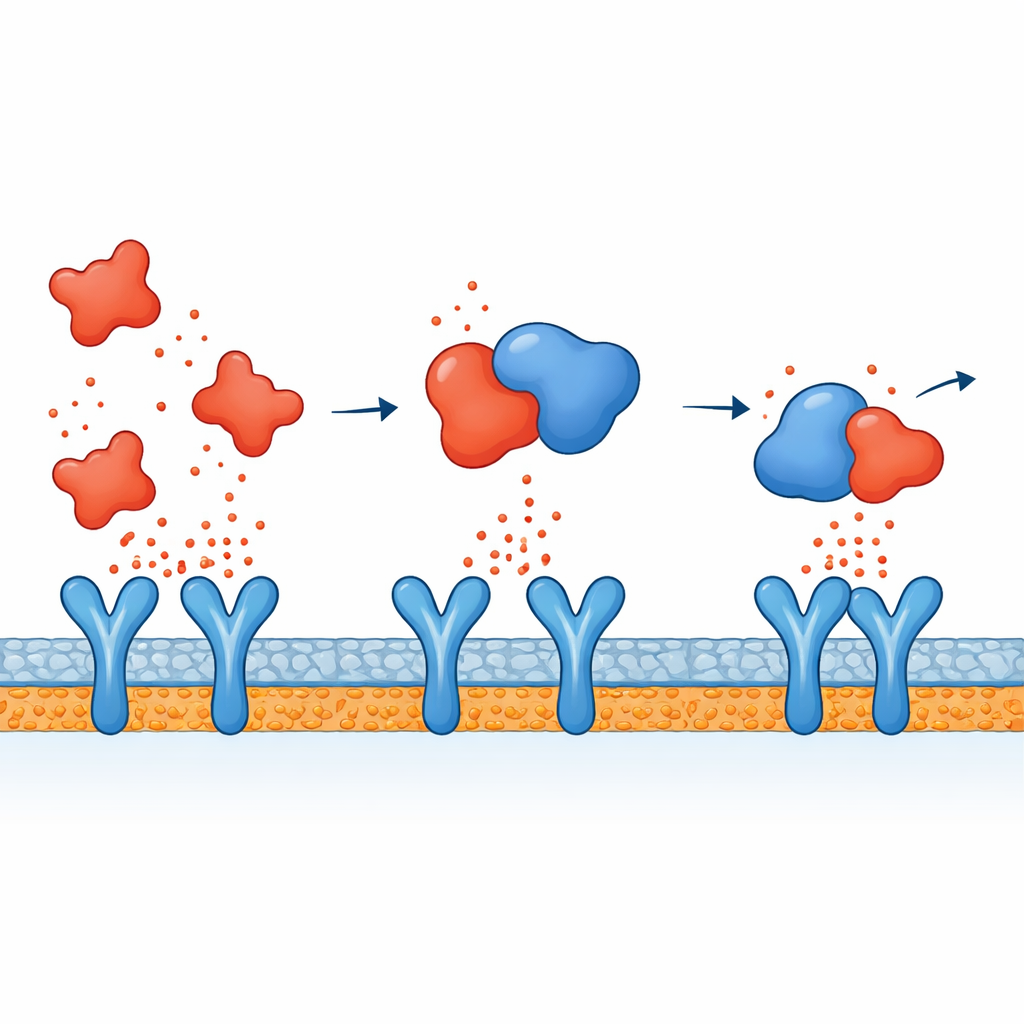
Powiązanie wiązania cząsteczki ze stłumieniem sygnalizacji
Składając elementy w całość, autorzy proponują dwuetapowy mechanizm działania atorwastatyny. Wewnątrz komórek odpornościowych wydaje się tłumić szlaki sygnałowe, które normalnie uruchamiają geny zapalne po napotkaniu mikroba, więc mniej cytokin jest wytwarzanych na samym początku. Jednocześnie symulacje sugerują, że te cytokiny, które wydostaną się do krwiobiegu, mogą być częściowo neutralizowane, ponieważ atorwastatyna wiąże się bezpośrednio z nimi, zwłaszcza z TNF-alfa, utrudniając tym przekaźnikom dokowanie do ich receptorów i propagowanie alarmu. Ten złożony efekt może pomóc wyjaśnić, dlaczego obserwowano obniżenie markerów zapalenia u pacjentów stosujących statyny, wykraczające poza ich dobrze znany wpływ na cholesterol.
Co to może oznaczać dla pacjentów
Dla czytelnika ogólnego kluczowy wniosek jest taki, że znany lek obniżający cholesterol może także działać jako wszechstronny modulator zapalenia. Choć prace te wykonano w modelach komputerowych i hodowlach komórkowych — jeszcze nie u pacjentów — dostarczają one szczegółowego obrazu na poziomie molekularnym, jak atorwastatyna może bez uszkadzania komórek bezpośrednio unieszkodliwiać niektóre z najsilniejszych sygnałów zapalnych organizmu. Wyniki wzmacniają argument za przetestowaniem atorwastatyny, a być może także jej bliskich chemicznych krewnych, jako niedrogich i szeroko dostępnych terapii przewlekłych stanów zapalnych, uzupełniających ich ustaloną rolę w ochronie serca.
Cytowanie: Swaroop, K., M., R., Shaik, S. et al. Evaluation of the anti-inflammatory potential of atorvastatin targeting TNF-α, IL-6, and IL-1β using integrated in vitro and in silico approaches. Sci Rep 16, 9914 (2026). https://doi.org/10.1038/s41598-026-39082-6
Słowa kluczowe: atorwastatyna, przewlekłe zapalenie, cytokiny, ponowne zastosowanie leków, TNF-alfa