Clear Sky Science · he
הערכת הפוטנציאל האנטי־דלקתי של אטורvastatin המכוון ל‑TNF‑α, IL‑6 ו‑IL‑1β באמצעות גישות משולבות במעבדה ובחישוב
מדוע תרופת הורדת כולסטרול חשובה לדלקת
מיליוני אנשים נוטלים אטורvastatin כדי להוריד את הכולסטרול ולהגן על הלב. המחקר הזה שואל שאלה מפתיעה: האם אותו גלולה עשויה גם להרגיע דלקת מזיקה ברחבי הגוף? על ידי שילוב של דגמי מחשב עם ניסויים בתאים, החוקרים בודקים האם אטורvastatin יכול להפחית במישרין שליחי דלקת רבי עוצמה שמניעים מחלות כמו דלקת מפרקים, סוכרת ומחלות לב.
כיצד מערכת האזעקה של הגוף עלולה לפעול נגדנו
דלקת היא מערכת האזעקה המובנית של הגוף, שמופעלת כשאנו נתקלים בזיהום או בפציעה. בטווח הקצר היא מגינה, מזמינה תאי חיסון ועוזרת לתקן רקמות. הבעיה נוצרת כשהאזעקה לא נסוגה. אז שליחים כימיים מרכזיים הנקראים ציטוקינים — ובמיוחד TNF‑alpha, IL‑6 ו‑IL‑1 beta — נשארים ברמות גבוהות ומשאירים את הגוף במצב מלחמה כרוני רדום. דלקת כרונית זו מקושרת למגוון רחב של מחלות, החל ממחלת מפרקים והצטברות שומנים בעורקים ועד להפרעות נוירולוגיות ומינים מסוימים של סרטן. מכיוון שתרופות חדשות לחלוטין איטיות ויקרות לפיתוח, מדענים מעוניינים לבדוק האם תרופות מבוססות כמו סטטינים ניתנות לשימוש חוזר כדי למקד אותות דלקת אלה.
חקר מפגשי תרופה‑חלבון במחשב
הצוות השתמש תחילה בסימולציות מחשב מתקדמות כדי לבחון כיצד אטורvastatin עשויה לתקשר פיזית עם שלושת הציטוקינים. הם ביצעו דוקינג מולקולרי, שיטה החוזה עד כמה מולקולה קטנה תסתדר על פני שטח של חלבון, ואחר כך הריצו סימולציות דינמיקות מולקולריות ארוכות כדי לצפות בהתנהגות המורכב לאורך זמן. אטורvastatin הציגה התאמה הדוקה ויציבה ביותר עם TNF‑alpha, כאשר היא יושבת באזור שטחי המשמש לקשירה לקולטן על תאים. המורכב הווירטואלי נשאר קומפקטי ויציב במהלך ריצת 200 ננו‑שניות, וחישובי אנרגיה הציעו כי כוחות משיכה בין אזורים הידרופוביים וטבעתיים של התרופה והחלבון תורמים רבות לקשירה.
בדיקת ההשפעה האנטי‑דלקתית בתאי חיסון
כדי לבדוק האם התחזיות מהמחשב מתורגמות לביולוגיה אמיתית, החוקרים פנו למודל מעבדתי סטנדרטי של דלקת. הם חשפו תאי מקרופאג של עכבר — תאי חיסון המסייעים לתיאום תגובות דלקתיות — למרכיב חיידקי שמפעיל אותם בעוצמה. לפני ההפעלה הזו, התאים טופלו במינונים שונים של אטורvastatin. התרופה לא פגעה בהישרדות התאים עד ריכוז של 20 מיקרומול, כלומר ההשפעות לא נבעו מטוקסיות. ככל שהמינון עלה, התאים שחררו פחות ויותר של TNF‑alpha, IL‑6 ו‑IL‑1 beta לסביבה שלהם. במינון הגבוה ביותר, רמות שליחי הדלקת צנחו באופן חד. בנוסף, אטורvastatin צמצמה גם את ייצור חנקן חד‑חמצני, מולקולה שנוטה לעלות בדלקת ויכולה לפגוע ברקמות כשמייצרים אותה בכמות מופרזת.
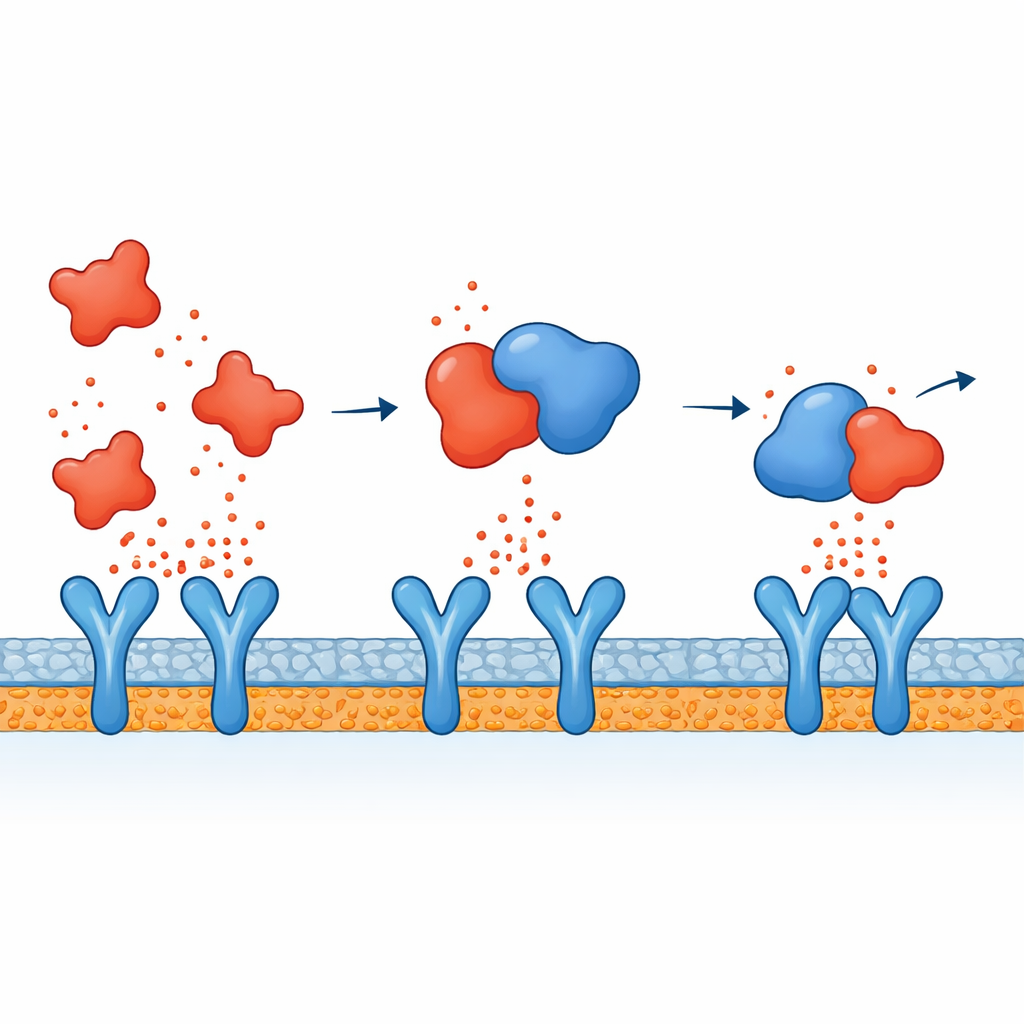
קישור בין קשירת המולקולה להירגעות האיתות
בהרכבת הממצאים, המחברים מציעים מנגנון דו‑חרצי לפעולת אטורvastatin. בתוך תאי החיסון, נראה שהיא מרפה את מסלולי האותות שבאופן רגיל מדליקים גנים דלקתיים אחרי איום מיקרוביאלי, כך שמיוצרים פחות ציטוקינים מלכתחילה. במקביל, הסימולציות מרמזות כי ציטוקינים שמצליחים להימלט אל זרם הדם עלולים להיות מנוטרלים בחלקם כי אטורvastatin נקשרת אליהם במישרין, במיוחד ל‑TNF‑alpha, וכך מקשה עליהם להקשר לקולטנים ולהעביר את האות. השילוב הזה עשוי להסביר מדוע נצפו סטטינים בהפחתת מדדי דלקת בחולים, מעבר להשפעתם המוכרת על הכולסטרול.
מה משמעות הדבר לחולים
לקורא כללי, המסקנה המרכזית היא שתרופה מוכרת להורדת כולסטרול עשויה גם לפעול כמווסת דלקת רב‑תכליתי. בעוד שהעבודה בוצעה בדגמי מחשב ובתרביות תאים — ולא עדיין בחולים — היא מציעה תמונה מולקולרית מפורטת של איך אטורvastatin עשוי לנטרל ישירות כמה מהאותות הדלקתיים החזקים בגוף בלי לפגוע בתאים. הממצאים מחזקים את הבסיס לבחינת אטורvastatin, ואולי גם תרכובות קרובות מבחינה כימית, כטיפולים זולים ונגישים למצבים דלקתיים כרוניים, לצד תפקידם המוסכם בהגנה על הלב.
ציטוט: Swaroop, K., M., R., Shaik, S. et al. Evaluation of the anti-inflammatory potential of atorvastatin targeting TNF-α, IL-6, and IL-1β using integrated in vitro and in silico approaches. Sci Rep 16, 9914 (2026). https://doi.org/10.1038/s41598-026-39082-6
מילות מפתח: אטורvastatin, דלקת כרונית, ציטוקינים, שימוש מחדש בתרופות, TNF‑alpha