Clear Sky Science · pt
Células linfoides inatas imaturas infiltrantes de tumor no câncer colorretal mostram viés para diferenciação ILC1/células NK residentes de tecido
Por que nossas próprias defesas importam no câncer de cólon
O câncer colorretal está entre os mais letais do mundo e, quando se espalha para o revestimento do abdome — chamado metástase peritoneal — torna-se especialmente difícil de tratar. Cirurgia e quimioterapia beneficiam alguns pacientes, mas muitos não respondem aos medicamentos imunomoduladores atuais. Este estudo vai além das conhecidas células T e foca em células imunes menos estudadas, chamadas células linfoides inatas e células natural killer. Ao mapear o comportamento dessas células dentro dos tumores, os pesquisadores revelam novas formas pelas quais o organismo pode tentar — e às vezes falhar — em combater o câncer colorretal, apontando para terapias futuras que possam aproveitar melhor nossas próprias defesas.
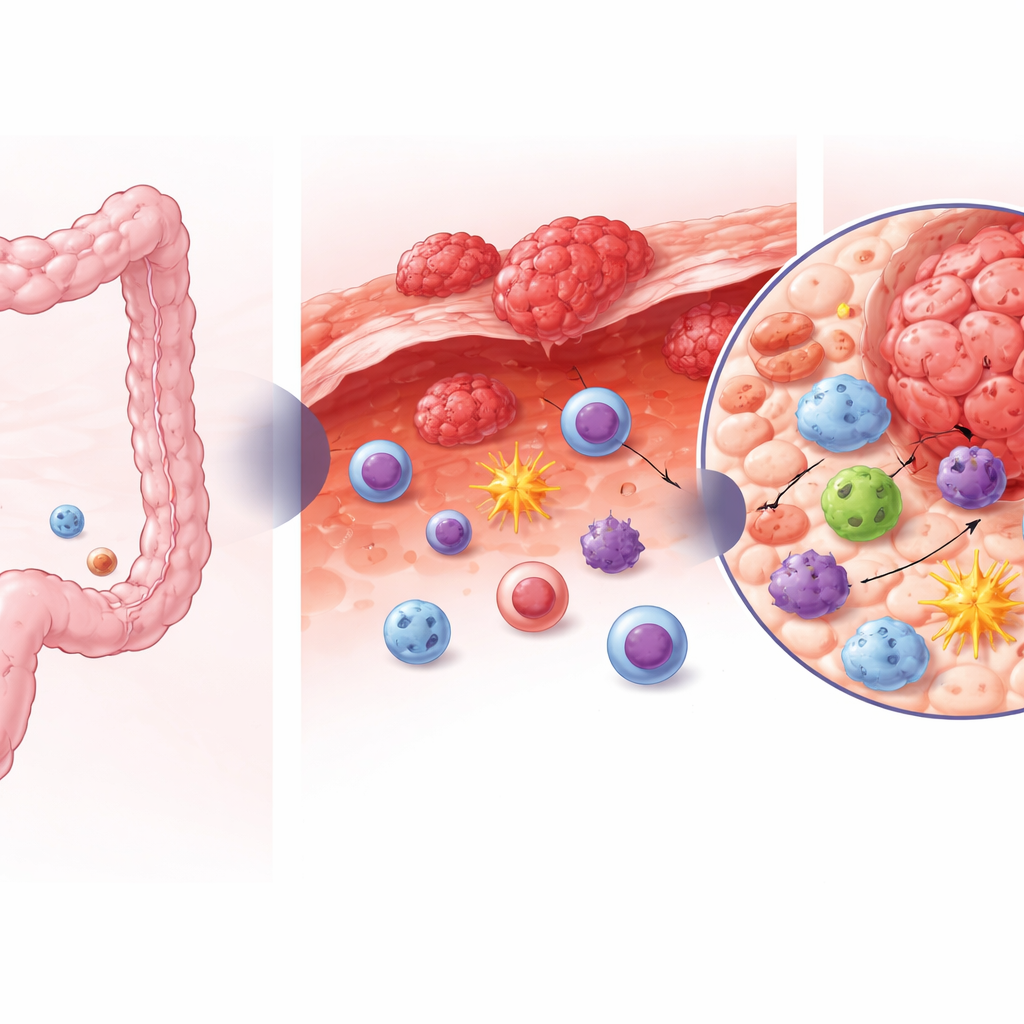
Os atores ocultos na defesa contra tumores
No interior de um cólon saudável, o epitélio é patrulhado por uma mistura de células linfoides inatas que ajudam a manter o equilíbrio com os micróbios intestinais e a reparar tecidos. Entre elas, um grupo (frequentemente chamado de ILC3) contribui para a integridade da parede intestinal e pode proteger contra o câncer. Os autores coletaram amostras de tecido de cólon saudável, tumores colorretais primários e metástases peritoneais de pacientes submetidos à cirurgia. Usando sequenciamento de RNA em célula única e perfis celulares detalhados, eles analisaram mais de 23.000 células linfoides inatas e células assassinas, permitindo observar, célula a célula, quais tipos estavam presentes e quais genes estavam sendo ativados.
Como os tumores remodelam o panorama imune
A equipe constatou que os tumores, tanto no cólon quanto no peritônio, remodelavam profundamente esse panorama imune. Em comparação com o cólon saudável, os tumores apresentavam depleção das células ILC3 protetoras da mucosa, mas exibiam abundância de vários tipos de células com características de assassinas: diferentes variantes de células linfoides inatas tipo 1 e tanto células NK residentes de tecido quanto células NK convencionais. Essas populações enriquecidas no tumor mostraram misturas de traços: algumas se assemelhavam a células assassinas típicas circulantes, enquanto outras portavam marcadores de células que se estabelecem nos tecidos a longo prazo. Essa mudança sugere que, à medida que o câncer colorretal se desenvolve e se dissemina, há um favorecimento de células imunes semelhantes a assassinas residentes, com perda daquelas que normalmente sustentam a saúde da barreira intestinal.
Células imaturas prontas para se tornarem assassinas locais
Em meio a esse conjunto, os cientistas identificaram duas populações “imaturas” que parecem atuar como precursores locais. Uma, chamada células linfoides inatas naïve, e outra, apelidada de células NK precoces, compartilhavam assinaturas gênicas associadas a células jovens e flexíveis que ainda podem escolher seu destino. Ao rastrear mudanças na expressão gênica ao longo de um “pseudotempo” computacional, os autores mostraram que essas células imaturas ocupavam o início de trajetórias de desenvolvimento que terminavam em células mais especializadas, tanto assassinas quanto residentes de tecido. Nos tumores, as células naïve apresentaram viés para se tornarem ILC1-like e células NK residentes de tecido, em vez do tipo ILC3 protetor do intestino visto com mais frequência no cólon saudável, sugerindo que o ambiente tumoral as direciona para uma identidade mais parecida com assassinas.
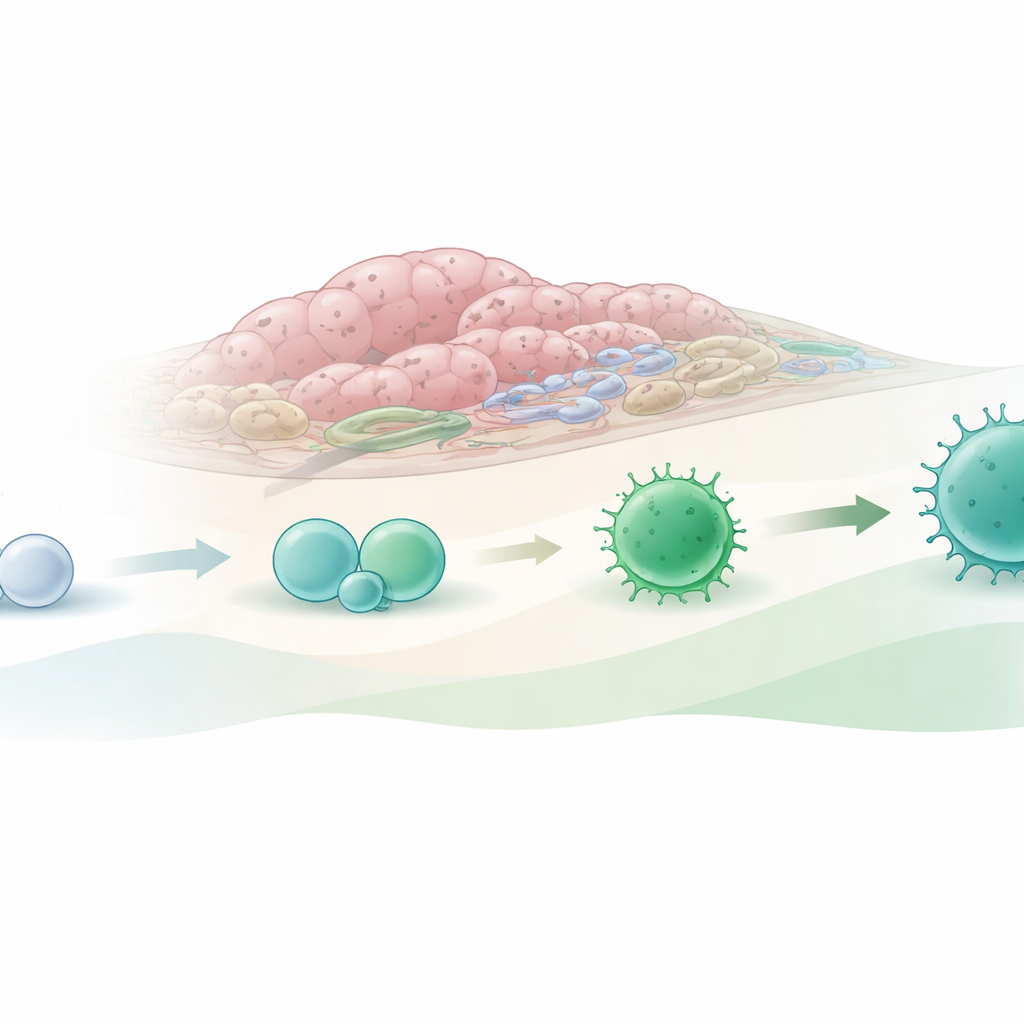
Testando como o ambiente tumoral orienta o destino
Para testar essa hipótese, a equipe isolou essas células imaturas tanto do cólon saudável quanto dos tumores e as cultivou no laboratório com células “enfermeiras” de suporte e diferentes combinações de proteínas sinalizadoras. Quando células naïve oriundas de tumores foram cultivadas em condições que imitam sinais presentes no tecido canceroso, elas mais prontamente se diferenciaram em células com características de células assassinas residentes de tecido: passaram a expressar mais moléculas ligadas à atividade citotóxica e à permanência a longo prazo nos tecidos. Em alguns cenários, também mostraram maior tendência a gerar células semelhantes a outro subconjunto linfoide inato, ILC2, que tem sido implicado tanto no crescimento tumoral quanto no controle do tumor. Ao cocultivar os precursores imaturos com uma linhagem humana de câncer colorretal, precursores derivados de cólon e de tumor puderam se tornar células com traços assassinos, ressaltando o quão fortemente o microambiente tumoral orienta seu desenvolvimento.
O que isso significa para tratamentos futuros
Essas descobertas revelam que tumores colorretais não são meros alvos passivos; eles remodelam ativamente as células imunes inatas próximas, atraindo precursores imaturos e viésando-os para estados de células assassinas residentes de tecido. Embora essas células possuam maquinaria para atacar o câncer, o ambiente tumoral também pode atenuar sua eficácia. Compreender como células linfoides inatas naïve e células NK precoces são guiadas dentro dos tumores abre várias possibilidades terapêuticas: reforçar sinais que as empurrem para estados assassinos potentes e de longa duração, ou mesmo coletar e reprogramar esses precursores locais para terapias celulares personalizadas. Para pacientes com câncer colorretal avançado ou metastático, especialmente aqueles que não respondem às terapias imunológicas atuais, este trabalho oferece um roteiro para novas estratégias que trabalhem com — e não contra — os sentinelas celulares do próprio corpo.
Citação: Marchalot, A., Ljunggren, M., Stamper, C. et al. Tumor-infiltrating immature innate lymphoid cells in colorectal cancer are biased toward ILC1/tissue-resident NK cell differentiation. Nat Commun 17, 3035 (2026). https://doi.org/10.1038/s41467-026-71085-9
Palavras-chave: câncer colorretal, células linfoides inatas, células natural killer, microambiente tumoral, imunoterapia