Clear Sky Science · de
Tumorinfiltrierende unreife angeborene lymphoide Zellen bei kolorektalem Krebs sind zugunsten einer ILC1-/gewebsansässigen NK-Zell-Differenzierung verschoben
Warum unsere eigenen Abwehrkräfte beim Darmkrebs wichtig sind
Kolorektales Karzinom gehört zu den tödlichsten Krebsarten weltweit; breitet es sich in die Bauchfellauskleidung aus (Peritonealmetastasen), wird die Behandlung besonders schwierig. Operation und Chemotherapie helfen einigen Patientinnen und Patienten, doch viele profitieren nicht von den heute verfügbaren immunbasierten Therapien. Diese Studie blickt über die bekannten T‑Zellen hinaus und richtet den Fokus auf weniger bekannte Immunzellen: angeborene lymphoide Zellen und natürliche Killerzellen. Durch die Kartierung ihres Verhaltens innerhalb von Tumoren decken die Forschenden neue Wege auf, wie der Körper versucht — und mitunter scheitert —, kolorektalen Krebs zu bekämpfen, und zeigen Ansätze für künftige Therapien, die unsere eigenen Abwehrkräfte gezielter nutzen könnten.
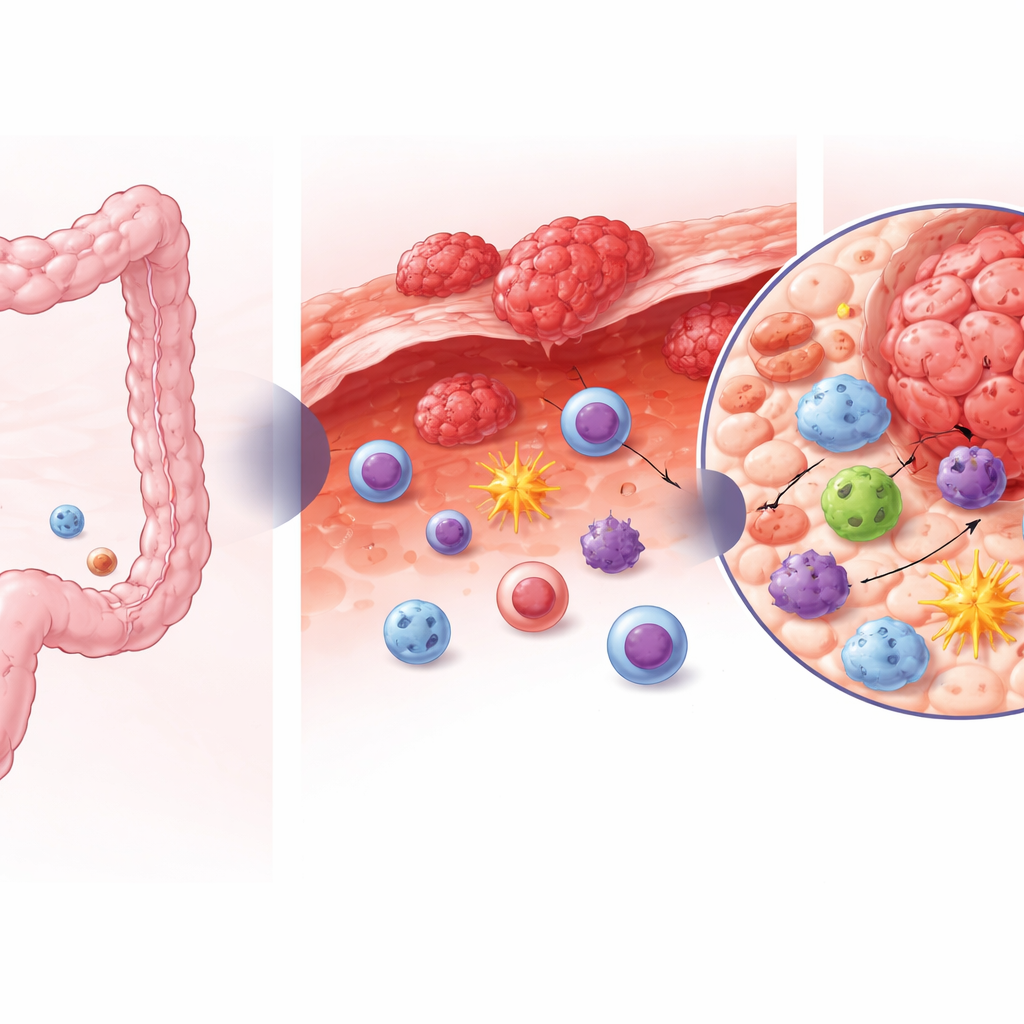
Die verborgenen Akteure der Tumorabwehr
In einem gesunden Darm wird die Schleimhaut von einem Gemisch angeborener lymphoider Zellen überwacht, die das Gleichgewicht mit der Darmflora erhalten und Gewebe reparieren. Unter ihnen trägt eine Gruppe (häufig ILC3 genannt) dazu bei, die Darmwand gesund zu halten und möglicherweise vor Krebs zu schützen. Die Autorinnen und Autoren entnahmen Proben aus gesundem Darmgewebe, primären kolorektalen Tumoren und Peritonealmetastasen von operierten Patientinnen und Patienten. Mit Einzelzell-RNA-Sequenzierung und detaillierter Zellcharakterisierung analysierten sie mehr als 23.000 angeborene lymphoide und Killerzellen, sodass sie zellengenau feststellen konnten, welche Zelltypen vorhanden waren und welche Gene aktiviert wurden.
Wie Tumoren die Immunlandschaft umgestalten
Das Team fand heraus, dass Tumoren im Darm und im Peritoneum die Immunlandschaft tiefgreifend verändern. Im Vergleich zum gesunden Darm waren Tumoren arm an den darm-schützenden ILC3-Zellen, dafür aber reich an verschiedenen killerähnlichen Zelltypen: unterschiedlichen Varianten angeborener lymphoider Typ‑1‑Zellen sowie sowohl gewebsansässigen als auch konventionellen natürlichen Killerzellen. Diese tumorangereicherten Zellen zeigten Mischmerkmale: einige erinnerten an typische im Blut zirkulierende Killerzellen, andere trugen Marker von Zellen, die langfristig in Geweben verweilen. Dieser Wandel legt nahe, dass bei Entstehung und Ausbreitung kolorektalen Krebses Zellen bevorzugt werden, die residenten Killerzellen ähneln, während Zellen verloren gehen, die normalerweise die Barrierefunktion unterstützen.
Unreife Zellen, bereit, zu lokalen Killern zu werden
Zwischen dieser Vielfalt entdeckten die Wissenschaftler zwei „unreife“ Populationen, die offenbar als lokale Vorläufer fungieren. Die eine bezeichneten sie als naive angeborene lymphoide Zellen, die andere als frühe NK‑Zellen; beide wiesen Genprofile auf, die mit jungen, noch formbaren Zellen assoziiert sind, die ihre weitere Differenzierung noch wählen können. Durch das Nachverfolgen von Genexpressionsänderungen entlang eines computationalen «Pseudotimes» zeigten die Autorinnen und Autoren, dass diese unreifen Zellen am Anfang von Entwicklungsverläufen standen, die in spezialisiertere Killer‑ und gewebsansässige Zelltypen mündeten. In Tumoren tendierten die naiven Zellen eher dazu, ILC1‑ähnliche und gewebsansässigen NK‑ähnlichen Zellen zu werden, statt des darmprotektiven ILC3‑Typs, der im gesunden Darm häufiger vorkommt — ein Hinweis darauf, dass die Tumorumgebung sie in Richtung einer killerähnlichen Identität lenkt.
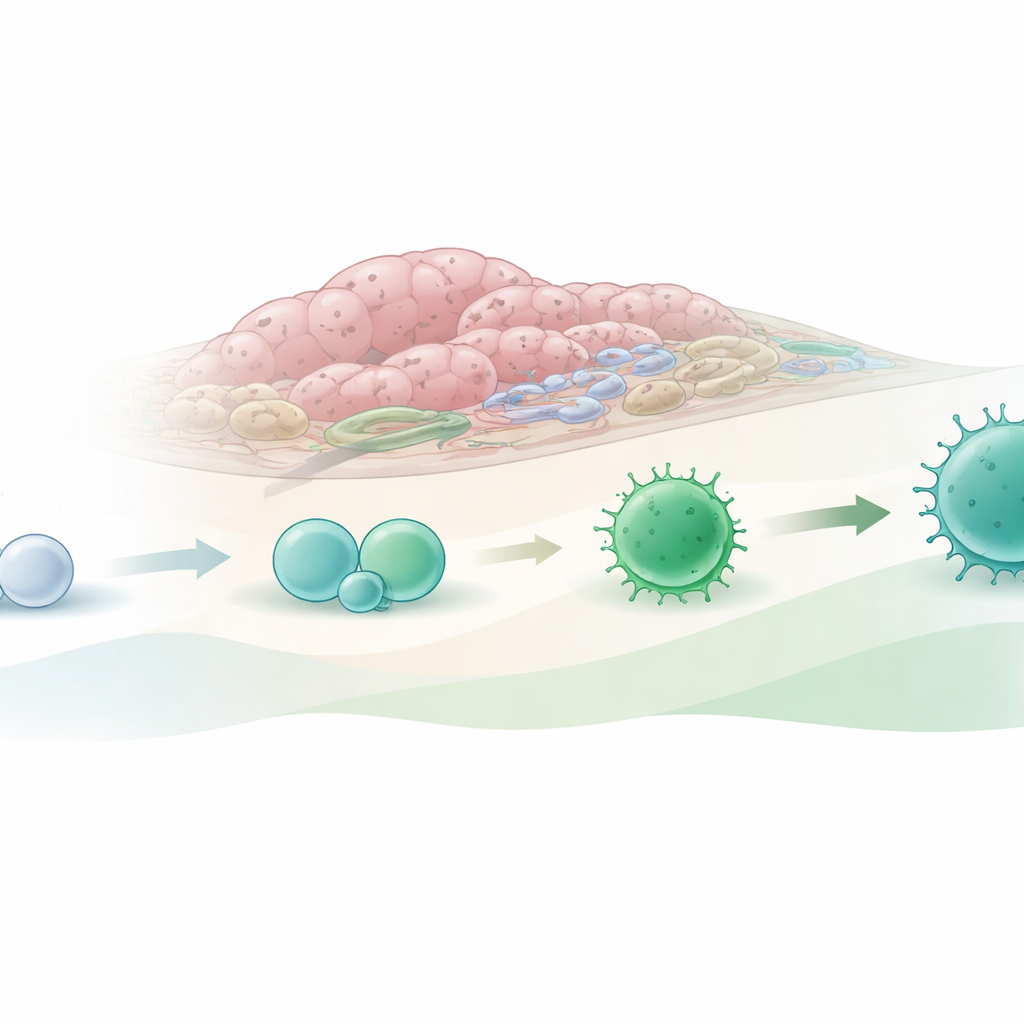
Tests, wie die Tumorumgebung die Zellschicksale steuert
Um diese Idee zu prüfen, isolierte das Team diese unreifen Zellen aus gesundem Darm und aus Tumoren und kultivierte sie im Labor mit unterstützenden „Nurse“-Zellen und verschiedenen Kombinationen von Signalmolekülen. Wenn naive Zellen aus Tumoren unter Bedingungen kultiviert wurden, die Signale nachahmen, wie sie im Krebssgewebe vorkommen, differenzierten sie leichter in Zellen mit Merkmalen gewebsansässiger Killerzellen: Sie exprimierten mehr Moleküle, die mit zytotoxischer Aktivität und langfristigem Verbleib im Gewebe verbunden sind. In einigen Konstellationen zeigten sie auch eine erhöhte Neigung, Zellen zu erzeugen, die einem anderen angeborenen lymphoiden Subtyp, ILC2, ähneln — ein Subtyp, der sowohl mit Tumorwachstum als auch mit Tumorkontrolle in Verbindung gebracht wurde. Beim Co‑Kultivieren der unreifen Zellen mit einer humanen kolorektalen Krebszelllinie konnten sowohl aus dem gesunden Darm als auch aus Tumoren stammende Vorläufer zu killerähnlichen Zellen werden, was unterstreicht, wie stark die lokale Tumorumgebung ihre Entwicklung steuert.
Was das für künftige Behandlungen bedeutet
Die Ergebnisse zeigen, dass kolorektale Tumoren nicht nur passive Ziele sind, sondern die umliegenden angeborenen Immunzellen aktiv umgestalten: Sie rekrutieren unreife Vorläufer und lenken deren Differenzierung zugunsten gewebsansässiger Killerzustände. Zwar verfügen diese Zellen über die Werkzeuge, Krebs anzugreifen, doch die Tumorumgebung kann ihre Effektivität dämpfen. Das Verständnis, wie naive angeborene lymphoide und frühe NK‑Zellen in Tumoren gelenkt werden, eröffnet mehrere therapeutische Möglichkeiten: die Stärkung von Signalen, die sie in potente, langlebige tumorabtötende Zellen treiben, oder sogar das Ernten und Umprogrammieren dieser lokalen Vorläufer für personalisierte Zelltherapien. Für Patientinnen und Patienten mit fortgeschrittenem oder metastasiertem kolorektalem Krebs — insbesondere jene, die nicht auf aktuelle Immuntherapien ansprechen — bietet diese Arbeit eine Orientierung für neue Strategien, die mit den zellulären Schutzsystemen des Körpers zusammenarbeiten statt gegen sie.
Zitation: Marchalot, A., Ljunggren, M., Stamper, C. et al. Tumor-infiltrating immature innate lymphoid cells in colorectal cancer are biased toward ILC1/tissue-resident NK cell differentiation. Nat Commun 17, 3035 (2026). https://doi.org/10.1038/s41467-026-71085-9
Schlüsselwörter: kolorektales Karzinom, angeborene lymphoide Zellen, natürliche Killerzellen, Tumormikroumgebung, Immuntherapie