Clear Sky Science · pl
Niedojrzałe naciekające nowotwór wrodzone komórki limfoidalne w raku jelita grubego wykazują skłonność do różnicowania w kierunku ILC1/komórek NK rezydentnych w tkance
Dlaczego nasze własne mechanizmy obronne mają znaczenie w raku jelita grubego
Rak jelita grubego jest jednym z najbardziej śmiertelnych nowotworów na świecie, a kiedy rozprzestrzenia się na otrzewną — tzw. przerzuty otrzewnowe — staje się szczególnie trudny w leczeniu. Chirurgia i chemioterapia pomagają niektórym pacjentom, ale wielu nie odnosi korzyści z dostępnych dziś leków immunologicznych. W tym badaniu autorzy wychodzą poza dobrze znane limfocyty T i koncentrują się na mniej rozpoznanych komórkach odpornościowych, zwanych wrodzonymi komórkami limfoidalnymi i komórkami NK. Mapując zachowanie tych komórek wewnątrz guzów, badacze ujawniają nowe sposoby, w jakie organizm może próbować — i czasem zawodnie — walczyć z rakiem jelita grubego, wskazując na kierunki przyszłych terapii, które mogłyby lepiej wykorzystać nasze własne mechanizmy obronne.
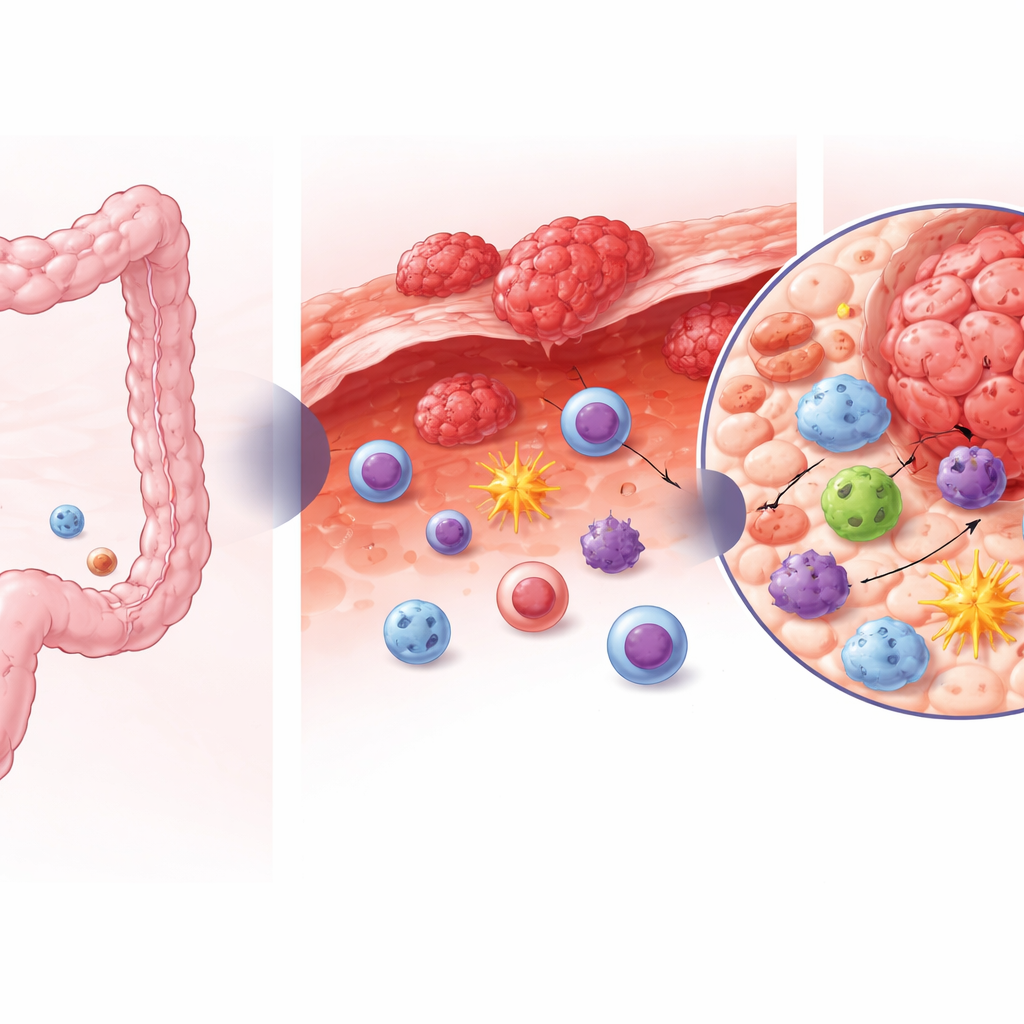
Ukryci gracze w obronie przed guzem
W zdrowym jelicie wyściółka jest patrolowana przez mieszaninę wrodzonych komórek limfoidalnych, które pomagają utrzymać równowagę z mikrobiotą jelitową i naprawiać tkankę. Wśród nich jedna grupa (często określana jako ILC3) wspiera zdrowie ściany jelita i może chronić przed rakiem. Autorzy zebrali próbki ze zdrowej tkanki jelita, z pierwotnych guzów jelita grubego oraz z przerzutów otrzewnowych od pacjentów poddawanych operacji. Wykorzystując sekwencjonowanie RNA pojedynczych komórek oraz szczegółowe profilowanie komórek, przeanalizowali ponad 23 000 wrodzonych komórek limfoidalnych i komórek zabójczych, co pozwoliło im zobaczyć, komórka po komórce, jakie typy występowały i jakie geny były w nich aktywowane.
Jak guzy przekształcają krajobraz odpornościowy
Zespół stwierdził, że guzy, zarówno w jelicie, jak i w otrzewnej, głęboko przekształcają ten krajobraz odpornościowy. W porównaniu ze zdrowym jelitem guzy były pozbawione ochronnych dla jelita komórek ILC3, za to obfitowały w kilka rodzajów komórek o cechach zabójczych: różne odmiany wrodzonych komórek limfoidalnych typu 1 oraz zarówno rezydentne w tkance, jak i konwencjonalne komórki NK. Komórki wzbogacone w guzach wykazywały mieszankę cech: niektóre przypominały typowe krążące we krwi komórki zabójcze, inne nosiły markery charakterystyczne dla komórek osiedlających się w tkankach na dłużej. Ta zmiana sugeruje, że w miarę rozwoju i rozsiewu raka jelita grubego faworyzowane są komórki przypominające rezydentne komórki zabójcze, przy jednoczesnej utracie tych, które normalnie wspierają integralność bariery jelitowej.
Niedojrzałe komórki gotowe, by stać się lokalnymi zabójcami
Wśród tego tłumu naukowcy odkryli dwie populacje „niedojrzałych” komórek, które wydają się pełnić rolę lokalnych prekursorów. Jedna, określana jako naiwny wrodzony komórki limfoidalne, a druga, nazwana wczesnymi komórkami NK, dzieliły sygnatury genowe związane z młodymi, plastycznymi komórkami, które wciąż mogą wybrać swoją drogę rozwojową. Śledząc zmiany ekspresji genów w tzw. pseudoczase obliczeniowym, autorzy pokazali, że te niedojrzałe komórki znajdują się na początku szlaków rozwojowych, które kończą się wyspecjalizowanymi komórkami zabójczymi i rezydentnymi w tkance. W guzach komórki naiwnych były skłonne różnicować się w kierunku komórek podobnych do ILC1 i rezydentnych komórek NK, zamiast w stronę ochronnych dla jelita komórek ILC3, częściej widywanych w zdrowym jelicie, co sugeruje, że mikrośrodowisko guza skłania je ku tożsamości zabójczej.
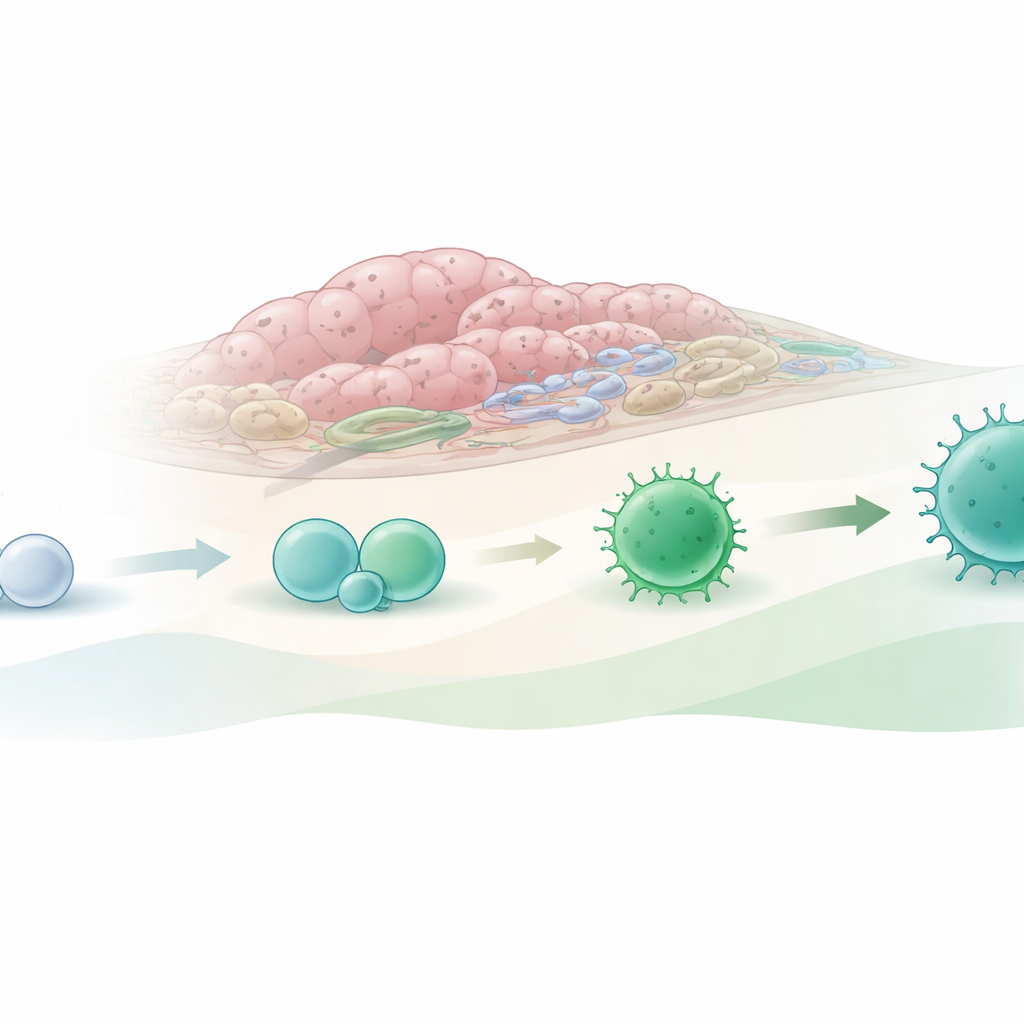
Testowanie, jak środowisko guza kieruje losem komórek
Aby sprawdzić tę hipotezę, zespół izolował te niedojrzałe komórki ze zdrowego jelita i z guzów, a następnie hodował je w laboratorium z podporowymi „komórkami pielęgniarki” i różnymi kombinacjami białek sygnałowych. Gdy naiwny komórki pochodzące z guzów były hodowane w warunkach naśladujących sygnały obecne w tkance nowotworowej, łatwiej przekształcały się w komórki noszące cechy rezydentnych komórek zabójczych: wykazywały większą ekspresję cząsteczek powiązanych z aktywnością cytotoksyczną i długotrwałym osiedlaniem się w tkankach. W niektórych warunkach obserwowano też zwiększoną tendencję do powstawania komórek przypominających inną podgrupę wrodzonych komórek limfoidalnych, ILC2, która bywa wiązana zarówno ze wspieraniem wzrostu guza, jak i jego kontrolą. Gdy badacze współhodowali niedojrzałe komórki z ludzką linią komórek raka jelita grubego, prekursory pochodzące i z jelita, i z guza mogły stać się komórkami o cechach zabójczych, co podkreśla, jak silnie lokalne mikrośrodowisko guza kieruje ich rozwojem.
Co to oznacza dla przyszłych terapii
Wyniki te pokazują, że guzy jelita grubego nie są jedynie biernymi celami; aktywnie przekształcają pobliskie wrodzone komórki odpornościowe, przyciągając niedojrzałe prekursory i kierując je ku stanom rezydentnych komórek zabójczych. Chociaż te komórki posiadają narzędzia do atakowania nowotworu, mikrośrodowisko guza może także tłumić ich skuteczność. Zrozumienie, jak naiwny wrodzone komórki limfoidalne i wczesne komórki NK są kierowane wewnątrz guzów, otwiera kilka możliwości terapeutycznych: wzmacnianie sygnałów, które popychają je w stronę silnych, długowiecznych komórek zabójczych, lub nawet pozyskiwanie i przeprogramowywanie tych lokalnych prekursorów do spersonalizowanych terapii komórkowych. Dla pacjentów z zaawansowanym lub rozsianym rakiem jelita grubego, zwłaszcza tych, którzy nie reagują na obecne leki immunologiczne, ta praca daje mapę drogową do nowych strategii współpracujących, a nie walczących, z własnymi komórkowymi strażnikami organizmu.
Cytowanie: Marchalot, A., Ljunggren, M., Stamper, C. et al. Tumor-infiltrating immature innate lymphoid cells in colorectal cancer are biased toward ILC1/tissue-resident NK cell differentiation. Nat Commun 17, 3035 (2026). https://doi.org/10.1038/s41467-026-71085-9
Słowa kluczowe: rak jelita grubego, wrodzone komórki limfoidalne, komórki natural killer, mikrośrodowisko guza, immunoterapia