Clear Sky Science · es
Las células linfoides innatas inmaduras infiltrantes en tumores de cáncer colorrectal están sesgadas hacia la diferenciación ILC1/células NK residentes en tejido
Por qué importan nuestras propias defensas en el cáncer de colon
El cáncer colorrectal es uno de los más mortales del mundo y, cuando se disemina al revestimiento del abdomen, lo que se conoce como metástasis peritoneal, resulta especialmente difícil de tratar. La cirugía y la quimioterapia ayudan a algunos pacientes, pero muchos no se benefician de los fármacos inmunitarios actuales. Este estudio va más allá de las bien conocidas células T y se centra en células inmunitarias menos estudiadas: las células linfoides innatas y las células asesinas naturales. Al cartografiar cómo se comportan estas células dentro de los tumores, los investigadores revelan nuevas formas en que el cuerpo puede intentar —y a veces fracasar— en la lucha contra el cáncer colorrectal, apuntando a futuras terapias que podrían aprovechar mejor nuestras propias defensas.
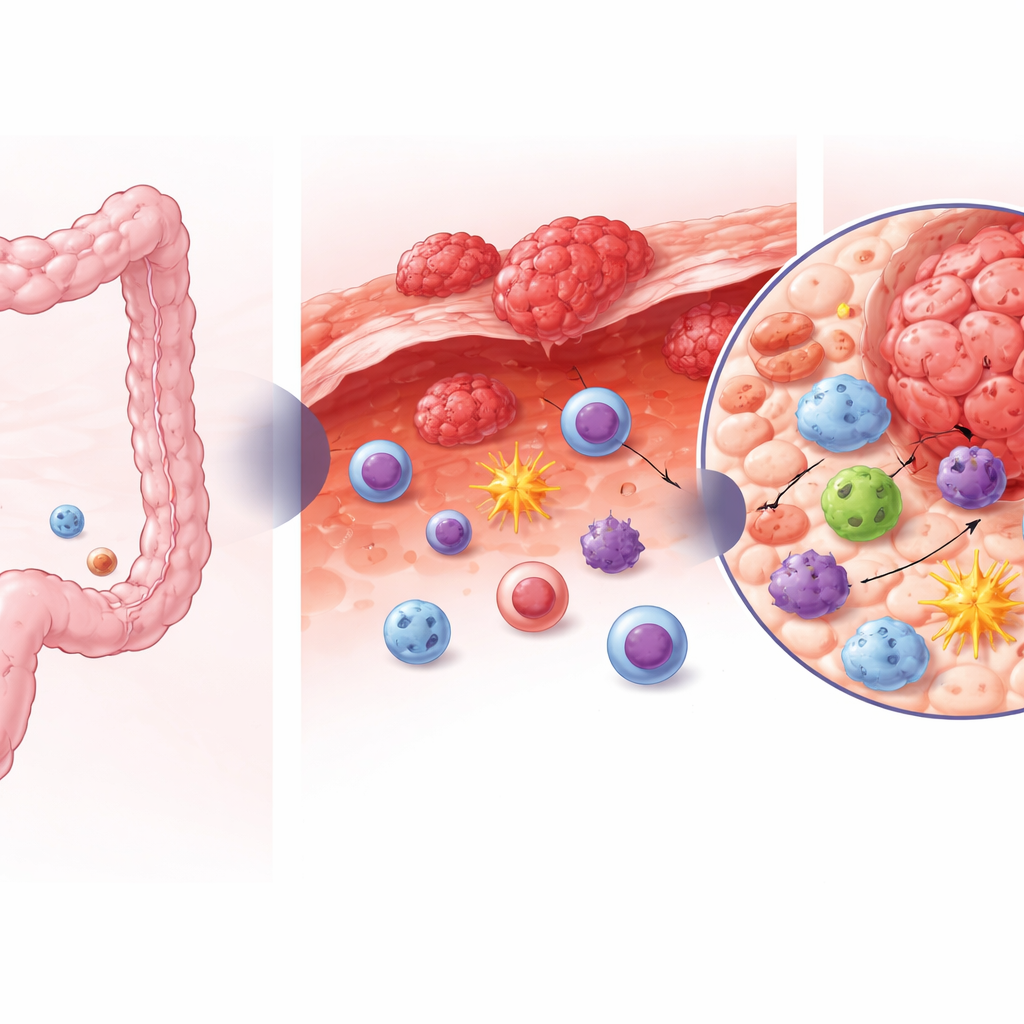
Los actores ocultos en la defensa contra el tumor
En el interior de un colon sano, el epitelio está patrullado por una mezcla de células linfoides innatas que ayudan a mantener el equilibrio con los microbios intestinales y a reparar el tejido. Entre ellas, un grupo (a menudo denominado ILC3) contribuye a conservar la salud de la pared intestinal y puede proteger frente al cáncer. Los autores recogieron muestras de tejido de colon sano, tumores colorrectales primarios y metástasis peritoneales de pacientes sometidos a cirugía. Usando secuenciación de ARN a nivel de célula única y perfiles celulares detallados, analizaron más de 23.000 células linfoides innatas y células asesinas, lo que les permitió ver, célula por célula, qué tipos estaban presentes y qué genes activaban.
Cómo los tumores remodelan el paisaje inmune
El equipo halló que los tumores, tanto en el colon como en el peritoneo, remodelan profundamente este paisaje inmunitario. En comparación con el colon sano, los tumores estaban empobrecidos en células ILC3 protectoras de la mucosa, pero llenos de varios tipos de células de aspecto asesino: distintas variantes de células linfoides innatas tipo 1 y tanto células NK residentes en tejido como convencionales. Estas poblaciones enriquecidas en el tumor mostraban mezclas de rasgos: algunas se asemejaban a las células asesinas circulantes típicas, mientras que otras exhibían marcadores de células que se establecen de forma duradera en los tejidos. Este cambio sugiere que, a medida que el cáncer colorrectal se desarrolla y se disemina, favorece células inmunitarias que recuerdan a asesinos residentes, perdiendo aquellas que normalmente mantienen la integridad de la barrera intestinal.
Células inmaduras preparadas para convertirse en asesinas locales
Entre esa multitud, los científicos identificaron dos poblaciones “inmaduras” que parecen actuar como precursores locales. Una, denominada células linfoides innatas naïve, y otra, llamadas células NK tempranas, compartían firmas génicas asociadas a células jóvenes y flexibles que aún pueden elegir su destino. Al rastrear los cambios en la expresión génica a lo largo de un “pseudotiempo” computacional, los autores mostraron que estas células inmaduras ocupaban el inicio de trayectorias de desarrollo que terminaban en células más especializadas, tanto asesinas como residentes en tejido. En los tumores, las células naïve estaban inclinadas a convertirse en células similares a ILC1 y a células NK residentes en tejido, en lugar del tipo ILC3 protector de la mucosa que se observa con más frecuencia en colon sano, lo que sugiere que el microambiente tumoral las empuja hacia una identidad de tipo asesino.
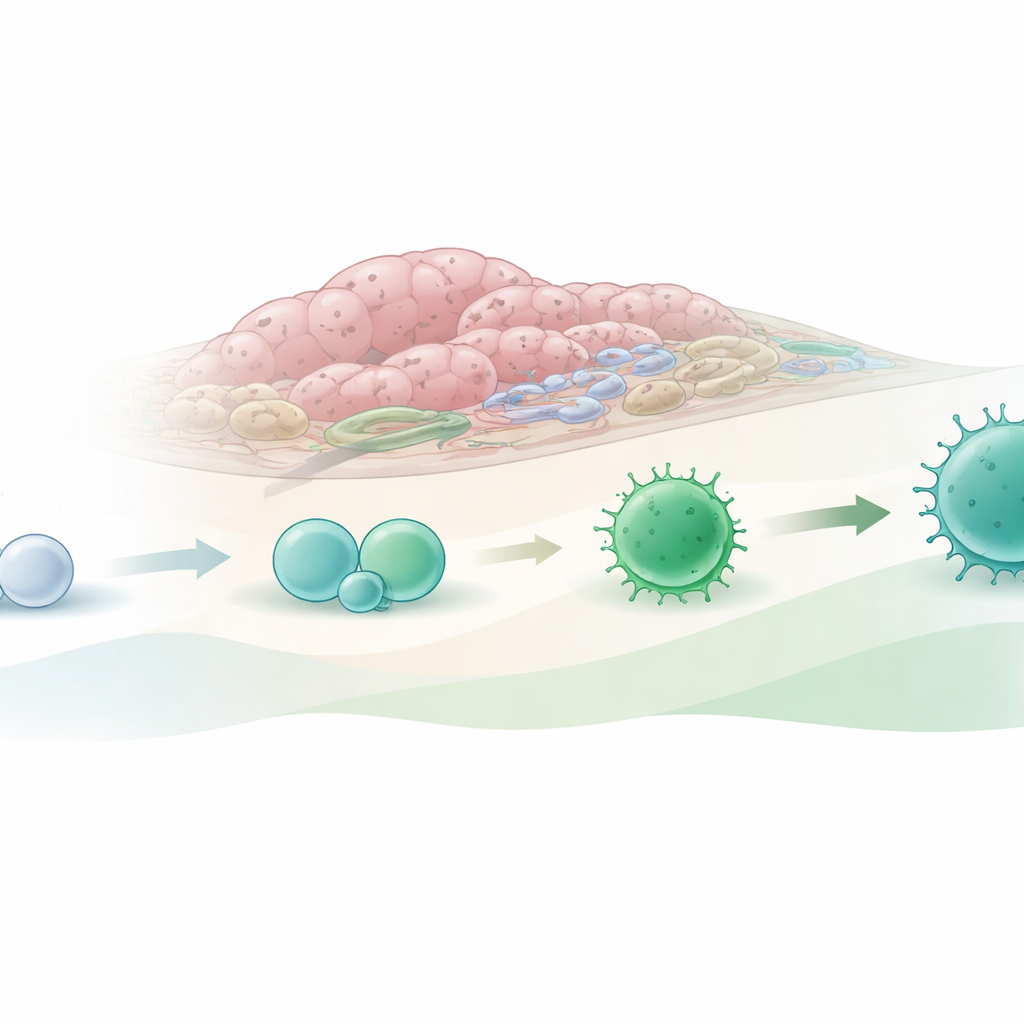
Comprobar cómo el entorno tumoral guía el destino
Para probar esta idea, el equipo aisló estas células inmaduras tanto de colon sano como de tumores y las cultivó en el laboratorio con células “nutridoras” de apoyo y distintas mezclas de proteínas señalizadoras. Cuando las células naïve procedentes de tumores se cultivaron bajo condiciones que imitan señales presentes en tejido canceroso, se diferenciaron más fácilmente en células con rasgos de células asesinas residentes en tejido: expresaban más moléculas relacionadas con la actividad citotóxica y con el asentamiento a largo plazo en los tejidos. En algunos contextos, también mostraron una mayor tendencia a generar células parecidas a otro subconjunto de células linfoides innatas, las ILC2, que se han implicado tanto en el crecimiento tumoral como en el control del tumor. Cuando los investigadores co-cultivaron las células inmaduras con una línea celular humana de cáncer colorrectal, tanto los precursores derivados del colon como los derivados del tumor podían convertirse en células de tipo asesino, lo que subraya lo decisivo que es el entorno tumoral local para orientar su desarrollo.
Qué significa esto para tratamientos futuros
Estos hallazgos revelan que los tumores colorrectales no son meros objetivos pasivos; remodelan activamente las células inmunitarias innatas cercanas, atrayendo precursores inmaduros y sesgándolos hacia estados de asesinos residentes en tejido. Aunque estas células disponen de la maquinaria para atacar el cáncer, el entorno tumoral también puede atenuar su efectividad. Comprender cómo las células linfoides innatas naïve y las células NK tempranas son guiadas dentro de los tumores abre varias posibilidades terapéuticas: potenciar las señales que las empujen hacia células citotóxicas potentes y de larga duración, o incluso extraer y reprogramar estos precursores locales para terapias celulares personalizadas. Para pacientes con cáncer colorrectal avanzado o diseminado, especialmente aquellos que no responden a los fármacos inmunitarios actuales, este trabajo ofrece una hoja de ruta hacia nuevas estrategias que trabajen con, en lugar de contra, los centinelas celulares del propio organismo.
Cita: Marchalot, A., Ljunggren, M., Stamper, C. et al. Tumor-infiltrating immature innate lymphoid cells in colorectal cancer are biased toward ILC1/tissue-resident NK cell differentiation. Nat Commun 17, 3035 (2026). https://doi.org/10.1038/s41467-026-71085-9
Palabras clave: cáncer colorrectal, células linfoides innatas, células asesinas naturales, microambiente tumoral, inmunoterapia