Clear Sky Science · pt
O canal sensível a ácido 1a modula comportamentos relacionados à ansiedade e depressão ao influenciar a atividade de neurônios que expressam o hormônio liberador de corticotropina no núcleo paraventricular hipotalâmico em camundongos machos
Como um interruptor minúsculo no cérebro molda nossos níveis de estresse
O estresse é parte conhecida da vida moderna, mas por baixo da superfície ele é conduzido por sinais elétricos e químicos precisos no cérebro. Este estudo em camundongos machos revela um componente antes invisível nesse sistema: um minúsculo canal “sensível ao ácido” em neurônios específicos que comandam o estresse. Ao mostrar como esse canal aumenta hormônios do estresse e comportamentos ansiosos ou depressivos — e como bloqueá‑lo acalma tanto o cérebro quanto o corpo — o trabalho aponta para novos tipos de tratamentos para ansiedade, depressão e outras doenças associadas ao estresse.
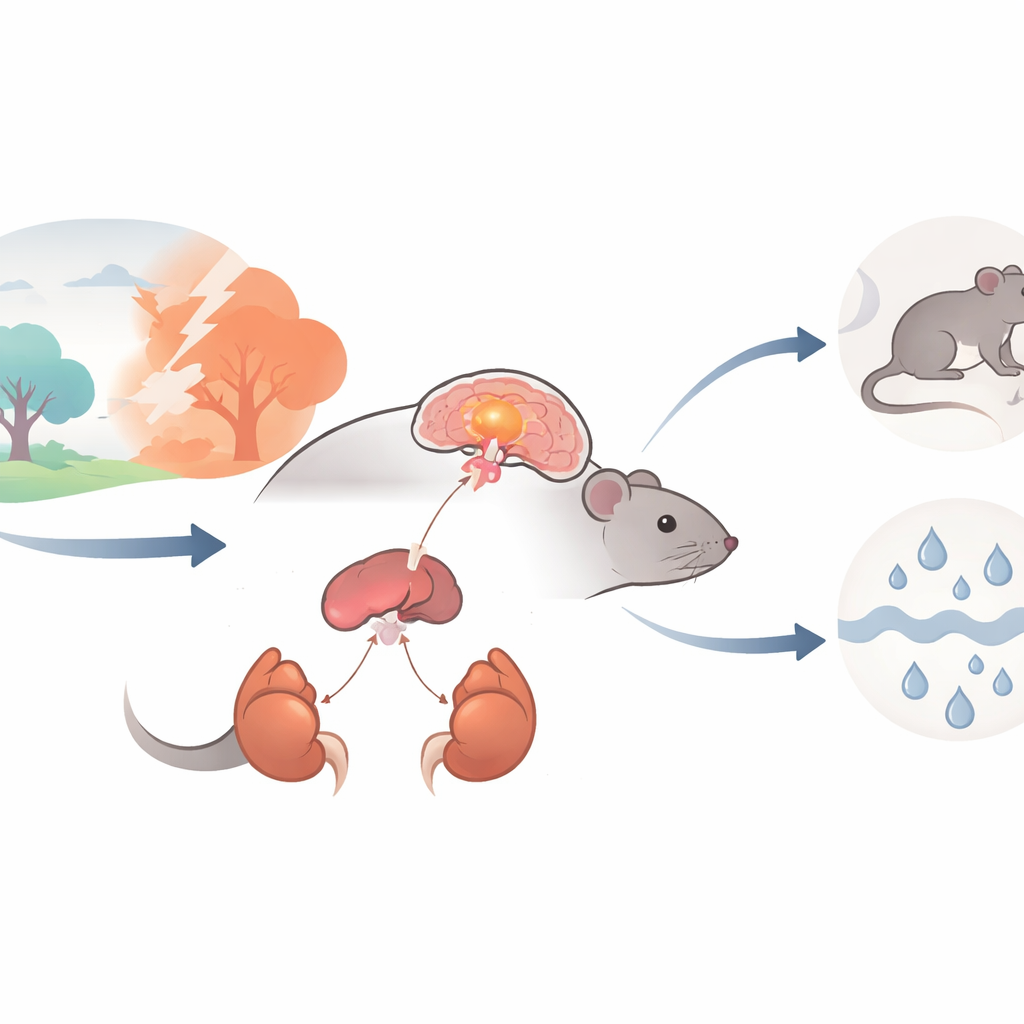
O principal alarme de estresse do corpo
Quando enfrentamos um desafio, uma cadeia de comando chamada eixo hipotálamo–hipófise–adrenal (HPA) entra em ação. Ela começa em uma pequena região do cérebro, o núcleo paraventricular hipotalâmico (PVN), onde células nervosas especiais liberam o hormônio liberador de corticotropina (CRH). O CRH sinaliza à hipófise, que então instrui as glândulas adrenais sobre os rins a inundarem a corrente sanguínea com hormônios do estresse, como a corticosterona. Esses hormônios são essenciais para a sobrevivência em picos de curta duração, mas se esse alarme for acionado com muita intensidade ou com muita frequência, pode contribuir para ansiedade, depressão, doenças metabólicas e hipertensão. Os autores investigaram se um canal iônico específico, chamado ASIC1a, dentro dos neurônios produtores de CRH do PVN ajuda a ajustar o ganho desse alarme de estresse.
Uma válvula oculta em neurônios do estresse
ASIC1a é um canal proteico na membrana celular que se abre quando o fluido ao redor se torna mais ácido, permitindo que íons carregados positivamente, incluindo cálcio, entrem rapidamente na célula. A equipe primeiro confirmou que ASIC1a é abundante nos neurônios produtores de CRH no PVN de camundongos. Em seguida, usaram duas estratégias complementares para reduzir a ação desse canal. Em uma, infundiram um bloqueador altamente seletivo de ASIC1a diretamente no PVN. Na outra, utilizaram vírus geneticamente modificados em camundongos CRH‑Cre para silenciar o gene ASIC1a especificamente nos neurônios que produzem CRH. Em ambos os casos, os camundongos exibiram comportamento menos ansioso nos testes de exploração e mostraram menos sinais semelhantes à depressão em ensaios comportamentais clássicos, mesmo que seu movimento e velocidade geral não tenham mudado. Ao mesmo tempo, os níveis sanguíneos dos hormônios do estresse ACTH e corticosterona após um estressor agudo caíram, enquanto os níveis basais permaneceram normais. Em conjunto, esses achados sugerem que ASIC1a não é necessário para a função ordinária, mas contribui para a reação exagerada ao estresse.
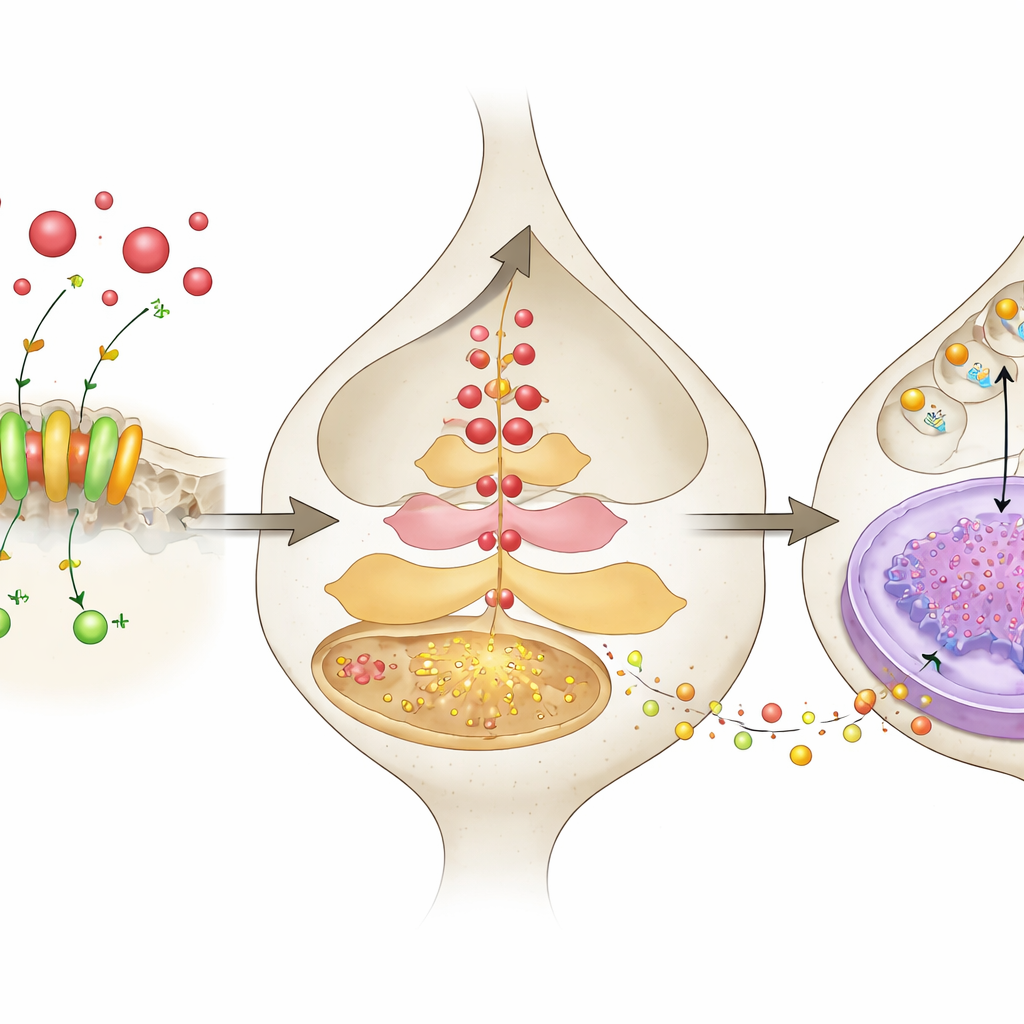
Dando zoom: de sinais ácidos à liberação de hormônios do estresse
Para investigar o que acontece dentro dos neurônios, os pesquisadores registraram a atividade de cálcio em tempo real de neurônios CRH do PVN usando um repórter fluorescente entregue por vírus e lido com fibras ópticas em camundongos acordados. Durante eventos estressantes, como um choque no pé ou nado forçado, neurônios com ASIC1a normal mostraram rajadas fortes de sinais de cálcio, enquanto neurônios sem ASIC1a responderam de forma muito mais fraca. Em culturas celulares, reduzir brevemente o pH da solução ao redor — imitando um ambiente mais ácido — aumentou fortemente a liberação de CRH, mas esse efeito foi atenuado quando ASIC1a foi bloqueado ou reduzido. O pulso ácido também elevou a produção de CRH dentro das células, tanto em níveis de proteína quanto de RNA mensageiro, novamente de modo dependente de ASIC1a. Esses experimentos conectam a acidez fora do neurônio, a abertura de ASIC1a, a entrada de cálcio e o aumento da produção de CRH como partes de uma única cascata.
O relé interno: uma cadeia de sinalização dirigida pelo cálcio
A equipe então dissecou a cadeia de sinalização entre a entrada de cálcio e a ativação do gene CRH. Quando ASIC1a foi estimulada por condições ácidas, os níveis de uma forma ativada da enzima CaMKII aumentaram, assim como os níveis de c‑Fos, um fator de transcrição de ação rápida conhecido por ativar genes relacionados ao estresse. Bloquear ASIC1a ou seu fluxo iônico reduziu essas mudanças. Usando um fármaco que interfere com o AP‑1, o complexo proteico que inclui c‑Fos, os pesquisadores atenuaram o aumento desencadeado pelo ácido na produção e liberação de CRH em neurônios cultivados. Infundir esse bloqueador de AP‑1 no PVN de camundongos também aliviou comportamentos semelhantes à ansiedade e depressão. Esses resultados apoiam um modelo no qual sinais de cálcio dirigidos por ASIC1a ativam CaMKII e c‑Fos, que então impulsionam o gene CRH para um patamar mais alto, amplificando a resposta ao estresse.
O que isso significa para tratamentos futuros
Em termos simples, o estudo identifica ASIC1a nos neurônios produtores de CRH do PVN como um “botão de volume” molecular na principal via cerebral do estresse. Quando ASIC1a está muito ativa, os neurônios do estresse disparam com mais força, os hormônios do estresse sobem mais e os animais exibem comportamentos mais ansiosos e semelhantes à depressão. Reduzir a atividade de ASIC1a — seja com ferramentas genéticas precisas ou com fármacos — suaviza essa reação sem desligar o comportamento normal. Embora o trabalho tenha sido realizado em camundongos machos e focado em estresse agudo, ele sugere que medicamentos que tenham como alvo ASIC1a ou seus parceiros de sinalização dirigidos pelo cálcio poderiam, no futuro, oferecer uma nova via para tratar transtornos relacionados ao estresse, como ansiedade, depressão e até algumas doenças metabólicas.
Citação: Yue, J., Zhang, Q., Wang, M. et al. The acid-sensing ion channel 1a modulates anxiety- and depression-related behaviors via its influencing on the activity of corticotropin-releasing hormone-expressing neurons in the hypothalamic paraventricular nucleus in male mice. Transl Psychiatry 16, 189 (2026). https://doi.org/10.1038/s41398-026-03946-2
Palavras-chave: resposta ao estresse, canais iônicos sensíveis a ácido, hormônio liberador de corticotropina, ansiedade e depressão, eixo hipotálamo-hipófise-adrenal