Clear Sky Science · nl
Het zuurstofgevoelige ionkanaal 1a moduleert angst- en depressiegerelateerd gedrag via zijn invloed op de activiteit van corticotropine-releasing hormone-expressende neuronen in de hypothalamische paraventriculaire nucleus bij mannelijke muizen
Hoe een klein schakelaarretje in de hersenen onze stressniveaus bepaalt
Stress is een vertrouwd onderdeel van het moderne leven, maar onder de oppervlakte wordt het gestuurd door nauwkeurige elektrische en chemische signalen in de hersenen. Deze studie bij mannelijke muizen onthult een eerder onopgemerkte speler in dat systeem: een klein "zuurgevoelig" kanaal in specifieke stressregulerende neuronen. Door te laten zien hoe dit kanaal stresshormonen en angst- of depressieachtig gedrag versterkt — en hoe blokkering het zowel hersenen als lichaam kalmeert — wijst het werk op nieuwe soorten behandelingen voor angst, depressie en andere stressgerelateerde aandoeningen.
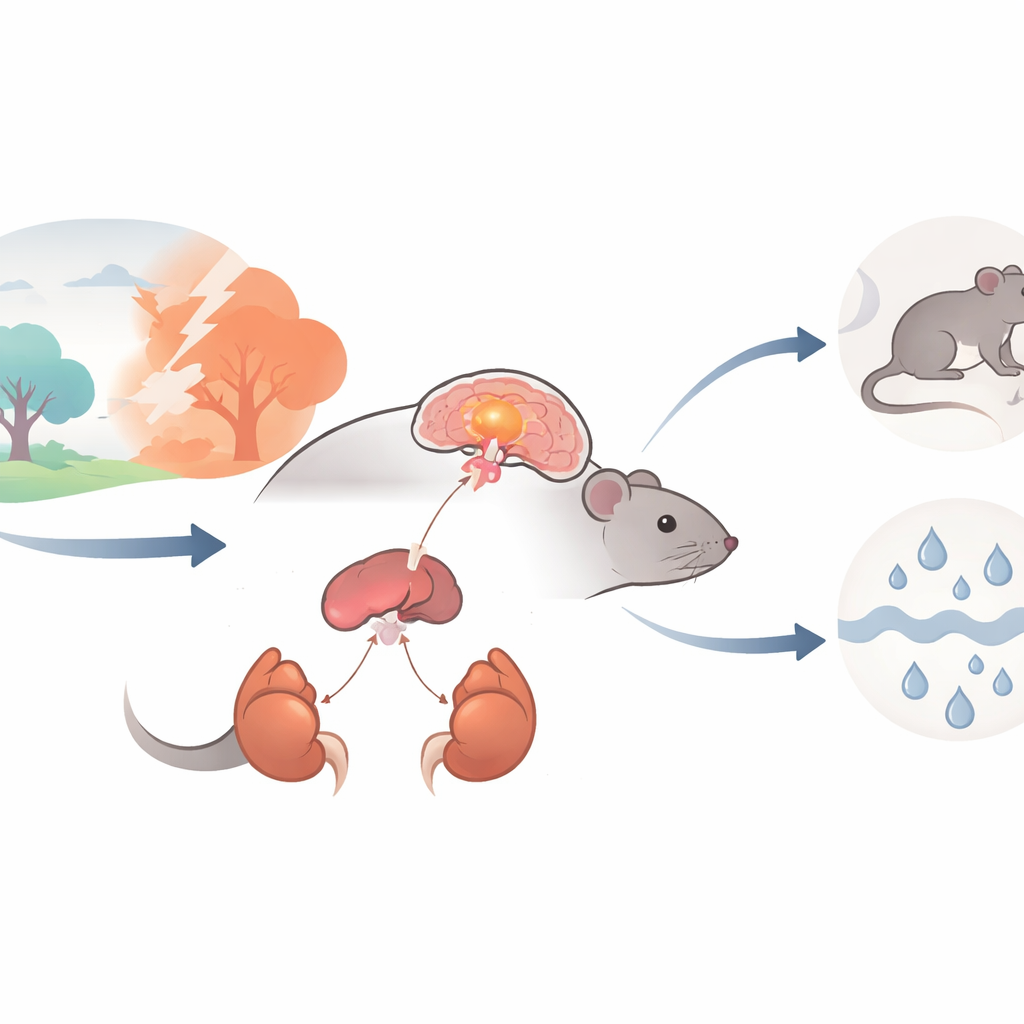
Het belangrijkste stressalarm van het lichaam
Wanneer we een uitdaging tegenkomen, treedt een commandoketen in werking die de hypothalamus–hypofyse–bijnier (HPA) as wordt genoemd. Deze begint in een kleine hersenregio, de paraventriculaire nucleus van de hypothalamus (PVN), waar gespecialiseerde zenuwcellen corticotropin-releasing hormone (CRH) afgeven. CRH geeft een signaal aan de hypofyse, die op haar beurt de bijnieren bovenop de nieren instrueert om de bloedbaan te overspoelen met stresshormonen zoals corticosteron. Deze hormonen zijn essentieel voor overleving op korte termijn, maar wanneer dit alarm te sterk of te vaak wordt geactiveerd, kan het bijdragen aan angst, depressie, stofwisselingsziekten en hoge bloeddruk. De auteurs onderzochten of een specifiek ionkanaal, ASIC1a genoemd, in CRH-producerende PVN-neuronen helpt de versterking van dit stressalarm te bepalen.
Een verborgen klep in stressneuronen
ASIC1a is een proteïne-kanaal in celmembranen dat opent wanneer de omliggende vloeistof zuurder wordt, waardoor positief geladen ionen, waaronder calcium, de cel binnenstromen. Het team bevestigde eerst dat ASIC1a overvloedig aanwezig is in CRH-producerende PVN-neuronen bij muizen. Vervolgens gebruikten ze twee aanvullende strategieën om dit kanaal te dempen. In de ene methode brachten ze een zeer selectieve ASIC1a-blokker direct in de PVN in. In de andere gebruikten ze ontworpen virussen in CRH-Cre muizen om het ASIC1a-gen specifiek in CRH-neuronen uit te schakelen. In beide gevallen gedroegen muizen zich minder angstig in exploratietests en vertoonden ze minder depressieachtige tekenen in klassieke gedragsassays, hoewel hun algemene beweging en snelheid ongewijzigd bleven. Tegelijkertijd daalden hun bloedspiegels van de stresshormonen ACTH en corticosteron na een acute stressor, terwijl de basale hormoonspiegels normaal bleven. Samen suggereren deze bevindingen dat ASIC1a niet nodig is voor gewone functies maar wel bijdraagt aan de overreactie op stress.
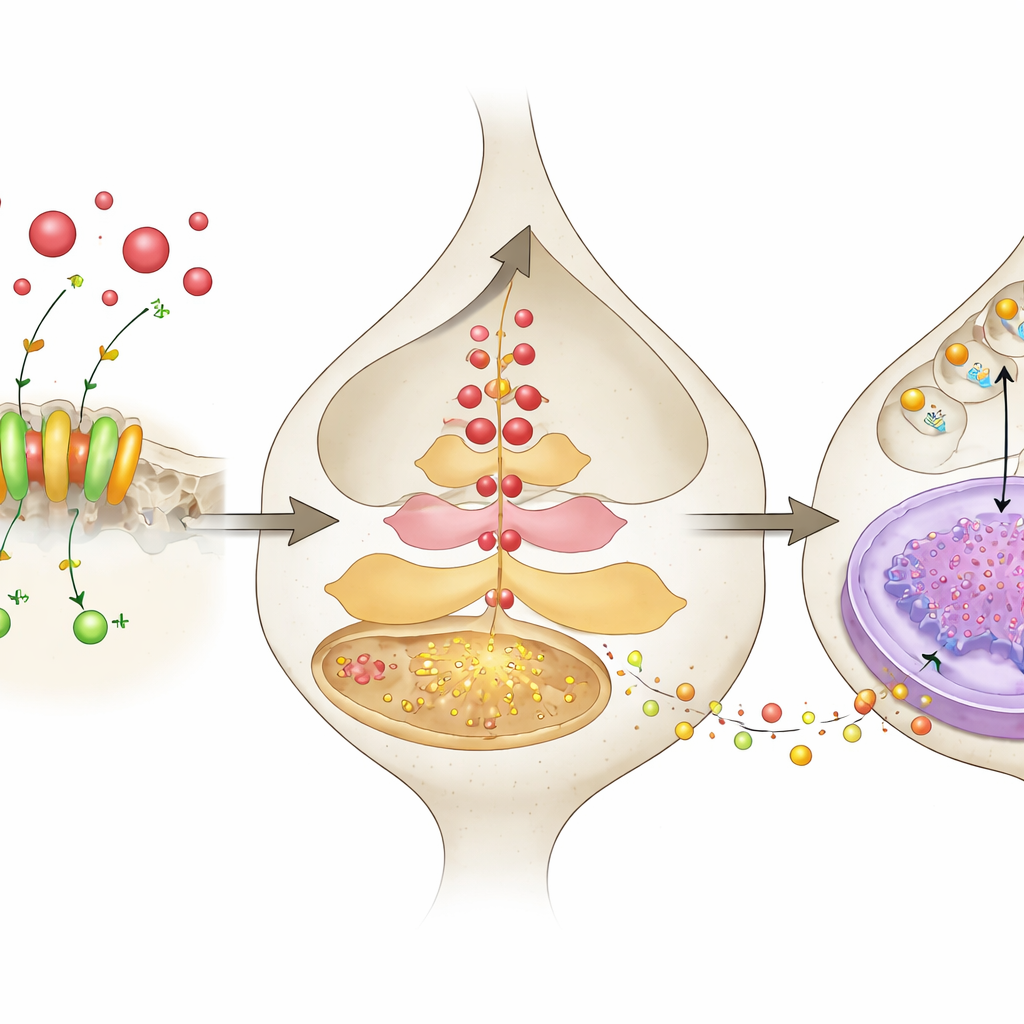
Inzoomen: van zuurprikkels naar afgifte van stresshormonen
Om te onderzoeken wat er in de neuronen gebeurt, registreerden de onderzoekers realtime calciumactiviteit van CRH PVN-neuronen met een fluorescerende reporter die door een virus werd afgeleverd en uitgelezen via optische vezels in ontwakende muizen. Tijdens stressvolle gebeurtenissen zoals een elektrische schok of een gedwongen zwemproef toonden neuronen met normaal aanwezige ASIC1a sterke uitbarstingen van calciumsignalen, terwijl neuronen zonder ASIC1a veel zwakker reageerden. In celkweken verhoogde het kort verlagen van de pH van de omgevende oplossing — wat een zuurdere omgeving nabootst — scherp de CRH-afgifte, maar dit effect werd afgezwakt wanneer ASIC1a werd geblokkeerd of uitgeschakeld. De zuurpuls verhoogde ook de CRH-productie in de cellen, zowel op eiwit- als op boodschapper-RNA-niveau, opnieuw afhankelijk van ASIC1a. Deze experimenten koppelen buitenneuronaire zuurtegraad, het openen van ASIC1a, calciuminstroom en verhoogde CRH-uitvoer als onderdelen van één cascade.
De interne schakel: een calcium-gedreven signaalcascade
Het team ontleedde vervolgens de signaalketen tussen calciuminstroom en activering van het CRH-gen. Wanneer ASIC1a door zure omstandigheden werd gestimuleerd, stegen de niveaus van een geactiveerde vorm van het enzym CaMKII, evenals de niveaus van c-Fos, een snel reagerende transcriptiefactor die bekendstaat om het inschakelen van stressgerelateerde genen. Het blokkeren van ASIC1a of zijn ionenstroom verminderde deze veranderingen. Met een medicijn dat interfereert met AP-1, het eiwitcomplex waar c-Fos deel van uitmaakt, dempten de onderzoekers de zuurgestuurde toename van CRH-productie en -afgifte in gekweekte neuronen. Het infunderen van deze AP-1-blokker in de PVN van muizen verminderde ook angst- en depressieachtig gedrag. Deze resultaten ondersteunen een model waarin ASIC1a-gedreven calciumsignalen CaMKII en c-Fos activeren, die vervolgens het CRH-gen omhoog schakelen en zo de stressreactie versterken.
Wat dit betekent voor toekomstige behandelingen
Simpel gezegd identificeert de studie ASIC1a in CRH-producerende PVN-neuronen als een moleculaire "volumeknop" op de belangrijkste stressweg van de hersenen. Wanneer ASIC1a sterk actief is, vuren stressneuronen krachtiger, schieten stresshormonen hoger omhoog en vertonen dieren meer angstig en depressieachtig gedrag. Het dempen van ASIC1a — met precieze genetische instrumenten of met geneesmiddelen — verzacht deze reactie zonder normaal gedrag uit te schakelen. Hoewel het werk werd uitgevoerd bij mannelijke muizen en zich richtte op acute stress, suggereert het dat medicijnen die ASIC1a of zijn calcium-gedreven signaalpartners richten, mogelijk een nieuwe route kunnen bieden voor de behandeling van stressgerelateerde aandoeningen zoals angst, depressie en zelfs sommige stofwisselingsziekten.
Bronvermelding: Yue, J., Zhang, Q., Wang, M. et al. The acid-sensing ion channel 1a modulates anxiety- and depression-related behaviors via its influencing on the activity of corticotropin-releasing hormone-expressing neurons in the hypothalamic paraventricular nucleus in male mice. Transl Psychiatry 16, 189 (2026). https://doi.org/10.1038/s41398-026-03946-2
Trefwoorden: stressreactie, zuurstofgevoelige ionkanalen, corticotropin-releasing hormone, angst en depressie, hypothalamus-hypofyse-bijnier as