Clear Sky Science · de
Der säureempfindliche Ionenkanal 1a moduliert angst- und depressionsähnliches Verhalten über seinen Einfluss auf die Aktivität corticotropin-freisetzender Hormon-exprimierender Neurone im hypothalamischen paraventrikulären Nukleus bei männlichen Mäusen
Wie ein winziger Schalter im Gehirn unser Stressniveau formt
Stress ist ein vertrauter Teil des modernen Lebens, wird aber unter der Oberfläche von präzisen elektrischen und chemischen Signalen im Gehirn gesteuert. Diese Studie an männlichen Mäusen enthüllt einen bislang verborgenen Akteur in diesem System: einen kleinen „säureempfindlichen“ Kanal in bestimmten Stress-Kommando-Neuronen. Indem gezeigt wird, wie dieser Kanal Stresshormone sowie ängstliches oder depressionsähnliches Verhalten verstärkt — und wie seine Blockade sowohl Gehirn als auch Körper beruhigt — deutet die Arbeit auf neue Behandlungsansätze für Angststörungen, Depressionen und andere stressassoziierte Erkrankungen hin.
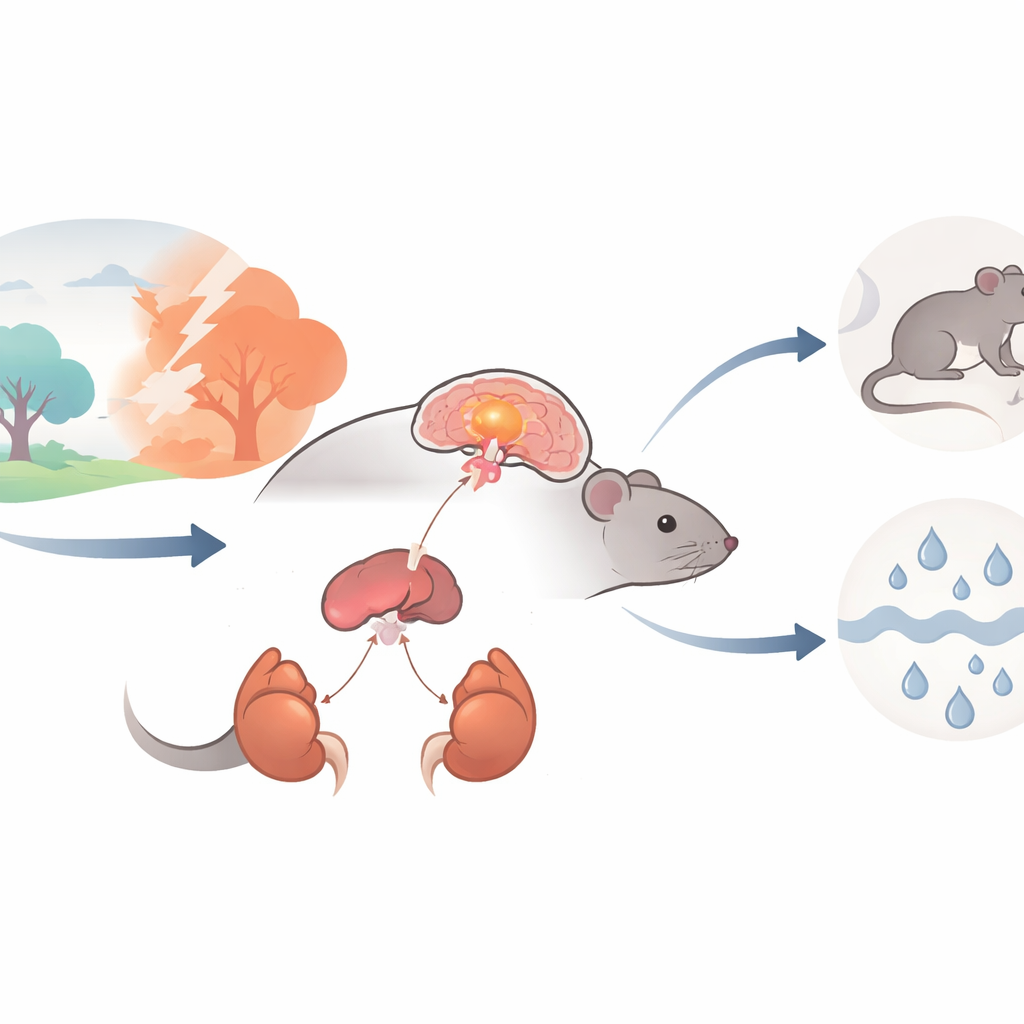
Der wichtigste Stressalarm des Körpers
Wenn wir einer Herausforderung gegenüberstehen, tritt eine Befehlskette in Aktion, die als Hypothalamus–Hypophysen–Nebennieren-(HPA-)Achse bezeichnet wird. Sie beginnt in einer kleinen Gehirnregion, dem paraventrikulären Nukleus des Hypothalamus (PVN), in der spezielle Nervenzellen das corticotropin-releasing hormone (CRH) freisetzen. CRH signalisiert der Hypophyse, die dann den Nebennieren über den Nieren befiehlt, den Blutkreislauf mit Stresshormonen wie Corticosteron zu fluten. Diese Hormone sind für das Überleben in kurzen Phasen essentiell, doch wenn dieser Alarm zu stark oder zu häufig ausgelöst wird, kann das zu Angst, Depression, Stoffwechselerkrankungen und Bluthochdruck beitragen. Die Autorinnen und Autoren fragten, ob ein bestimmter Ionenkanal, genannt ASIC1a, in CRH-produzierenden PVN-Neuronen die Verstärkung dieses Stressalarms mitbestimmt.
Ein verborgenes Ventil in Stressneuronen
ASIC1a ist ein Proteinkanals in Zellmembranen, der sich öffnet, wenn die umgebende Flüssigkeit saurer wird, und positiv geladene Ionen, darunter Calcium, in die Zelle strömen lässt. Das Team bestätigte zunächst, dass ASIC1a in CRH-produzierenden PVN-Neuronen von Mäusen reichlich vorkommt. Anschließend verwendeten sie zwei komplementäre Strategien, um diesen Kanal herunterzuregeln. In der einen infundierten sie einen hochselektiven ASIC1a-Blocker direkt in den PVN. In der anderen setzten sie gentechnisch veränderte Viren in CRH-Cre-Mäusen ein, um das ASIC1a-Gen spezifisch in CRH-Neuronen stumm zu schalten. In beiden Fällen zeigten die Mäuse in Erkundungstests weniger ängstliches Verhalten und in klassischen Verhaltensassays weniger depressionsähnliche Anzeichen, obwohl ihre Gesamtbewegung und Geschwindigkeit unverändert blieben. Gleichzeitig sanken nach einem akuten Stressor die Blutwerte der Stresshormone ACTH und Corticosteron, während die Basalwerte der Hormone normal blieben. Zusammengenommen deuten diese Befunde darauf hin, dass ASIC1a für die normale Funktion nicht erforderlich ist, wohl aber die Überreaktion auf Stress antreibt.
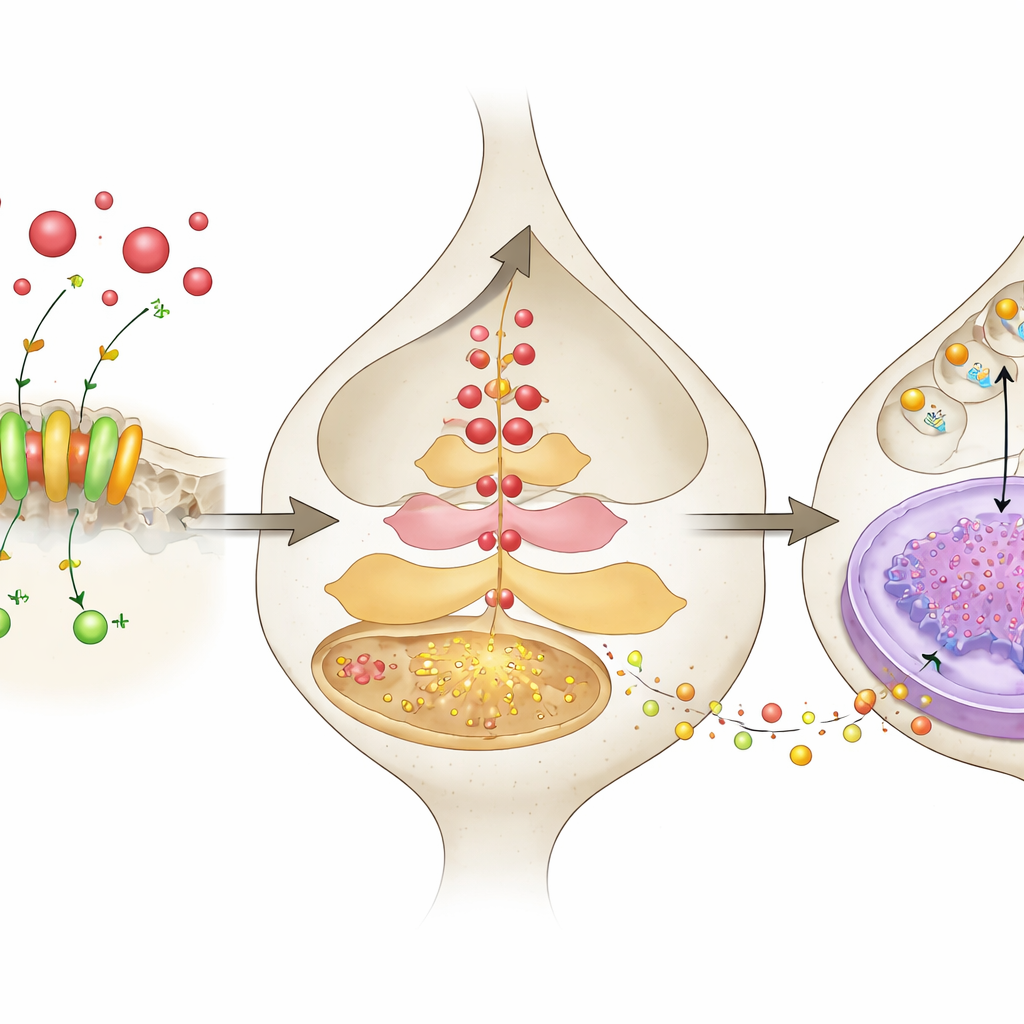
Ins Detail: Von Säuresignalen zur Freisetzung von Stresshormonen
Um zu untersuchen, was in den Neuronen geschieht, zeichneten die Forschenden die Calciumaktivität von CRH-PVN-Neuronen in Echtzeit auf, indem sie einen fluoreszenten Reporter per Virus einschleusten und diesen mit Lichtleitfasern bei wachen Mäusen auslasen. Während stressiger Ereignisse wie einem Fußschock oder einem erzwungenen Schwimmen zeigten Neurone mit normalem ASIC1a starke Calcium-Ausbrüche, während Neurone ohne ASIC1a deutlich schwächer reagierten. In Zellkulturen führte ein kurzzeitiges Absenken des pH-Werts der umgebenden Lösung — als Nachahmung einer sauren Umgebung — zu einer starken Erhöhung der CRH-Freisetzung, doch dieser Effekt wurde abgeschwächt, wenn ASIC1a blockiert oder herunterreguliert war. Der Säurereiz steigerte außerdem die CRH-Produktion innerhalb der Zellen auf Protein- und mRNA-Ebene, wiederum abhängig von ASIC1a. Diese Experimente verbinden äußere Azidität, das Öffnen von ASIC1a, Calciumeinstrom und erhöhte CRH-Ausschüttung als Teile einer einzigen Kaskade.
Die innere Schaltstelle: Eine calciumgetriebene Signalkette
Das Team untersuchte anschließend die Signalkette zwischen Calciumeinstrom und Aktivierung des CRH-Gens. Wenn ASIC1a durch saure Bedingungen aktiviert wurde, stiegen die Spiegel einer aktivierten Form des Enzyms CaMKII sowie die Spiegel von c-Fos, einem schnell wirkenden Transkriptionsfaktor, der Stress-assoziierte Gene einschaltet. Die Blockade von ASIC1a oder seines Ionenflusses verringerte diese Veränderungen. Mit einem Wirkstoff, der AP-1 — den Proteinkomplex, zu dem c-Fos gehört — beeinträchtigt, dämpften die Forschenden den säureausgelösten Anstieg der CRH-Produktion und -Freisetzung in kultivierten Neuronen. Die Infusion dieses AP-1-Blockers in den PVN von Mäusen reduzierte ebenfalls angst- und depressionsähnliches Verhalten. Diese Ergebnisse stützen ein Modell, in dem ASIC1a-vermittelte Calcium-Signale CaMKII und c-Fos aktivieren, die dann das CRH-Gen hochfahren und die Stressantwort verstärken.
Was das für künftige Behandlungen bedeutet
Kurz gesagt identifiziert die Studie ASIC1a in CRH-produzierenden PVN-Neuronen als molekularen „Lautstärkeregler“ der wichtigsten Stressbahn des Gehirns. Wenn ASIC1a stark aktiv ist, feuern Stressneurone stärker, Stresshormone steigen höher, und die Tiere zeigen mehr ängstliches und depressionsähnliches Verhalten. Das Herunterregeln von ASIC1a — sowohl mit präzisen genetischen Werkzeugen als auch mit Medikamenten — mildert diese Reaktion, ohne das normale Verhalten abzuschalten. Obwohl die Arbeit an männlichen Mäusen und unter akutem Stress durchgeführt wurde, legt sie nahe, dass Medikamente, die ASIC1a oder seine calciumgetriebenen Signalkomponenten ansprechen, eines Tages einen neuen Weg zur Behandlung stressbedingter Störungen wie Angst, Depression und sogar einiger Stoffwechselerkrankungen eröffnen könnten.
Zitation: Yue, J., Zhang, Q., Wang, M. et al. The acid-sensing ion channel 1a modulates anxiety- and depression-related behaviors via its influencing on the activity of corticotropin-releasing hormone-expressing neurons in the hypothalamic paraventricular nucleus in male mice. Transl Psychiatry 16, 189 (2026). https://doi.org/10.1038/s41398-026-03946-2
Schlüsselwörter: Stressreaktion, säureempfindliche Ionenkanäle, corticotropin-releasing hormone, Angst und Depression, Hypothalamus-Hypophysen-Nebennieren-Achse