Clear Sky Science · it
Il canale sensibile agli acidi 1a modula comportamenti correlati ad ansia e depressione influenzando l’attività dei neuroni che esprimono l’ormone di rilascio della corticotropina nel nucleo paraventricolare ipotalamico nei topi maschi
Come un piccolo interruttore cerebrale modella i nostri livelli di stress
Lo stress è un elemento familiare della vita moderna, ma al suo interno è guidato da segnali elettrici e chimici molto precisi nel cervello. Questo studio sui topi maschi svela un attore finora nascosto in quel sistema: un minuscolo canale “sensibile agli acidi” in specifici neuroni che comandano la risposta allo stress. Dimostrando come questo canale aumenti gli ormoni dello stress e i comportamenti ansiosi o depressivi — e come il suo blocco calmi sia il cervello sia il corpo — il lavoro indica nuove possibili vie terapeutiche per ansia, depressione e altre malattie legate allo stress.
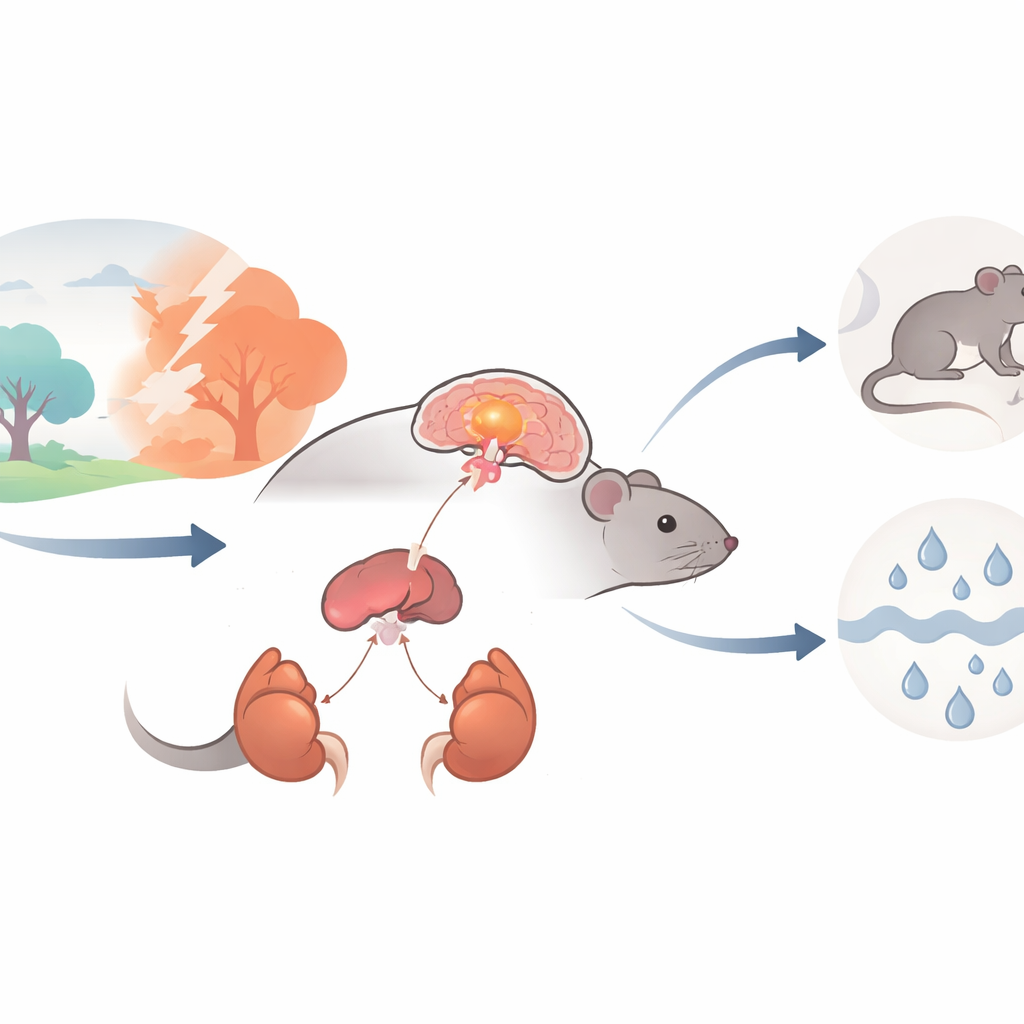
Il principale allarme dello stress nel corpo
Quando affrontiamo una sfida, entra in azione una catena di comando chiamata asse ipotalamo–ipofisi–surrene (HPA). Ha origine in una piccola regione cerebrale, il nucleo paraventricolare dell’ipotalamo (PVN), dove cellule nervose specializzate rilasciano l’ormone di rilascio della corticotropina (CRH). Il CRH segnala l’ipofisi, che a sua volta ordina alle ghiandole surrenali sopra i reni di riversare nel flusso sanguigno ormoni dello stress come il corticosterone. Questi ormoni sono essenziali per la sopravvivenza quando attivati per brevi periodi, ma se questo allarme rimane acceso troppo intensamente o troppo spesso può contribuire ad ansia, depressione, malattie metaboliche e ipertensione. Gli autori si sono chiesti se un particolare canale ionico, chiamato ASIC1a, presente nei neuroni PVN che producono CRH, contribuisca a regolare l’intensità di questo allarme.
Una valvola nascosta nei neuroni dello stress
ASIC1a è un canale proteico nelle membrane cellulari che si apre quando il fluido circostante diventa più acido, permettendo a ioni positivi, inclusi il calcio, di entrare rapidamente nella cellula. Il gruppo ha prima confermato che ASIC1a è abbondante nei neuroni PVN che producono CRH nei topi. Poi ha usato due strategie complementari per ridurne l’attività. In una, hanno infuso nel PVN un bloccante altamente selettivo di ASIC1a. Nell’altra, hanno utilizzato virus ingegnerizzati in topi CRH-Cre per silenziare specificamente il gene ASIC1a nei neuroni CRH. In entrambi i casi, i topi si comportavano con meno ansia nei test di esplorazione e mostravano meno segni di comportamento depressivo nei classici saggi comportamentali, pur mantenendo movimento e velocità complessivi invariati. Contemporaneamente, i livelli ematici degli ormoni dello stress ACTH e corticosterone dopo uno stress acuto diminuivano, mentre i livelli basali degli ormoni restavano normali. Nel complesso, questi risultati suggeriscono che ASIC1a non è necessario per la funzione ordinaria ma contribuisce a guidare la sovra-reazione allo stress.
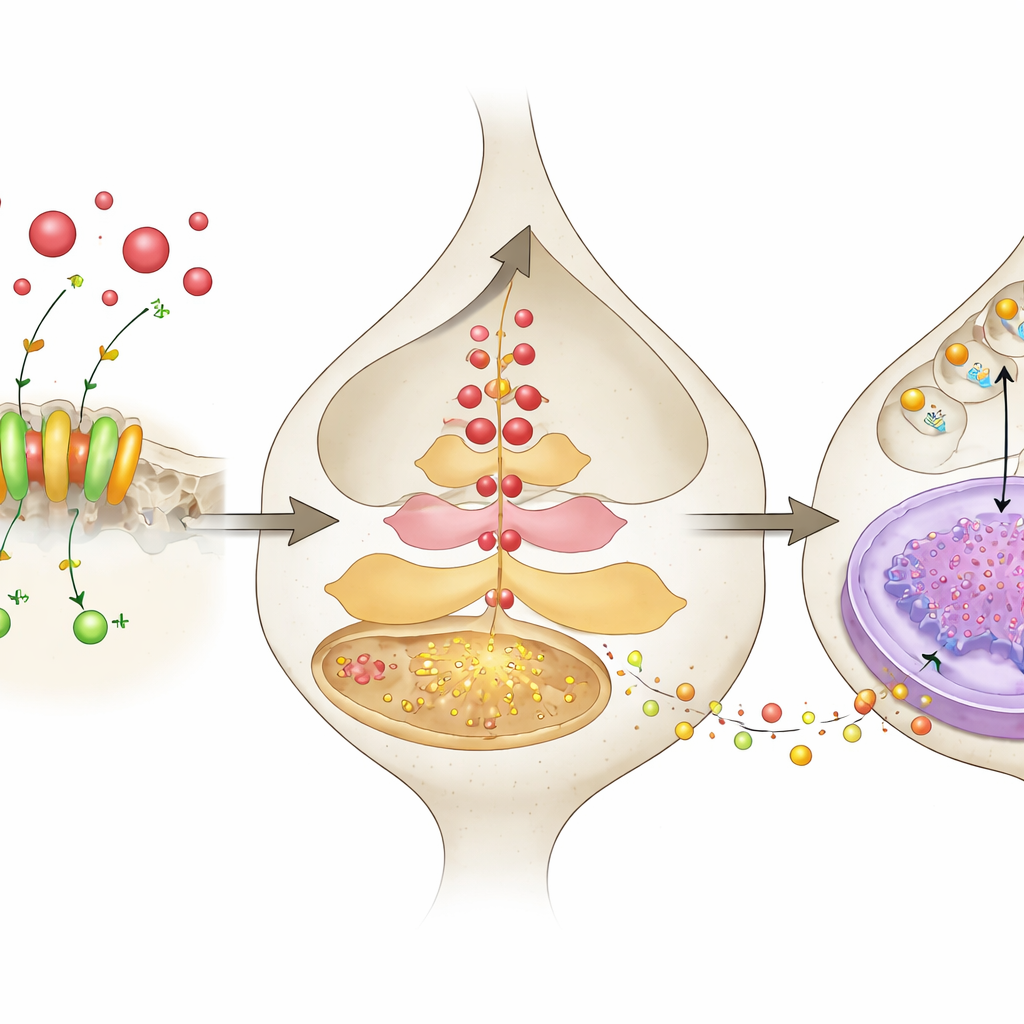
Zoom: dai segnali acidi al rilascio degli ormoni dello stress
Per indagare cosa accade all’interno dei neuroni, i ricercatori hanno registrato in tempo reale l’attività del calcio dai neuroni CRH del PVN usando un marcatore fluorescente consegnato tramite virus e letto con fibre ottiche in topi svegli. Durante eventi stressanti come una scarica elettrica al piede o il nuoto forzato, i neuroni con ASIC1a normale mostravano forti raffiche di segnali di calcio, mentre i neuroni privi di ASIC1a rispondevano in modo molto più debole. In colture cellulari, una breve diminuzione del pH della soluzione circostante — che imita un ambiente più acido — aumentava nettamente il rilascio di CRH, ma questo effetto era attenuato quando ASIC1a veniva bloccato o ridotto. L’impulso acido aumentava anche la produzione di CRH all’interno delle cellule, sia a livello di proteina sia di RNA messaggero, di nuovo in modo dipendente da ASIC1a. Questi esperimenti collegano l’acidità fuori dalla cellula, l’apertura di ASIC1a, l’ingresso di calcio e l’aumento dell’output di CRH come parti di una singola cascata.
Il circuito interno: una catena di segnali guidata dal calcio
Il gruppo ha quindi scomposto la catena di segnalazione tra l’ingresso del calcio e l’attivazione del gene CRH. Quando ASIC1a veniva stimolato da condizioni acide, aumentavano i livelli di una forma attivata dell’enzima CaMKII, così come i livelli di c-Fos, un fattore di trascrizione a rapida azione noto per attivare geni legati allo stress. Bloccare ASIC1a o il suo flusso ionico riduceva questi cambiamenti. Utilizzando un farmaco che interferisce con AP-1, il complesso proteico che include c-Fos, i ricercatori attenuavano l’aumento indotto dall’acidità nella produzione e nel rilascio di CRH nelle cellule in coltura. Infondere questo bloccante di AP-1 nel PVN dei topi riduceva anch’esso i comportamenti simili ad ansia e depressione. Questi risultati supportano un modello in cui i segnali di calcio guidati da ASIC1a attivano CaMKII e c-Fos, che quindi potenziano il gene CRH, amplificando la risposta allo stress.
Cosa significa per i trattamenti futuri
In termini semplici, lo studio identifica ASIC1a nei neuroni PVN che producono CRH come una “manopola del volume” molecolare sul principale percorso dello stress del cervello. Quando ASIC1a è molto attivo, i neuroni dello stress si attivano più intensamente, gli ormoni dello stress aumentano di più e gli animali mostrano comportamenti più ansiosi e simili alla depressione. Ridurre l’attività di ASIC1a — sia con strumenti genetici precisi sia con farmaci — attenua questa reazione senza spegnere il comportamento normale. Pur essendo il lavoro condotto su topi maschi e concentrato sullo stress acuto, suggerisce che farmaci mirati contro ASIC1a o i suoi partner di segnalazione guidati dal calcio potrebbero un giorno offrire una nuova via per trattare disturbi legati allo stress come ansia, depressione e persino alcune malattie metaboliche.
Citazione: Yue, J., Zhang, Q., Wang, M. et al. The acid-sensing ion channel 1a modulates anxiety- and depression-related behaviors via its influencing on the activity of corticotropin-releasing hormone-expressing neurons in the hypothalamic paraventricular nucleus in male mice. Transl Psychiatry 16, 189 (2026). https://doi.org/10.1038/s41398-026-03946-2
Parole chiave: risposta allo stress, canali sensibili agli acidi, ormone di rilascio della corticotropina, ansia e depressione, asse ipotalamo-ipofisi-surrene