Clear Sky Science · pl
Kanał jonowy reagujący na kwasowość 1a moduluje zachowania związane z lękiem i depresją poprzez wpływ na aktywność neuronów produkujących hormon uwalniający kortykotropinę w przykomorowym jądrze podwzgórza u samców myszy
Jak maleńki przełącznik w mózgu kształtuje nasze reakcje na stres
Stres to znajoma część współczesnego życia, ale pod powierzchnią jest napędzany precyzyjnymi sygnałami elektrycznymi i chemicznymi w mózgu. Badanie to na samcach myszy ujawnia wcześniej ukrytego uczestnika tego systemu: niewielki kanał „wyczuwający” kwasowość obecny w specyficznych neuronach sterujących stresem. Pokazując, jak ten kanał zwiększa wydzielanie hormonów stresu oraz nasila zachowania lękowe i depresyjne — i jak jego zablokowanie uspokaja zarówno mózg, jak i ciało — praca ta wskazuje nowe kierunki terapii lęku, depresji i innych chorób związanych ze stresem.
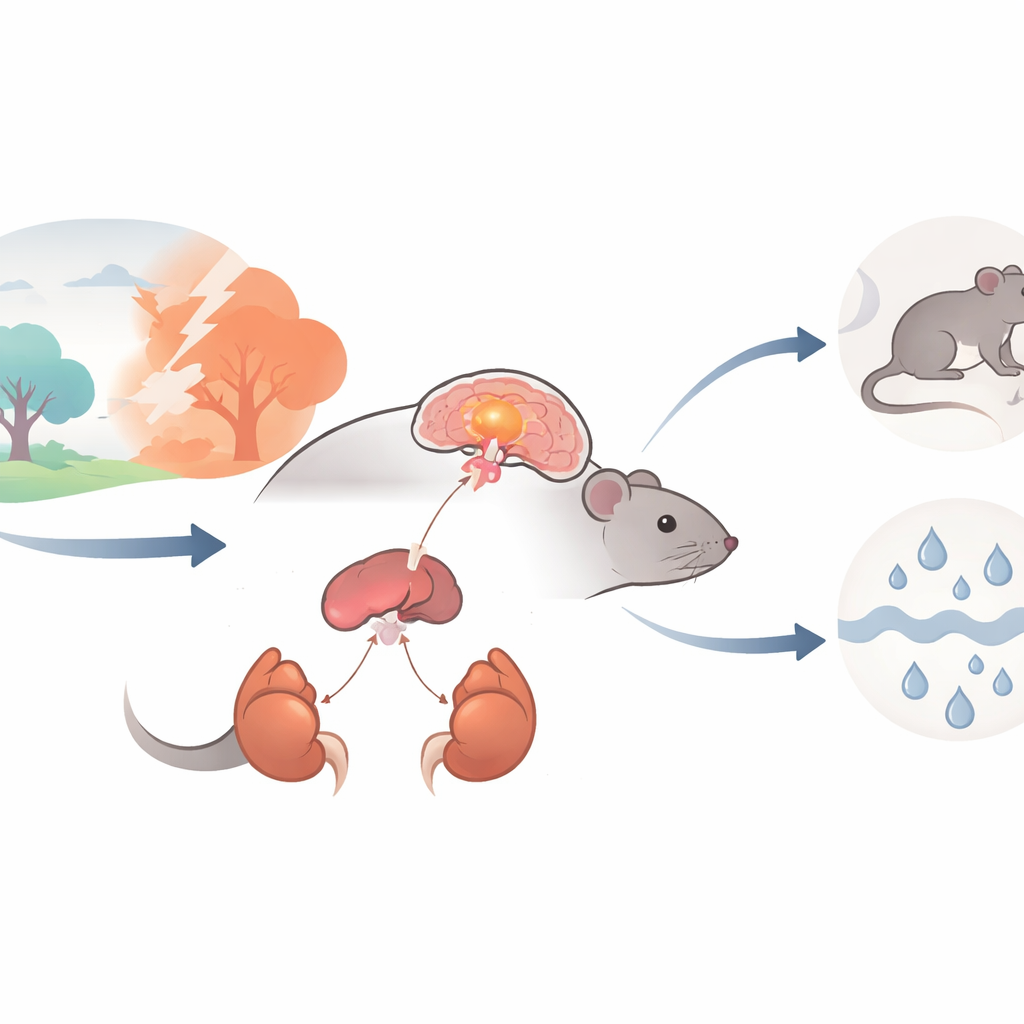
Główny alarm stresowy organizmu
Kiedy stajemy przed wyzwaniem, uruchamia się łańcuch dowodzenia zwany osią podwzgórze–przysadka–nadnercza (HPA). Zaczyna się w małym obszarze mózgu, przykomorowym jądrze podwzgórza (PVN), gdzie specjalne komórki nerwowe uwalniają hormon uwalniający kortykotropinę (CRH). CRH wysyła sygnał do przysadki, która z kolei nakazuje nadnerczom na szczycie nerek uwolnić do krwiobiegu hormony stresu, takie jak kortykosteron. Hormony te są niezbędne do przetrwania przy krótkotrwałych zagrożeniach, ale jeśli alarm działa zbyt mocno lub zbyt często, może przyczyniać się do lęku, depresji, chorób metabolicznych i nadciśnienia. Autorzy postawili pytanie, czy określony kanał jonowy, zwany ASIC1a, obecny w neuronach PVN produkujących CRH, pomaga regulować siłę tego alarmu.
Ukrywany zawór w neuronach stresowych
ASIC1a to białkowy kanał w błonie komórkowej, który otwiera się, gdy otaczający płyn staje się bardziej kwaśny, pozwalając dodatnio naładowanym jonów, w tym wapniowi, gwałtownie napłynąć do komórki. Zespół najpierw potwierdził, że ASIC1a jest obficie obecny w neuronach PVN produkujących CRH u myszy. Następnie zastosowali dwie uzupełniające się strategie osłabienia działania tego kanału. W jednej bezpośrednio winfudowali do PVN wysoce selektywny bloker ASIC1a. W drugiej użyli zmodyfikowanych wirusów u myszy CRH-Cre, aby wyciszyć gen ASIC1a specyficznie w neuronach CRH. W obu przypadkach myszy wykazywały mniejszą skłonność do zachowań lękowych w testach eksploracyjnych i mniej oznak podobnych do depresji w klasycznych testach behawioralnych, mimo że ich ogólna aktywność i prędkość poruszania się pozostały niezmienione. Jednocześnie poziomy we krwi hormonów stresu ACTH i kortykosteronu po ostrej stresującej sytuacji spadły, podczas gdy poziomy podstawowe pozostały normalne. Razem wyniki te sugerują, że ASIC1a nie jest niezbędny do zwykłego funkcjonowania, ale pomaga napędzać nadmierną reakcję na stres.
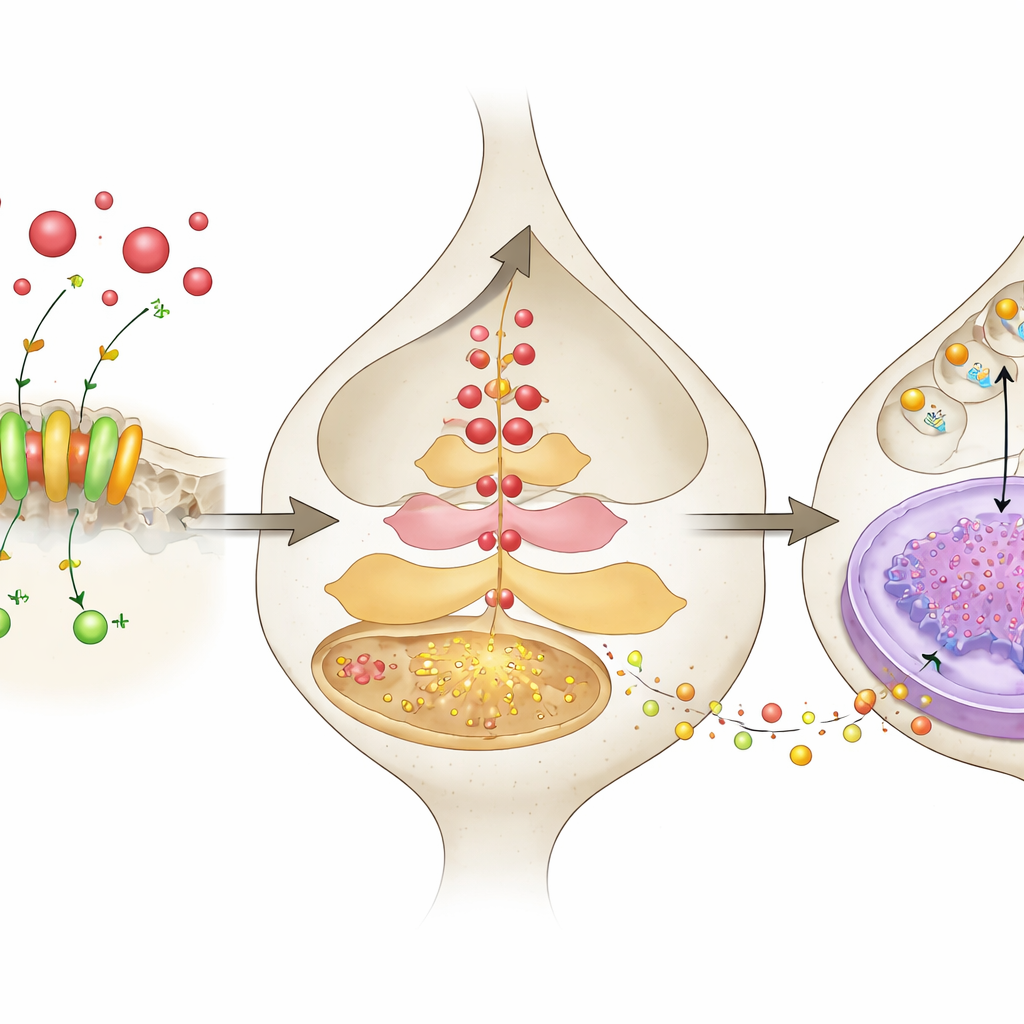
Zbliżenie: od sygnałów kwasowych do uwalniania hormonów stresu
Aby zbadać, co dzieje się wewnątrz neuronów, badacze rejestrowali aktywność wapniową w czasie rzeczywistym w neuronach CRH PVN przy użyciu fluorescencyjnego reportera dostarczonego wirusem i odczytywanego za pomocą włókien optycznych u przebudzonych myszy. Podczas stresujących zdarzeń, takich jak porażenie elektryczne łapy czy przymusowe pływanie, neurony z prawidłowym ASIC1a wykazywały silne serie sygnałów wapniowych, podczas gdy neurony pozbawione ASIC1a reagowały znacznie słabiej. W hodowlach komórkowych krótkotrwałe obniżenie pH otaczającego roztworu — naśladujące bardziej kwaśne środowisko — wyraźnie zwiększało uwalnianie CRH, ale efekt ten był osłabiony, gdy ASIC1a został zablokowany lub wyciszony. Impuls kwasowy także zwiększał produkcję CRH w komórkach, zarówno na poziomie białka, jak i mRNA, ponownie w sposób zależny od ASIC1a. Te eksperymenty łączą zewnętrzną kwasowość, otwarcie ASIC1a, napływ wapnia i zwiększone wydzielanie CRH jako elementy jednego kaskadowego procesu.
Wewnętrzne przekaźnictwo: łańcuch sygnałowy napędzany wapniem
Zespół następnie rozebrał na części łańcuch sygnałowy między napływem wapnia a aktywacją genu CRH. Gdy ASIC1a był stymulowany przez kwaśne warunki, wzrastały poziomy aktywowanej formy enzymu CaMKII, podobnie jak poziomy c-Fos, szybko działającego czynnika transkrypcyjnego znanego z uruchamiania genów związanych ze stresem. Zablokowanie ASIC1a lub jego przepływu jonowego zmniejszało te zmiany. Zastosowanie leku ingerującego w AP-1, kompleks białkowy zawierający c-Fos, osłabiło kwasowo wywołany wzrost produkcji i uwalniania CRH w hodowlach neuronów. Winfudowanie tego inhibitora AP-1 do PVN myszy również łagodziło zachowania związane z lękiem i depresją. Wyniki te wspierają model, w którym sygnały wapniowe wywołane przez ASIC1a aktywują CaMKII i c-Fos, które następnie zwiększają aktywność genu CRH, wzmacniając odpowiedź na stres.
Co to znaczy dla przyszłych terapii
Krótko mówiąc, badanie identyfikuje ASIC1a w neuronach PVN produkujących CRH jako molekularny „pokrętło głośności” głównej ścieżki stresowej mózgu. Gdy ASIC1a jest silnie aktywny, neurony stresowe wybuchają większą aktywnością, poziomy hormonów stresu rosną, a zwierzęta wykazują więcej zachowań lękowych i depresyjnych. Osłabienie ASIC1a — zarówno przy użyciu precyzyjnych narzędzi genetycznych, jak i leków — łagodzi tę reakcję bez wyłączania normalnego zachowania. Choć badania przeprowadzono na samcach myszy i skupiono się na stresie ostrym, sugerują, że leki celujące w ASIC1a lub jego partnerów w sygnalizacji napędzanej wapniem mogłyby w przyszłości otworzyć nową drogę leczenia zaburzeń związanych ze stresem, takich jak lęk, depresja, a nawet niektóre choroby metaboliczne.
Cytowanie: Yue, J., Zhang, Q., Wang, M. et al. The acid-sensing ion channel 1a modulates anxiety- and depression-related behaviors via its influencing on the activity of corticotropin-releasing hormone-expressing neurons in the hypothalamic paraventricular nucleus in male mice. Transl Psychiatry 16, 189 (2026). https://doi.org/10.1038/s41398-026-03946-2
Słowa kluczowe: odpowiedź na stres, kanały jonowe reagujące na kwasowość, hormon uwalniający kortykotropinę, lęk i depresja